第51页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
- 第189页
- 第190页
- 第191页
- 第192页
- 第193页
- 第194页
- 第195页
- 第196页
- 第197页
- 第198页
- 第199页
- 第200页
- 第201页
- 第202页
- 第203页
- 第204页
- 第205页
- 第206页
- 第207页
- 第208页
- 第209页
- 第210页
- 第211页
- 第212页
- 第213页
- 第214页
- 第215页
- 第216页
- 第217页
- 第218页
- 第219页
- 第220页
- 第221页
- 第222页
- 第223页
- 第224页
- 第225页
- 第226页
- 第227页
- 第228页
- 第229页
- 第230页
- 第231页
- 第232页
- 第233页
- 第234页
- 第235页
- 第236页
- 第237页
- 第238页
- 第239页
- 第240页
- 第241页
- 第242页
- 第243页
- 第244页
- 第245页
- 第246页
- 第247页
- 第248页
- 第249页
- 第250页
- 第251页
- 第252页
- 第253页
- 第254页
- 第255页
- 第256页
- 第257页
- 第258页
- 第259页
- 第260页
- 第261页
铁盐和亚铁盐
(1)铁盐

F
(2)亚铁盐

(3)具体应用

【应用示例】
在CuCl₂、FeCl₃的混合溶液中加入一定量铁粉和铜粉的混合物。
(1)从氧化还原角度分析,氧化性:CuCl₂
(2)若金属全部溶解,则溶液中一定存在的金属阳离子有
(3)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有
(1)铁盐

F
(2)亚铁盐

(3)具体应用

【应用示例】
在CuCl₂、FeCl₃的混合溶液中加入一定量铁粉和铜粉的混合物。
(1)从氧化还原角度分析,氧化性:CuCl₂
<
(填“>”或“<”,下同)FeCl₃,还原性:Fe>
Cu。(2)若金属全部溶解,则溶液中一定存在的金属阳离子有
Fe²⁺、Cu²⁺
,可能存在的金属阳离子有Fe³⁺
。(3)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有
Fe²⁺
,一定不存在的金属阳离子有Fe³⁺、Cu²⁺
。
答案:
铁盐和亚铁盐
(1)铁盐
①Fe³⁺在溶液中呈棕黄色;
②Fe³⁺具有较强的氧化性,可与Cu、I⁻等还原性物质发生反应:2Fe³⁺ + Cu = Cu²⁺ + 2Fe²⁺、2Fe³⁺ + 2I⁻ = 2Fe²⁺ + I₂;
③向含有Fe³⁺的溶液中滴加KSCN溶液时,溶液变成红色
(2)亚铁盐
①含有Fe²⁺的溶液呈浅绿色;
②强还原性:Fe²⁺与Cl₂反应的离子方程式为2Fe²⁺ + Cl₂ = 2Fe³⁺ + 2Cl⁻;
③弱氧化性:Fe²⁺与Zn反应的离子方程式为Zn + Fe²⁺ = Fe + Zn²⁺
(3)具体应用
溶液配制和保存
Fe²⁺的盐溶液:加少量铁粉,防止Fe²⁺被氧化;加少量相应的酸,抑制Fe²⁺水解
Fe³⁺的盐溶液:加少量相应的酸,抑制Fe³⁺水解
物质的制备
制备无水FeCl₃:在干燥的HCl气流中加热蒸干FeCl₃溶液
制备Fe(OH)₃胶体:向沸水中加入饱和FeCl₃溶液并继续加热至液体呈红褐色
【应用示例】
在CuCl₂、FeCl₃的混合溶液中加入一定量铁粉和铜粉的混合物。
(1)从氧化还原角度分析,氧化性:CuCl₂<FeCl₃,还原性:Fe>Cu。
(2)若金属全部溶解,则溶液中一定存在的金属阳离子有Fe²⁺、Cu²⁺,可能存在的金属阳离子有Fe³⁺。
(3)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有Fe²⁺,一定不存在的金属阳离子有Fe³⁺、Cu²⁺。
(1)铁盐
①Fe³⁺在溶液中呈棕黄色;
②Fe³⁺具有较强的氧化性,可与Cu、I⁻等还原性物质发生反应:2Fe³⁺ + Cu = Cu²⁺ + 2Fe²⁺、2Fe³⁺ + 2I⁻ = 2Fe²⁺ + I₂;
③向含有Fe³⁺的溶液中滴加KSCN溶液时,溶液变成红色
(2)亚铁盐
①含有Fe²⁺的溶液呈浅绿色;
②强还原性:Fe²⁺与Cl₂反应的离子方程式为2Fe²⁺ + Cl₂ = 2Fe³⁺ + 2Cl⁻;
③弱氧化性:Fe²⁺与Zn反应的离子方程式为Zn + Fe²⁺ = Fe + Zn²⁺
(3)具体应用
溶液配制和保存
Fe²⁺的盐溶液:加少量铁粉,防止Fe²⁺被氧化;加少量相应的酸,抑制Fe²⁺水解
Fe³⁺的盐溶液:加少量相应的酸,抑制Fe³⁺水解
物质的制备
制备无水FeCl₃:在干燥的HCl气流中加热蒸干FeCl₃溶液
制备Fe(OH)₃胶体:向沸水中加入饱和FeCl₃溶液并继续加热至液体呈红褐色
【应用示例】
在CuCl₂、FeCl₃的混合溶液中加入一定量铁粉和铜粉的混合物。
(1)从氧化还原角度分析,氧化性:CuCl₂<FeCl₃,还原性:Fe>Cu。
(2)若金属全部溶解,则溶液中一定存在的金属阳离子有Fe²⁺、Cu²⁺,可能存在的金属阳离子有Fe³⁺。
(3)若剩余固体中有铁和铜,则溶液中一定存在的金属阳离子有Fe²⁺,一定不存在的金属阳离子有Fe³⁺、Cu²⁺。
例1(教材改编题)欲探究铁及其化合物的还原性或氧化性,可供选用的试剂有:铁粉、FeCl₃溶液、FeCl₂溶液、氯水、酸性KMnO₄溶液、锌片。下列说法中不正确的是(
A.在FeCl₂溶液中加入锌片,溶液由浅绿色变为无色:Zn + Fe²⁺ = Zn²⁺ + Fe
B.在FeCl₃溶液中加入足量铁粉,溶液由棕黄色变为浅绿色,体现Fe³⁺的氧化性
C.在酸性KMnO₄溶液中滴加足量FeCl₂溶液,溶液的紫红色逐渐褪去,体现Fe²⁺的还原性
D.在FeCl₂溶液中滴加氯水,溶液由浅绿色变为棕黄色:2Fe²⁺ + Cl₂ = 2Fe³⁺ + 2Cl⁻
C
)A.在FeCl₂溶液中加入锌片,溶液由浅绿色变为无色:Zn + Fe²⁺ = Zn²⁺ + Fe
B.在FeCl₃溶液中加入足量铁粉,溶液由棕黄色变为浅绿色,体现Fe³⁺的氧化性
C.在酸性KMnO₄溶液中滴加足量FeCl₂溶液,溶液的紫红色逐渐褪去,体现Fe²⁺的还原性
D.在FeCl₂溶液中滴加氯水,溶液由浅绿色变为棕黄色:2Fe²⁺ + Cl₂ = 2Fe³⁺ + 2Cl⁻
答案:
例1 C 解析 由于还原性:Zn>Fe,向FeCl₂溶液中加入锌片,锌置换出铁,溶液由浅绿色变为无色,A正确;在FeCl₃溶液中加入足量铁粉,发生反应2FeCl₃ + Fe = 3FeCl₂,溶液由棕黄色变为浅绿色,体现Fe³⁺的氧化性,B正确;在酸性KMnO₄溶液中滴加足量FeCl₂溶液,溶液的紫红色逐渐褪去,由于Fe²⁺、Cl⁻均能将MnO₄⁻还原为Mn²⁺而使溶液褪色,故不能说明Fe²⁺具有还原性,C错误;在FeCl₂溶液中滴加氯水,Cl₂将FeCl₂氧化生成FeCl₃,溶液由浅绿色变为棕黄色,D正确。
[对点训练1]
(2024·七省适应性测试广西化学,8)实验小组用过量FeCl₃溶液处理覆铜板得到浸出液,并对其中的物质进行回收,流程如下。下列有关说法正确的是(
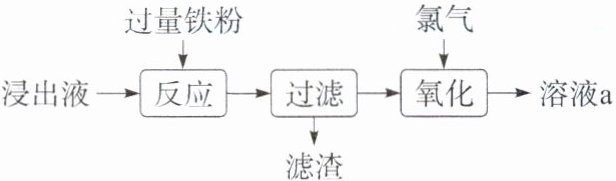
浸出液→(过量铁粉,反应)→(过滤)→(滤渣,氯气,氧化)→溶液a
A.浸出液呈中性
B.滤渣只有铜粉
C.用KSCN溶液检验是否“氧化”完全
D.溶液a回收后可用于处理覆铜板
(2024·七省适应性测试广西化学,8)实验小组用过量FeCl₃溶液处理覆铜板得到浸出液,并对其中的物质进行回收,流程如下。下列有关说法正确的是(
D
)
浸出液→(过量铁粉,反应)→(过滤)→(滤渣,氯气,氧化)→溶液a
A.浸出液呈中性
B.滤渣只有铜粉
C.用KSCN溶液检验是否“氧化”完全
D.溶液a回收后可用于处理覆铜板
答案:
对点训练1 D 解析 用过量FeCl₃溶液处理覆铜板时发生反应:2FeCl₃ + Cu = 2FeCl₂ + CuCl₂,所得浸出液中含有FeCl₃、FeCl₂和CuCl₂,由于Fe³⁺、Fe²⁺和Cu²⁺均发生水解反应,故浸出液呈酸性,A错误;由于铁粉过量,则滤渣中还有铁单质,B错误;“氧化”步骤通入Cl₂,将FeCl₂氧化生成FeCl₃,检验是否“氧化”完全的实质是检验溶液中是否含有Fe²⁺,不能用KSCN溶液检验,应加入K₃[Fe(CN)₆]溶液看是否生成蓝色沉淀,C错误;溶液a中含有FeCl₃,回收后可用于处理覆铜板,D正确。
例2(教材改编题)某实验小组同学为了检验某FeCl₃溶液中是否含有FeCl₂,设计了如下实验方案,其中最合理的是(
A.加入适量铜粉,观察溶液是否变蓝
B.先滴加氯水,再滴加KSCN溶液,观察溶液是否变红
C.滴加酸性KMnO₄溶液,观察溶液是否褪色
D.滴加K₃[Fe(CN)₆]溶液,观察是否生成蓝色沉淀
D
)A.加入适量铜粉,观察溶液是否变蓝
B.先滴加氯水,再滴加KSCN溶液,观察溶液是否变红
C.滴加酸性KMnO₄溶液,观察溶液是否褪色
D.滴加K₃[Fe(CN)₆]溶液,观察是否生成蓝色沉淀
答案:
例2 D 解析 加入适量铜粉无法检验FeCl₃,A错误;先滴加氯水,Cl₂可将FeCl₂氧化生成FeCl₃,不能判断是否含有FeCl₃,B错误;Fe²⁺、Cl⁻都能被酸性KMnO₄溶液氧化,不能判断是否含有FeCl₂,C错误;若FeCl₃溶液中含有FeCl₂,滴加K₃[Fe(CN)₆]溶液,反应生成蓝色沉淀KFe[Fe(CN)₆],实验现象最明显,该方案最合理,D正确。
查看更多完整答案,请扫码查看


