2025年赢在微点化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年赢在微点化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第66页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
- 第189页
- 第190页
- 第191页
- 第192页
- 第193页
- 第194页
- 第195页
- 第196页
- 第197页
- 第198页
- 第199页
- 第200页
- 第201页
- 第202页
- 第203页
- 第204页
- 第205页
- 第206页
- 第207页
- 第208页
- 第209页
- 第210页
- 第211页
- 第212页
- 第213页
- 第214页
- 第215页
- 第216页
- 第217页
- 第218页
- 第219页
- 第220页
- 第221页
- 第222页
- 第223页
- 第224页
- 第225页
- 第226页
- 第227页
- 第228页
- 第229页
- 第230页
- 第231页
- 第232页
- 第233页
- 第234页
- 第235页
- 第236页
- 第237页
- 第238页
- 第239页
- 第240页
- 第241页
- 第242页
- 第243页
- 第244页
- 第245页
- 第246页
- 第247页
- 第248页
- 第249页
- 第250页
- 第251页
- 第252页
- 第253页
- 第254页
- 第255页
- 第256页
- 第257页
- 第258页
- 第259页
- 第260页
- 第261页
- 第262页
- 第263页
- 第264页
- 第265页
- 第266页
- 第267页
- 第268页
- 第269页
- 第270页
- 第271页
- 第272页
- 第273页
- 第274页
- 第275页
- 第276页
- 第277页
- 第278页
- 第279页
- 第280页
- 第281页
- 第282页
- 第283页
- 第284页
- 第285页
- 第286页
- 第287页
- 第288页
- 第289页
- 第290页
- 第291页
- 第292页
- 第293页
- 第294页
- 第295页
- 第296页
- 第297页
- 第298页
- 第299页
- 第300页
- 第301页
- 第302页
- 第303页
- 第304页
- 第305页
- 第306页
- 第307页
- 第308页
- 第309页
- 第310页
- 第311页
- 第312页
- 第313页
- 第314页
- 第315页
- 第316页
- 第317页
- 第318页
- 第319页
- 第320页
- 第321页
7.用如图所示装置(夹持仪器省略)制备氢氧化亚铁。
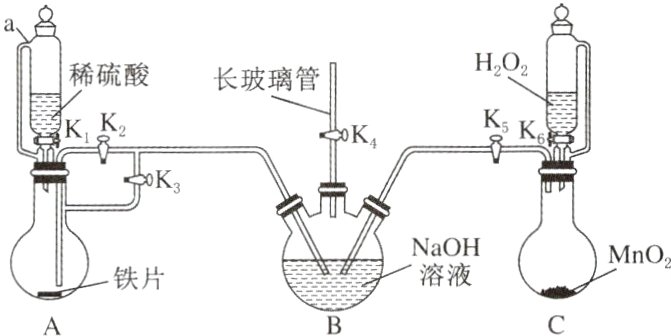
实验步骤如下:
Ⅰ.检查装置气密性后,关闭K₂、K₅,打开K₁、K₃、K₄,使装置A中产生的气体进入装置B中,排尽B中空气。
Ⅱ.待B中空气排尽后,关闭K₃,打开K₂,将A中溶液压入B中并观察现象。
Ⅲ.关闭K₁、K₂,打开K₅、K₆,使C中气体通入B中并观察现象。
回答下列问题:
(1)仪器a的名称是__________,B中长玻璃管的作用是______________________________。
(2)装置A中金属离子的检验方法是________。
(3)步骤Ⅲ装置B中的现象是______________,其发生反应的化学方程式为______________________________。

实验步骤如下:
Ⅰ.检查装置气密性后,关闭K₂、K₅,打开K₁、K₃、K₄,使装置A中产生的气体进入装置B中,排尽B中空气。
Ⅱ.待B中空气排尽后,关闭K₃,打开K₂,将A中溶液压入B中并观察现象。
Ⅲ.关闭K₁、K₂,打开K₅、K₆,使C中气体通入B中并观察现象。
回答下列问题:
(1)仪器a的名称是__________,B中长玻璃管的作用是______________________________。
(2)装置A中金属离子的检验方法是________。
(3)步骤Ⅲ装置B中的现象是______________,其发生反应的化学方程式为______________________________。
答案:
答案
(1)恒压滴液漏斗 平衡气压,辅助排出装置B中的空气
(2)取少量装置A烧瓶中的液体于洁净试管中,滴加几滴$KSCN$溶液,无红色出现,再滴加$H_{2}O_{2}$,溶液变为红色,则证明存在$Fe^{2+}$或加入铁氰化钾溶液,产生蓝色沉淀,证明存在$Fe^{2+}$
(3)白色沉淀逐渐变为灰绿色,最后变为红褐色 $4Fe(OH)_{2} + O_{2} + 2H_{2}O = 4Fe(OH)_{3}$
解析 氢氧化亚铁容易被氧气氧化,因此打开$K_{1}$、$K_{3}$、$K_{4}$,关闭$K_{2}$和$K_{5}$,装置A中产生$H_{2}$,排出装置B中的空气,因此长导管作用之一是辅助排出装置B中的空气,作用之二是平衡压强,防止装置中压强过大,发生危险。
(1)恒压滴液漏斗 平衡气压,辅助排出装置B中的空气
(2)取少量装置A烧瓶中的液体于洁净试管中,滴加几滴$KSCN$溶液,无红色出现,再滴加$H_{2}O_{2}$,溶液变为红色,则证明存在$Fe^{2+}$或加入铁氰化钾溶液,产生蓝色沉淀,证明存在$Fe^{2+}$
(3)白色沉淀逐渐变为灰绿色,最后变为红褐色 $4Fe(OH)_{2} + O_{2} + 2H_{2}O = 4Fe(OH)_{3}$
解析 氢氧化亚铁容易被氧气氧化,因此打开$K_{1}$、$K_{3}$、$K_{4}$,关闭$K_{2}$和$K_{5}$,装置A中产生$H_{2}$,排出装置B中的空气,因此长导管作用之一是辅助排出装置B中的空气,作用之二是平衡压强,防止装置中压强过大,发生危险。
1.判断正误,正确的画“√”,错误的画“×”。
(1)古壁画颜料中所用的铁红,其成分为Fe₂O₃。(2023·新课标卷)( )
(2)Fe₂O₃呈红色,可用作颜料。(2023·浙江卷1月)( )
(3)火星全球影像彩图显示了火星表土颜色,表土中赤铁矿主要成分为FeO。(2023·广东卷)( )
(4)FeO粉末在空气中受热,迅速被氧化成Fe₃O₄。(2021·湖南卷)( )
(1)古壁画颜料中所用的铁红,其成分为Fe₂O₃。(2023·新课标卷)( )
(2)Fe₂O₃呈红色,可用作颜料。(2023·浙江卷1月)( )
(3)火星全球影像彩图显示了火星表土颜色,表土中赤铁矿主要成分为FeO。(2023·广东卷)( )
(4)FeO粉末在空气中受热,迅速被氧化成Fe₃O₄。(2021·湖南卷)( )
答案:
答案
(1)√
(2)√
(3)×
(4)√
解析
(1)$Fe_{2}O_{3}$为红色,常被用于油漆、涂料、油墨和橡胶的红色颜料,俗称铁红。
(2)$Fe_{2}O_{3}$的颜色是红色,可用作红色颜料。
(3)赤铁矿的主要成分是$Fe_{2}O_{3}$,不是$FeO$。
(4)氧化亚铁具有较强的还原性,在空气中受热容易被氧气氧化为稳定的四氧化三铁。
(1)√
(2)√
(3)×
(4)√
解析
(1)$Fe_{2}O_{3}$为红色,常被用于油漆、涂料、油墨和橡胶的红色颜料,俗称铁红。
(2)$Fe_{2}O_{3}$的颜色是红色,可用作红色颜料。
(3)赤铁矿的主要成分是$Fe_{2}O_{3}$,不是$FeO$。
(4)氧化亚铁具有较强的还原性,在空气中受热容易被氧气氧化为稳定的四氧化三铁。
2.(2022·浙江卷6月)关于化合物FeO(OCH₃)的性质,下列推测不合理的是( )
A.与稀盐酸反应生成FeCl₃、CH₃OH、H₂O
B.隔绝空气加热分解生成FeO、CO₂、H₂O
C.溶于氢碘酸(HI),再加CCl₄萃取,有机层呈紫红色
D.在空气中,与SiO₂高温下反应能生成Fe₂(SiO₃)₃
A.与稀盐酸反应生成FeCl₃、CH₃OH、H₂O
B.隔绝空气加热分解生成FeO、CO₂、H₂O
C.溶于氢碘酸(HI),再加CCl₄萃取,有机层呈紫红色
D.在空气中,与SiO₂高温下反应能生成Fe₂(SiO₃)₃
答案:
B 解析 化合物$FeO(OCH_{3})$中$Fe$元素的化合价为+3价,故其与稀盐酸反应生成$FeCl_{3}$、$CH_{3}OH$、$H_{2}O$,反应原理为$FeO(OCH_{3}) + 3HCl = FeCl_{3} + H_{2}O + CH_{3}OH$,A项合理;化合物$FeO(OCH_{3})$中$Fe$元素的化合价为+3价,C元素为-2价,若隔绝空气加热分解生成$FeO$、$CO_{2}$、$H_{2}O$,则得失电子总数不相等,不符合氧化还原反应规律,即不可能生成$FeO$、$CO_{2}$、$H_{2}O$,B项不合理;化合物$FeO(OCH_{3})$中$Fe$元素的化合价为+3价,故其溶于氢碘酸(HI)生成的$Fe^{3+}$能将$I^{-}$氧化为$I_{2}$,反应原理为$2FeO(OCH_{3}) + 6HI = 2FeI_{2} + I_{2} + 2H_{2}O + 2CH_{3}OH$,再加$CCl_{4}$萃取,有机层呈紫红色,C项合理;化合物$FeO(OCH_{3})$在空气中高温下将生成$Fe_{2}O_{3}$、$CO_{2}$和$H_{2}O$,由于$Fe_{2}O_{3}$为碱性氧化物,$SiO_{2}$为酸性氧化物,故化合物$FeO(OCH_{3})$与$SiO_{2}$高温下反应能生成$Fe_{2}(SiO_{3})_{3}$,D项合理。
3.(2021·广东卷)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是( )

A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b循环转化关系

A.a可与e反应生成b
B.b既可被氧化,也可被还原
C.可将e加入浓碱液中制得d的胶体
D.可存在b→c→d→e→b循环转化关系
答案:
C 解析 题图中所示铁元素不同化合价的物质:a为$Fe$,b为$FeCl_{2}$、$FeSO_{4}$、$Fe(NO_{3})_{2}$等$Fe$(Ⅱ)的盐类物质,c为$Fe(OH)_{2}$,e为$FeCl_{3}$、$Fe_{2}(SO_{4})_{3}$、$Fe(NO_{3})_{3}$等$Fe$(Ⅲ)的盐类物质,d为$Fe(OH)_{3}$。$Fe$与$Fe$(Ⅲ)的盐类物质可发生反应生成$Fe$(Ⅱ)的盐类物质,如$Fe + 2FeCl_{3} = 3FeCl_{2}$,A项合理;$Fe$(Ⅱ)为铁元素的中间价态,既有还原性也有氧化性,因此既可被氧化,也可被还原,B项合理;$Fe$(Ⅲ)的盐类物质与浓碱液反应生成的是$Fe(OH)_{3}$沉淀,制备$Fe(OH)_{3}$胶体的操作为:向沸水中滴加饱和$FeCl_{3}$溶液,继续煮沸至溶液呈红褐色,停止加热,C项不合理;b→c→d→e→b可转化,如$FeCl_{2}\xrightarrow{NaOH}Fe(OH)_{2}\xrightarrow{O_{2}、H_{2}O}Fe(OH)_{3}\xrightarrow{稀盐酸}FeCl_{3}\xrightarrow{Fe}FeCl_{2}$,D项合理。
查看更多完整答案,请扫码查看


