2025年赢在微点化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年赢在微点化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第258页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
- 第189页
- 第190页
- 第191页
- 第192页
- 第193页
- 第194页
- 第195页
- 第196页
- 第197页
- 第198页
- 第199页
- 第200页
- 第201页
- 第202页
- 第203页
- 第204页
- 第205页
- 第206页
- 第207页
- 第208页
- 第209页
- 第210页
- 第211页
- 第212页
- 第213页
- 第214页
- 第215页
- 第216页
- 第217页
- 第218页
- 第219页
- 第220页
- 第221页
- 第222页
- 第223页
- 第224页
- 第225页
- 第226页
- 第227页
- 第228页
- 第229页
- 第230页
- 第231页
- 第232页
- 第233页
- 第234页
- 第235页
- 第236页
- 第237页
- 第238页
- 第239页
- 第240页
- 第241页
- 第242页
- 第243页
- 第244页
- 第245页
- 第246页
- 第247页
- 第248页
- 第249页
- 第250页
- 第251页
- 第252页
- 第253页
- 第254页
- 第255页
- 第256页
- 第257页
- 第258页
- 第259页
- 第260页
- 第261页
- 第262页
- 第263页
- 第264页
- 第265页
- 第266页
- 第267页
- 第268页
- 第269页
- 第270页
- 第271页
- 第272页
- 第273页
- 第274页
- 第275页
- 第276页
- 第277页
- 第278页
- 第279页
- 第280页
- 第281页
- 第282页
- 第283页
- 第284页
- 第285页
- 第286页
- 第287页
- 第288页
- 第289页
- 第290页
- 第291页
- 第292页
- 第293页
- 第294页
- 第295页
- 第296页
- 第297页
- 第298页
- 第299页
- 第300页
- 第301页
- 第302页
- 第303页
- 第304页
- 第305页
- 第306页
- 第307页
- 第308页
- 第309页
- 第310页
- 第311页
- 第312页
- 第313页
- 第314页
- 第315页
- 第316页
- 第317页
- 第318页
- 第319页
- 第320页
- 第321页
二、影响化学平衡的外界因素
1. 影响化学平衡的因素
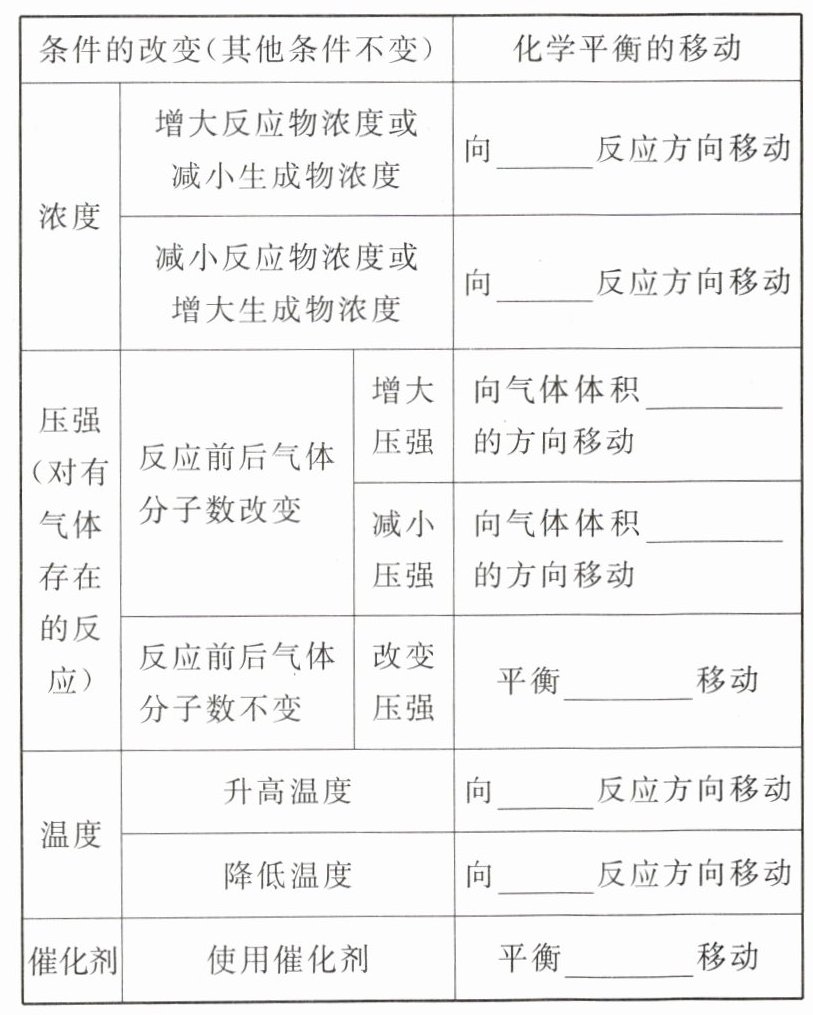
2. 几种特殊情况说明
(1)改变固体或纯液体的量,对化学平衡没影响。
(2)“惰性气体”对化学平衡的影响。
①恒温、恒容条件
原平衡体系$\xrightarrow{充入惰性气体}$体系总压强增大$\xrightarrow{}$体系中各组分的浓度不变$\xrightarrow{}$平衡不移动。
②恒温、恒压条件
原平衡体系$\xrightarrow{充入惰性气体}$容器容积增大,各反应气体的分压减小$\xrightarrow{}$体系中各组分的浓度同倍数减小(等效于减压)$\begin{cases}反应前后体积不变的反应\xrightarrow{}平衡不移动\\反应前后体积可变的反应\xrightarrow{}平衡向气体体积增大的方向移动\end{cases}$
(3)同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响。
1. 影响化学平衡的因素

2. 几种特殊情况说明
(1)改变固体或纯液体的量,对化学平衡没影响。
(2)“惰性气体”对化学平衡的影响。
①恒温、恒容条件
原平衡体系$\xrightarrow{充入惰性气体}$体系总压强增大$\xrightarrow{}$体系中各组分的浓度不变$\xrightarrow{}$平衡不移动。
②恒温、恒压条件
原平衡体系$\xrightarrow{充入惰性气体}$容器容积增大,各反应气体的分压减小$\xrightarrow{}$体系中各组分的浓度同倍数减小(等效于减压)$\begin{cases}反应前后体积不变的反应\xrightarrow{}平衡不移动\\反应前后体积可变的反应\xrightarrow{}平衡向气体体积增大的方向移动\end{cases}$
(3)同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响。
答案:
二、1.正 逆 减小 增大 不 吸热 放热 不
三、勒夏特列原理
1. 勒夏特列原理(平衡移动原理):已达____的可逆反应,如果改变____条件,平衡就向着____的方向移动。
2. 减弱:平衡移动只能减弱条件改变对平衡的影响,不能完全消除这种改变,更不能扭转这种改变。
1. 勒夏特列原理(平衡移动原理):已达____的可逆反应,如果改变____条件,平衡就向着____的方向移动。
2. 减弱:平衡移动只能减弱条件改变对平衡的影响,不能完全消除这种改变,更不能扭转这种改变。
答案:
三、平衡 影响平衡的一个 减弱这种改变
二、思维辨析
判断正误,正确的画“√”,错误的画“×”。
1. 温度改变,平衡一定发生移动。 ( )
2. 只要$v$(正)增大,平衡一定正向移动。 ( )
3. 不论恒温恒容,还是恒温恒压容器,加入稀有气体,平衡皆发生移动。 ( )
4. 起始加入原料的物质的量相等,则各种原料的转化率一定相等。 ( )
5. 通过改变一个条件使某反应向正反应方向移动,转化率一定增大。 ( )
判断正误,正确的画“√”,错误的画“×”。
1. 温度改变,平衡一定发生移动。 ( )
2. 只要$v$(正)增大,平衡一定正向移动。 ( )
3. 不论恒温恒容,还是恒温恒压容器,加入稀有气体,平衡皆发生移动。 ( )
4. 起始加入原料的物质的量相等,则各种原料的转化率一定相等。 ( )
5. 通过改变一个条件使某反应向正反应方向移动,转化率一定增大。 ( )
答案:
1.√ 提示:任何反应都伴随着能量的变化,通常表现为吸热或放热,故温度改变,化学平衡将发生移动。
2.× 提示:平衡正向移动是因为v(正)大于v(逆),若v(正)、v(逆)都增大,则平衡不一定正向移动。
3.× 提示:恒温恒容容器中的化学平衡,当充入稀有气体时,化学平衡不移动。
4.× 提示:只有起始原料的物质的量之比等于方程式的化学计量数之比,原料的转化率才相等。
5.× 提示:若反应物不止一种的反应通过增大某反应物的浓度使反应正向移动,则该反应物的转化率减小。
2.× 提示:平衡正向移动是因为v(正)大于v(逆),若v(正)、v(逆)都增大,则平衡不一定正向移动。
3.× 提示:恒温恒容容器中的化学平衡,当充入稀有气体时,化学平衡不移动。
4.× 提示:只有起始原料的物质的量之比等于方程式的化学计量数之比,原料的转化率才相等。
5.× 提示:若反应物不止一种的反应通过增大某反应物的浓度使反应正向移动,则该反应物的转化率减小。
查看更多完整答案,请扫码查看


