2025年天利38套五年真题高考试题分类化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年天利38套五年真题高考试题分类化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第77页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
4.(2023·辽宁卷,14分)硫酸工业在国民经济中占有重要地位。
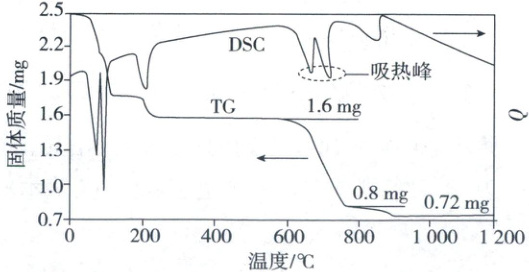
(1)我国古籍记载了硫酸的制备方法——“炼石胆${(CuSO_{4}· 5H_{2}O)}$取精华法”。借助现代仪器分析,该制备过程中${CuSO_{4}· 5H_{2}O}$分解的$TG$曲线(热重)及$DSC$曲线(反映体系热量变化情况,数值已省略)如图所示。$700\ ^{\circ}C$左右有两个吸热峰,则此时分解生成的氧化物有${SO_{2}}$、
(2)铅室法使用了大容积铅室制备硫酸($76\%$以下),副产物为亚硝基硫酸,主要反应如下:
${NO_{2} + SO_{2} + H_{2}O\xlongequal{}NO + H_{2}SO_{4}}$
${2NO + O_{2}\xlongequal{}2NO_{2}}$
(ⅰ)上述过程中${NO_{2}}$的作用为
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是
(3)接触法制硫酸的关键反应为${SO_{2}}$的催化氧化:
${SO_{2}(g) + \dfrac{1}{2}O_{2}(g)⇌ SO_{3}(g)}\ \ \ \Delta H=-98.9\ kJ/mol$
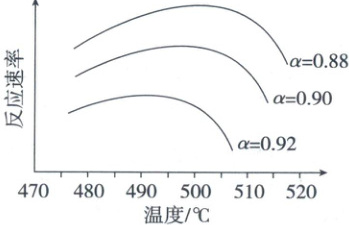
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率$(\alpha)$下反应速率(数值已略去)与温度的关系如图所示,下列说法正确的是
a. 温度越高,反应速率越大
b. $\alpha =0.88$的曲线代表平衡转化率
c. $\alpha$越大,反应速率最大值对应温度越低
d. 可根据不同$\alpha$下的最大速率,选择最佳生产温度
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是
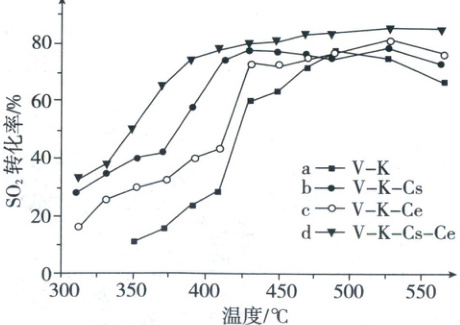
(ⅲ)设${O_{2}}$的平衡分压为$p$,${SO_{2}}$的平衡转化率为$\alpha_{e}$,用含$p$和$\alpha_{e}$的代数式表示上述催化氧化反应的$K_{p}=$
(1)我国古籍记载了硫酸的制备方法——“炼石胆${(CuSO_{4}· 5H_{2}O)}$取精华法”。借助现代仪器分析,该制备过程中${CuSO_{4}· 5H_{2}O}$分解的$TG$曲线(热重)及$DSC$曲线(反映体系热量变化情况,数值已省略)如图所示。$700\ ^{\circ}C$左右有两个吸热峰,则此时分解生成的氧化物有${SO_{2}}$、
CuO
和SO3
(填化学式)。
(2)铅室法使用了大容积铅室制备硫酸($76\%$以下),副产物为亚硝基硫酸,主要反应如下:
${NO_{2} + SO_{2} + H_{2}O\xlongequal{}NO + H_{2}SO_{4}}$
${2NO + O_{2}\xlongequal{}2NO_{2}}$
(ⅰ)上述过程中${NO_{2}}$的作用为
催化剂
。(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是
$NO_2$是有毒气体,污染环境;铅室法制硫酸产品浓度低;铅室法制备硫酸存在副产物
(答出两点即可)。(3)接触法制硫酸的关键反应为${SO_{2}}$的催化氧化:
${SO_{2}(g) + \dfrac{1}{2}O_{2}(g)⇌ SO_{3}(g)}\ \ \ \Delta H=-98.9\ kJ/mol$
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率$(\alpha)$下反应速率(数值已略去)与温度的关系如图所示,下列说法正确的是
cd
。
a. 温度越高,反应速率越大
b. $\alpha =0.88$的曲线代表平衡转化率
c. $\alpha$越大,反应速率最大值对应温度越低
d. 可根据不同$\alpha$下的最大速率,选择最佳生产温度
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如图所示,催化性能最佳的是
d
(填标号)。
(ⅲ)设${O_{2}}$的平衡分压为$p$,${SO_{2}}$的平衡转化率为$\alpha_{e}$,用含$p$和$\alpha_{e}$的代数式表示上述催化氧化反应的$K_{p}=$
$\frac{\alpha_e}{\sqrt{p}(1 - \alpha_e)}$
(用平衡分压代替平衡浓度计算)。
答案:
4.(14分)
(1)$CuO$ $SO_3$
(2)(ⅰ)催化剂 (ⅱ)$NO_2$是有毒气体,污染环境;铅室法制硫酸产品浓度低;铅室法制备硫酸存在副产物
(3)(ⅰ)cd (ⅱ)d (ⅲ)$\frac{\alpha_e}{\sqrt{p}(1 - \alpha_e)}$
[解析]化学反应原理综合
(1)由热重曲线可知600℃时,固体的质量为1.6mg,成分为$CuSO_4$,800℃时,固体的质量为0.8mg,成分为$CuO$,则700℃左右$CuSO_4$分解生成$CuO$,可能发生反应$CuSO_4\stackrel{700^{\circ}C}{=\!=\!=}CuO + SO_3\uparrow$、$2CuSO_4\stackrel{700^{\circ}C}{=\!=\!=}2CuO + 2SO_2\uparrow+O_2\uparrow$,则分解生成的氧化物有$SO_2$、$CuO$、$SO_3$。
(2)(ⅰ)由反应原理可知上述过程中$NO_2$作反应的催化剂。(ⅱ)由题意可知与接触法相比,铅室法主要存在的问题:得到的硫酸浓度较低;得到的硫酸存在副产物;使用氮氧化物作催化剂,污染环境。
(3)(ⅰ)由图像可知,当转化率一定时,随着温度的升高,反应速率先增大后减小,a错误;由图像可知,相同温度下,转化率可以达到0.90和0.92,则0.88的曲线不能代表平衡转化率,b错误;由图像可知,$\alpha$越大,反应速率最大值对应温度越低,c正确;实际生产时,可根据不同$\alpha$下最大速率选择最佳生产温度,d正确。(ⅱ)由图像可知,相同温度下使用d作为催化剂时,$SO_2$的转化率最大。(ⅲ)设起始时$SO_2$的物质的量为1mol,据此列出三段式:
$SO_2(g)+\frac{1}{2}O_2(g)\rightleftharpoons SO_3(g)$
起始(mol) 1 0
转化(mol) $\alpha_e$ $\alpha_e$
平衡(mol) $1 - \alpha_e$ $\alpha_e$
则平衡时$\frac{p(SO_3)}{p(SO_2)}=\frac{\alpha_e}{1 - \alpha_e}$,则$K_p=\frac{\alpha_e}{(1 - \alpha_e)× p^{\frac{1}{2}}}$。
(1)$CuO$ $SO_3$
(2)(ⅰ)催化剂 (ⅱ)$NO_2$是有毒气体,污染环境;铅室法制硫酸产品浓度低;铅室法制备硫酸存在副产物
(3)(ⅰ)cd (ⅱ)d (ⅲ)$\frac{\alpha_e}{\sqrt{p}(1 - \alpha_e)}$
[解析]化学反应原理综合
(1)由热重曲线可知600℃时,固体的质量为1.6mg,成分为$CuSO_4$,800℃时,固体的质量为0.8mg,成分为$CuO$,则700℃左右$CuSO_4$分解生成$CuO$,可能发生反应$CuSO_4\stackrel{700^{\circ}C}{=\!=\!=}CuO + SO_3\uparrow$、$2CuSO_4\stackrel{700^{\circ}C}{=\!=\!=}2CuO + 2SO_2\uparrow+O_2\uparrow$,则分解生成的氧化物有$SO_2$、$CuO$、$SO_3$。
(2)(ⅰ)由反应原理可知上述过程中$NO_2$作反应的催化剂。(ⅱ)由题意可知与接触法相比,铅室法主要存在的问题:得到的硫酸浓度较低;得到的硫酸存在副产物;使用氮氧化物作催化剂,污染环境。
(3)(ⅰ)由图像可知,当转化率一定时,随着温度的升高,反应速率先增大后减小,a错误;由图像可知,相同温度下,转化率可以达到0.90和0.92,则0.88的曲线不能代表平衡转化率,b错误;由图像可知,$\alpha$越大,反应速率最大值对应温度越低,c正确;实际生产时,可根据不同$\alpha$下最大速率选择最佳生产温度,d正确。(ⅱ)由图像可知,相同温度下使用d作为催化剂时,$SO_2$的转化率最大。(ⅲ)设起始时$SO_2$的物质的量为1mol,据此列出三段式:
$SO_2(g)+\frac{1}{2}O_2(g)\rightleftharpoons SO_3(g)$
起始(mol) 1 0
转化(mol) $\alpha_e$ $\alpha_e$
平衡(mol) $1 - \alpha_e$ $\alpha_e$
则平衡时$\frac{p(SO_3)}{p(SO_2)}=\frac{\alpha_e}{1 - \alpha_e}$,则$K_p=\frac{\alpha_e}{(1 - \alpha_e)× p^{\frac{1}{2}}}$。
查看更多完整答案,请扫码查看


