2025年天利38套五年真题高考试题分类化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年天利38套五年真题高考试题分类化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第5页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
1. (2025·1月浙江卷,3分)下列属于极性分子的是(
A.${HCl}$
B.${N_{2}}$
C.${He}$
D.${CH_{4}}$
A
)A.${HCl}$
B.${N_{2}}$
C.${He}$
D.${CH_{4}}$
答案:
1.A 物质分类 HCl由极性键构成,正负电荷中心不重合,属于极性分子,A正确。
2. (2025·辽吉黑内蒙古卷,3分)东北三省及内蒙古资源丰富,下列资源转化的主要过程不属于化学变化的是(
A.石灰石煅烧
B.磁铁矿炼铁
C.煤的液化
D.石油分馏
D
)A.石灰石煅烧
B.磁铁矿炼铁
C.煤的液化
D.石油分馏
答案:
2.D 物理变化与化学变化 石油分馏是利用石油中各组分沸点不同进行分离的方法,属于物理变化,D正确。
3. 【日常生活】(2025·湖北卷,3分)下列与生活相关的叙述中,不涉及化学变化的是(
A.干冰升华助力舞台云雾形成
B.珍珠遇酸后失去光泽
C.加酶洗衣粉清洗蛋白质污渍
D.植物油久置氧化变质
A
)A.干冰升华助力舞台云雾形成
B.珍珠遇酸后失去光泽
C.加酶洗衣粉清洗蛋白质污渍
D.植物油久置氧化变质
答案:
3.A 化学变化 干冰升华是物理变化,A正确;珍珠主要成分为碳酸钙,遇酸发生化学反应而溶解导致失去光泽,B错误;活性酶可以使蛋白质水解,达到去污的目的,涉及化学变化,C错误;植物油中含有碳碳双键,易被氧化而变质,涉及化学变化,D错误。
4. (2025·陕晋青宁卷,3分)某元素的单质及其化合物的转化关系如图。常温常压下${G}$、${J}$均为无色气体,${J}$具有漂白性。阿伏加德罗常数的值为$N_{A}$。下列说法错误的是(
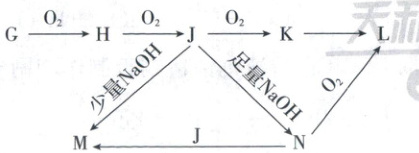
A.${G}$、${K}$均能与${NaOH}$溶液反应
B.${H}$、${N}$既具有氧化性也具有还原性
C.${M}$和${N}$溶液中的离子种类相同
D.$1\ mol\ {G}$与足量的${J}$反应,转移电子数为$N_{A}$
D
)
A.${G}$、${K}$均能与${NaOH}$溶液反应
B.${H}$、${N}$既具有氧化性也具有还原性
C.${M}$和${N}$溶液中的离子种类相同
D.$1\ mol\ {G}$与足量的${J}$反应,转移电子数为$N_{A}$
答案:
4.D 物质转化与性质
[思路分析]常温常压下J为无色气体,且具有漂白性,其所含元素发生连续氧化,则J为SO₂;常温常压下G为无色气体,可知为H₂S,H为S;SO₂分别与少量和足量NaOH反应,M为NaHSO₃,N为Na₂SO₃,Na₂SO₃被氧气氧化生成的L为Na₂SO₄。
H₂S$\xrightarrow{O_2}$S$\xrightarrow{O_2}$SO₂$\xrightarrow{O_2}$SO₃$\xrightarrow{Na_2SO_4}$
H₂S和SO₂均能与NaOH溶液反应,A正确;S、Na₂SO₃中S的化合价均为中间价态,既具有氧化性也具有还原性,B正确;HSO₃⁻可电离出SO₃²⁻,SO₃²⁻可水解为HSO₃⁻,M和N溶液中的离子种类相同,C正确;H₂S和足量SO₂反应的方程式为2H₂S + SO₂ = 3S + 2H₂O,由化学方程式可知1molH₂S完全反应,转移电子数为2N_A。
[思路分析]常温常压下J为无色气体,且具有漂白性,其所含元素发生连续氧化,则J为SO₂;常温常压下G为无色气体,可知为H₂S,H为S;SO₂分别与少量和足量NaOH反应,M为NaHSO₃,N为Na₂SO₃,Na₂SO₃被氧气氧化生成的L为Na₂SO₄。
H₂S$\xrightarrow{O_2}$S$\xrightarrow{O_2}$SO₂$\xrightarrow{O_2}$SO₃$\xrightarrow{Na_2SO_4}$
H₂S和SO₂均能与NaOH溶液反应,A正确;S、Na₂SO₃中S的化合价均为中间价态,既具有氧化性也具有还原性,B正确;HSO₃⁻可电离出SO₃²⁻,SO₃²⁻可水解为HSO₃⁻,M和N溶液中的离子种类相同,C正确;H₂S和足量SO₂反应的方程式为2H₂S + SO₂ = 3S + 2H₂O,由化学方程式可知1molH₂S完全反应,转移电子数为2N_A。
5. (2025·河南卷,3分)${X}$是自然界中一种常见矿物的主要成分,可以通过如图所示的四步反应转化为${Q}$(略去部分参与反应的物质和反应条件)。已知${X}$和${Q}$的组成元素相同。

下列说法错误的是(
A.${Y}$常用作油漆、涂料等的红色颜料
B.溶液${Z}$加热煮沸后颜色会发生变化
C.${R\longrightarrow Q}$反应需要在强酸性条件下进行
D.${Q}$可以通过单质间化合反应制备

下列说法错误的是(
C
)A.${Y}$常用作油漆、涂料等的红色颜料
B.溶液${Z}$加热煮沸后颜色会发生变化
C.${R\longrightarrow Q}$反应需要在强酸性条件下进行
D.${Q}$可以通过单质间化合反应制备
答案:
5.C 物质的转化与推断 综合题设情境可推断出X、Y、Q分别为FeS₂、Fe₂O₃、FeS,Z为铁盐溶液,R为亚铁盐溶液。红棕色的Fe₂O₃可用作油漆、涂料等的红色颜料,A正确;含有Fe²⁺的溶液加热煮沸会生成红褐色氢氧化铁,颜色发生变化,B正确;FeS与强酸反应生成H₂S,强酸性条件下无法制得FeS,C错误;FeS可以通过铁和硫单质直接化合制备,D正确。
6. (2025·广东卷,3分)能满足下列物质间直接转化关系,且推理成立的是(
$单质\ {X}\xrightarrow{{O_{2}}}氧化物\ 1\xrightarrow{{O_{2}}}氧化物\ 2\xrightarrow{{H_{2}O}}酸(或碱)\xrightarrow{{NaOH(或{HCl})}}盐$
A.${X}$可为铝,盐的水溶液一定显酸性
B.${X}$可为硫,氧化物$1$可使品红溶液褪色
C.${X}$可为钠,氧化物$2$可与水反应生成${H_{2}}$
D.${X}$可为碳,盐的热稳定性:${NaHCO_{3}}>{Na_{2}CO_{3}}$
B
)$单质\ {X}\xrightarrow{{O_{2}}}氧化物\ 1\xrightarrow{{O_{2}}}氧化物\ 2\xrightarrow{{H_{2}O}}酸(或碱)\xrightarrow{{NaOH(或{HCl})}}盐$
A.${X}$可为铝,盐的水溶液一定显酸性
B.${X}$可为硫,氧化物$1$可使品红溶液褪色
C.${X}$可为钠,氧化物$2$可与水反应生成${H_{2}}$
D.${X}$可为碳,盐的热稳定性:${NaHCO_{3}}>{Na_{2}CO_{3}}$
答案:
6.B 元素化合物的性质与转化 铝不是变价金属,不能发生连续氧化,A错误;若X为硫,则氧化物1为SO₂,SO₂具有漂白性,可使品红溶液褪色,B正确;若X为钠,则氧化物1为Na₂O,氧化物2为Na₂O₂,Na₂O₂与水反应生成NaOH和O₂,C错误;盐的热稳定性NaHCO₃<Na₂CO₃,D错误。
7. (2025·湖北卷,3分)如图所示的物质转化关系中,固体${A}$与固体${B}$研细后混合,常温下搅拌产生气体${C}$和固体${D}$,温度迅速下降。气体${C}$能使湿润的红色石蕊试纸变蓝。${G}$是一种强酸。${H}$是白色固体,常用作钡餐。下列叙述错误的是(

A.在${C}$的水溶液中加入少量固体${A}$,溶液${pH}$升高
B.${D}$为可溶于水的有毒物质
C.${F}$溶于雨水可形成酸雨
D.常温下可用铁制容器来盛装${G}$的浓溶液
A
)
A.在${C}$的水溶液中加入少量固体${A}$,溶液${pH}$升高
B.${D}$为可溶于水的有毒物质
C.${F}$溶于雨水可形成酸雨
D.常温下可用铁制容器来盛装${G}$的浓溶液
答案:
7.A 无机物的推断及性质
[物质推断]根据固体A与固体B研细后混合,常温能产生气体C和固体D,同时温度迅速下降,可以联想到NH₄Cl和Ba(OH)₂·8H₂O反应,根据气体C能使湿润的红色试纸变蓝,可知C为NH₃,A为NH₄Cl,根据H为白色固体,常用作钡餐,可知B可能为Ba(OH)₂·8H₂O,D为BaCl₂,H为BaSO₄,E为NO,F为NO₂,G为HNO₃。
少量固体NH₄Cl加入氨水中,增大NH₄⁺浓度,导致NH₃·H₂O电离平衡逆向移动,OH⁻浓度降低,pH降低,A错误;BaCl₂可溶于水,Ba²⁺属于重金属离子,有毒,B正确;F为NO₂,溶于水可形成硝酸型酸雨,C正确;G的浓溶液为浓硝酸,常温下Fe遇浓硝酸发生钝化,故常温下可以用铁制容器盛装浓硝酸,D正确。
[物质推断]根据固体A与固体B研细后混合,常温能产生气体C和固体D,同时温度迅速下降,可以联想到NH₄Cl和Ba(OH)₂·8H₂O反应,根据气体C能使湿润的红色试纸变蓝,可知C为NH₃,A为NH₄Cl,根据H为白色固体,常用作钡餐,可知B可能为Ba(OH)₂·8H₂O,D为BaCl₂,H为BaSO₄,E为NO,F为NO₂,G为HNO₃。
少量固体NH₄Cl加入氨水中,增大NH₄⁺浓度,导致NH₃·H₂O电离平衡逆向移动,OH⁻浓度降低,pH降低,A错误;BaCl₂可溶于水,Ba²⁺属于重金属离子,有毒,B正确;F为NO₂,溶于水可形成硝酸型酸雨,C正确;G的浓溶液为浓硝酸,常温下Fe遇浓硝酸发生钝化,故常温下可以用铁制容器盛装浓硝酸,D正确。
查看更多完整答案,请扫码查看


