2025年天利38套五年真题高考试题分类化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年天利38套五年真题高考试题分类化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第41页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
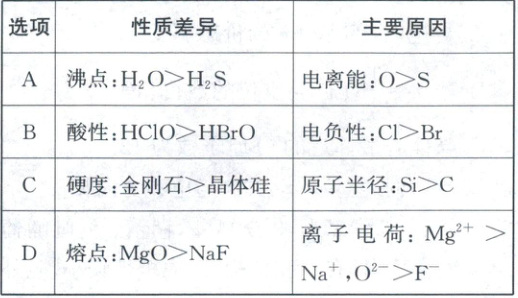
1. (2025·山东卷,2分)物质性质与组成元素的性质有关,下列对物质性质差异解释错误的是(
A
)
答案:
1.A 物质结构与性质 $\mathrm{H_2O}$ 的沸点更高是由于水分子间存在氢键,A错误;$\mathrm{Cl}$ 原子电负性大,导致 $\mathrm{HClO}$ 中羟基的极性更强,酸性相对更强,B 正确;碳原子半径更小,碳碳键的键长更短,键能更大,故金刚石的硬度高,C 正确;离子所带的电荷数越多,离子半径越小,则离子键越强,离子晶体的熔点越高,D正确。
易错警示
元素的非金属性(或电负性)的强弱除了可以判断最高价含氧酸的酸性强弱,也可以通过其对羟基($\mathrm{O—H}$)极性的影响判断简单低价含氧酸的酸性强弱,所以不能见到由非金属性(或电负性)的强弱来判断非最高价含氧酸的情况就认定其一定错误。
易错警示
元素的非金属性(或电负性)的强弱除了可以判断最高价含氧酸的酸性强弱,也可以通过其对羟基($\mathrm{O—H}$)极性的影响判断简单低价含氧酸的酸性强弱,所以不能见到由非金属性(或电负性)的强弱来判断非最高价含氧酸的情况就认定其一定错误。
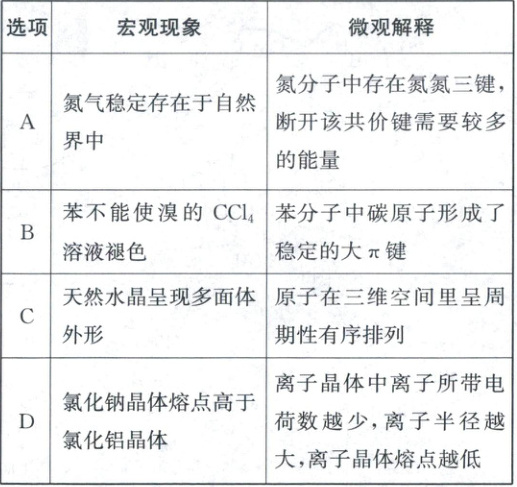
2. (2025·河北卷,3分)化学研究应当注重宏观与微观相结合。下列宏观现象与微观解释不符的是(
D
)
答案:
2.D 物质的结构与性质 由于 $\mathrm{N_2}$ 分子中存在氮氮三键,该共价键键能较大,更稳定,所以氮气常温下很难与其他物质反应,可稳定存在于自然界中,A正确;苯分子中不存在单双键交替的结构,存在稳定的大 $\pi$ 键,所以不能与溴发生加成反应而使溴的 $\mathrm{CCl_4}$ 溶液褪色,B正确;水晶为 $\mathrm{SiO_2}$ 晶体,为共价晶体,由硅原子和氧原子形成硅氧四面体在三维空间周期性有序排列而成,呈现规则的多面体外形,C正确;氯化钠属于离子晶体,微粒间作用力为离子键,而氯化铝属于分子晶体,分子间作用力较弱,氯化铝熔点低于氯化钠,D错误。
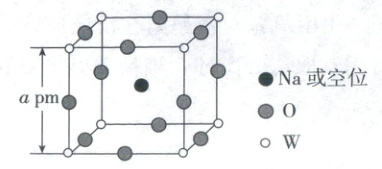
3. (2025·辽吉黑内蒙古卷,3分)${Na_{x}WO_{3}}$晶体因$x$变化形成空位而导致颜色各异,当$0.44\leqslant x\leqslant0.95$时,其立方晶胞结构如图。设$N_{A}$为阿伏加德罗常数的值,下列说法错误的是(
A.与${W}$最近且等距的${O}$有$6$个
B.$x$增大时,${W}$的平均价态升高
C.密度为$\dfrac{243.5×10^{30}}{a^{3}· N_{A}}\ {g/cm^{3}}$时,$x=0.5$
D.空位数不同,吸收的可见光波长不同
B
)
A.与${W}$最近且等距的${O}$有$6$个
B.$x$增大时,${W}$的平均价态升高
C.密度为$\dfrac{243.5×10^{30}}{a^{3}· N_{A}}\ {g/cm^{3}}$时,$x=0.5$
D.空位数不同,吸收的可见光波长不同
答案:
3.B 晶胞的结构与性质 由晶胞结构可知,与 $\mathrm{W}$ 最近且等距的 $\mathrm{O}$ 位于 $\mathrm{W}$ 的上、下、前、后、左、右,共有 $6$ 个,A正确;$\mathrm{Na_xWO_3}$ 总体呈电中性,$\mathrm{O}$ 为 $-2$ 价,$\mathrm{Na}$ 为 $+1$ 价,$x$ 增大时,$\mathrm{W}$ 的平均价态降低,B错误;由“均摊法”可知,$1$ 个晶胞含有 $1$ 个 $\mathrm{Na_xWO_3}$,则晶体的密度 $\rho=\frac{N× M}{N_A× V}=\frac{M_r× 10^{30}}{a^3· N_A}\ \mathrm{g/cm^3}$,当密度为 $\frac{243.5× 10^{30}}{a^3· N_A}\ \mathrm{g/cm^3}$ 时,说明 $\mathrm{Na_xWO_3}$ 的摩尔质量为 $243.5\ \mathrm{g/mol}$,即 $23x + 184 + 16× 3 = 243.5$,解得 $x = 0.5$,C正确;由题意可知,$\mathrm{Na_xWO_3}$ 晶体因 $x$ 变化形成空位而导致颜色不同,则空位数不同,吸收的可见光波长不同,D正确。
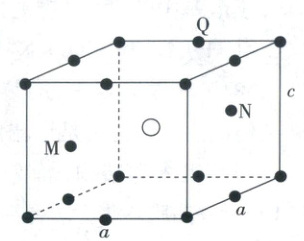
4. (2025·河北卷,3分)${SmCo_{k}}(k>1)$是一种具有优异磁性能的稀土永磁材料,在航空航天等领域中获得重要应用。${SmCo_{k}}$的六方晶胞示意图如图所示,晶胞参数$a=500\ {pm}$、$c=400\ {pm}$,$M$、$N$原子的分数坐标分别为$\left(\dfrac{5}{6},\dfrac{1}{6},\dfrac{1}{2}\right)$、$\left(\dfrac{1}{6},\dfrac{5}{6},\dfrac{1}{2}\right)$。设$N_{A}$是阿伏加德罗常数的值。

下列说法错误的是(
A.该物质的化学式为${SmCo_{5}}$
B.体心原子的分数坐标为$\left(\dfrac{1}{2},\dfrac{1}{2},\dfrac{1}{2}\right)$
C.晶体的密度为$\dfrac{890\sqrt{3}}{3N_{A}×10^{-22}}\ {g/cm^{3}}$
D.原子$Q$到体心的距离为$100\sqrt{41}\ {pm}$


下列说法错误的是(
D
)A.该物质的化学式为${SmCo_{5}}$
B.体心原子的分数坐标为$\left(\dfrac{1}{2},\dfrac{1}{2},\dfrac{1}{2}\right)$
C.晶体的密度为$\dfrac{890\sqrt{3}}{3N_{A}×10^{-22}}\ {g/cm^{3}}$
D.原子$Q$到体心的距离为$100\sqrt{41}\ {pm}$
答案:
4.D 晶体结构 白球所在位置为体心,数目为 $1$,黑球占据晶胞的所有顶点、$8$ 个棱心,$2$ 个黑球位于体内,所以其数目为 $\frac{1}{8}× 8 + \frac{1}{4}× 8 + 2 = 5$,可得其化学式为 $\mathrm{SmCo_5}$,A项正确;体心原子的分数坐标为 $(\frac{1}{2},\frac{1}{2},\frac{1}{2})$,B项正确;由A项可得晶胞质量为 $\frac{150 + 5× 59}{N_A}\ \mathrm{g}$,晶胞底面为菱形,底面积为 $2$ 个边长为 $a\ \mathrm{pm}$ 的正三角形面积之和,所以晶胞体积为 $2× \frac{\sqrt{3}}{4}a^2c\ \mathrm{pm^3}$(边长为 $a\ \mathrm{pm}$ 的正三角形的面积 $S = \frac{\sqrt{3}}{4}a^2\ \mathrm{pm^2}$),可得晶体密度 $\rho = \frac{m}{V} = \frac{\frac{150 + 5× 59}{N_A}\ \mathrm{g}}{2× \frac{\sqrt{3}}{4}× 500^2× 400× 10^{-30}\ \mathrm{cm^3}} = \frac{890\sqrt{3}}{3N_A× 10^{-22}}\ \mathrm{g/cm^3}$,C项正确;以上面中心作如图直角三角形
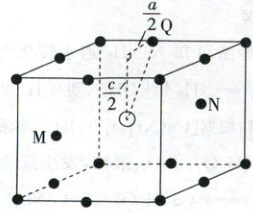
可得原子 $\mathrm{Q}$ 到体心的距离为 $\sqrt{(\frac{a}{2})^2 + (\frac{c}{2})^2} = \sqrt{(\frac{500}{2})^2 + (\frac{400}{2})^2}\ \mathrm{pm} = 50\sqrt{41}\ \mathrm{pm}$,D项错误。
4.D 晶体结构 白球所在位置为体心,数目为 $1$,黑球占据晶胞的所有顶点、$8$ 个棱心,$2$ 个黑球位于体内,所以其数目为 $\frac{1}{8}× 8 + \frac{1}{4}× 8 + 2 = 5$,可得其化学式为 $\mathrm{SmCo_5}$,A项正确;体心原子的分数坐标为 $(\frac{1}{2},\frac{1}{2},\frac{1}{2})$,B项正确;由A项可得晶胞质量为 $\frac{150 + 5× 59}{N_A}\ \mathrm{g}$,晶胞底面为菱形,底面积为 $2$ 个边长为 $a\ \mathrm{pm}$ 的正三角形面积之和,所以晶胞体积为 $2× \frac{\sqrt{3}}{4}a^2c\ \mathrm{pm^3}$(边长为 $a\ \mathrm{pm}$ 的正三角形的面积 $S = \frac{\sqrt{3}}{4}a^2\ \mathrm{pm^2}$),可得晶体密度 $\rho = \frac{m}{V} = \frac{\frac{150 + 5× 59}{N_A}\ \mathrm{g}}{2× \frac{\sqrt{3}}{4}× 500^2× 400× 10^{-30}\ \mathrm{cm^3}} = \frac{890\sqrt{3}}{3N_A× 10^{-22}}\ \mathrm{g/cm^3}$,C项正确;以上面中心作如图直角三角形

可得原子 $\mathrm{Q}$ 到体心的距离为 $\sqrt{(\frac{a}{2})^2 + (\frac{c}{2})^2} = \sqrt{(\frac{500}{2})^2 + (\frac{400}{2})^2}\ \mathrm{pm} = 50\sqrt{41}\ \mathrm{pm}$,D项错误。
5. (2025·江苏卷,3分)在溶有$15-$冠$-5$ 的有机溶剂中,苄氯
的有机溶剂中,苄氯 与${NaF}$发生反应:
与${NaF}$发生反应:
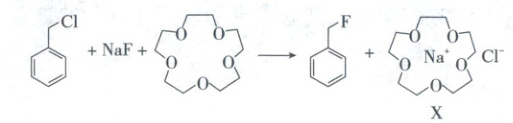
下列说法正确的是(
A.苄氯是非极性分子
B.电负性:$\chi({F})<\chi({Cl})$
C.离子半径:$r({F^{-}})>r({Na^{+}})$
D.${X}$中$15-$冠$-5$与${Na^{+}}$间存在离子键
 的有机溶剂中,苄氯
的有机溶剂中,苄氯 与${NaF}$发生反应:
与${NaF}$发生反应:
下列说法正确的是(
C
)A.苄氯是非极性分子
B.电负性:$\chi({F})<\chi({Cl})$
C.离子半径:$r({F^{-}})>r({Na^{+}})$
D.${X}$中$15-$冠$-5$与${Na^{+}}$间存在离子键
答案:
5.C 物质的结构与性质 苄氯分子正负电荷中心不重合,属于极性分子,A错误;$\mathrm{F}$、$\mathrm{Cl}$ 为同族元素,由上到下电负性减弱,$\chi(\mathrm{F})>\chi(\mathrm{Cl})$,B错误;$\mathrm{Na^+}$ 与 $\mathrm{F^-}$ 核外电子数相等,$\mathrm{F^-}$ 核电荷数小于 $\mathrm{Na^+}$,原子核对核外电子的吸引力弱于 $\mathrm{Na^+}$,因此离子半径 $r(\mathrm{F^-})>r(\mathrm{Na^+})$,C正确;$15 - 冠 - 5$ 与 $\mathrm{Na^+}$ 间存在弱配位键,不是离子键,D错误。
查看更多完整答案,请扫码查看


