2025年天利38套五年真题高考试题分类化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年天利38套五年真题高考试题分类化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第66页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
5. (2022·河北卷,4分,不定项)恒温恒容条件下,向密闭容器中加入一定量X,发生反应的方程式为①${X = Y}$;②${Y = Z}$。反应①的速率$v_{1}=k_{1}c{(X)}$,反应②的速率$v_{2}=k_{2}c{(Y)}$,式中$k_{1}$、$k_{2}$为速率常数。图甲为该体系中X、Y、Z浓度随时间变化的曲线,图乙为反应①和②的$\ln k~\dfrac{1}{T}$曲线。下列说法错误的是 (
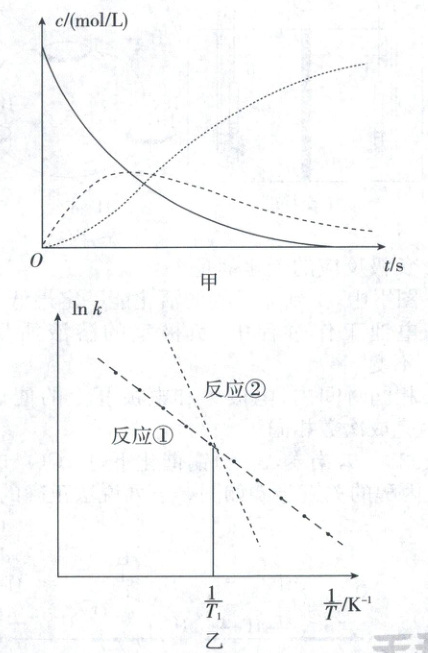
A.随$c{(X)}$的减小,反应①、②的速率均降低
B.体系中$v{(X)}=v{(Y)}+v{(Z)}$
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于$T_{1}$时,总反应速率由反应②决定
AB
)
A.随$c{(X)}$的减小,反应①、②的速率均降低
B.体系中$v{(X)}=v{(Y)}+v{(Z)}$
C.欲提高Y的产率,需提高反应温度且控制反应时间
D.温度低于$T_{1}$时,总反应速率由反应②决定
答案:
5.AB 化学反应速率及其影响因素 随$c(X)$减小,反应①速率减小,由图甲可知,$c(Y)$先增大后减小,$c(Y)$增大时反应②速率增大,A错误;Y达到最大值之前,由反应方程式可知,$\Delta c(X)=\Delta c(Y)+\Delta c(Z)$,由速率计算公式可知$v(X)=v(Y)+v(Z)$,Y达到最大值之后,$\Delta c(X)+\Delta c(Y)=\Delta c(Z)$,即$v(X)+v(Y)=v(Z)$,B错误;欲提高Y的产率,需提高反应温度增大反应①的速率,并且要控制反应时间,使$c(Y)$停在最高点,C正确;由图乙知,温度低于$T_{1}$时,$k_{1}>k_{2}$,总反应速率取决于慢反应,由反应②决定,D正确。
6. (2021·广东卷,4分)反应${X = 2Z}$经历两步:①${X\longrightarrow Y}$;②${Y\longrightarrow 2Z}$。反应体系中X、Y、Z的浓度$c$随时间$t$的变化曲线如图所示。下列说法不正确的是 (
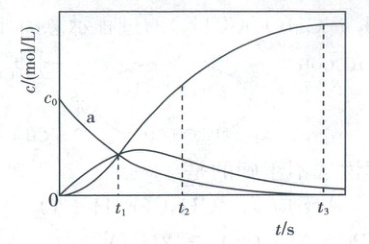
A.a为$c{(X)}$随$t$的变化曲线
B.$t_{1}$时,$c{(X)}=c{(Y)}=c{(Z)}$
C.$t_{2}$时,Y的消耗速率大于生成速率
D.$t_{3}$后,$c{(Z)}=2c_{0}-c{(Y)}$
D
)
A.a为$c{(X)}$随$t$的变化曲线
B.$t_{1}$时,$c{(X)}=c{(Y)}=c{(Z)}$
C.$t_{2}$时,Y的消耗速率大于生成速率
D.$t_{3}$后,$c{(Z)}=2c_{0}-c{(Y)}$
答案:
6.D 化学反应速率
【图像分析】
物质的量浓度一直增大,表示生成物Z的浓度随t的变化曲线
a曲线对应物质的浓度一直减少,表示$c(X)$随t的变化曲线,A正确
$t_{1}$时,三条曲线相交于一点,表示X、Y、Z的物质的量浓度相等,B正确
$t_{2}$时$c(Y)$处于净减少状态,即消耗速率大于生成速率,C正确;由图像可知$t_{3}$时刻X全部转化为Y、Y部分转化为Z,所以此时$c(Z)=2[c_{0}-c(Y)]$,D错误。
【图像分析】
物质的量浓度一直增大,表示生成物Z的浓度随t的变化曲线
a曲线对应物质的浓度一直减少,表示$c(X)$随t的变化曲线,A正确
$t_{1}$时,三条曲线相交于一点,表示X、Y、Z的物质的量浓度相等,B正确
$t_{2}$时$c(Y)$处于净减少状态,即消耗速率大于生成速率,C正确;由图像可知$t_{3}$时刻X全部转化为Y、Y部分转化为Z,所以此时$c(Z)=2[c_{0}-c(Y)]$,D错误。
7. (2021·辽宁卷,3分)某温度下,降冰片烯在钛杂环丁烷催化下聚合,反应物浓度与催化剂浓度及时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法错误的是 (
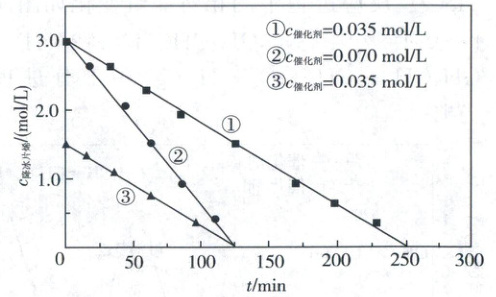
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为$0.012\ mol/(L·min)$
D.条件②,降冰片烯起始浓度为3.0 mol/L时,半衰期为62.5 min
B
)
A.其他条件相同时,催化剂浓度越大,反应速率越大
B.其他条件相同时,降冰片烯浓度越大,反应速率越大
C.条件①,反应速率为$0.012\ mol/(L·min)$
D.条件②,降冰片烯起始浓度为3.0 mol/L时,半衰期为62.5 min
答案:
7.B 化学反应速率 根据条件①、②及其对应的图像可知,催化剂浓度变为原来的2倍,反应时间变为原来的$\frac{1}{2}$,即其他条件相同时,催化剂浓度越大,反应速率越大,A项正确;曲线①、③的斜率相等,即二者的反应速率相等,故反应速率与起始浓度无关,B项错误;条件①对应的反应速率为$0.012mol/(L·min)$,C项正确;结合图像②可知降冰片烯起始浓度为$3.0mol/L$,至完全反应耗时$125min$,则对应的半衰期为$125min×\frac{1}{2}=62.5min$,D项正确。
查看更多完整答案,请扫码查看


