2025年天利38套五年真题高考试题分类化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年天利38套五年真题高考试题分类化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第19页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
1. (2025·甘肃卷,3 分)处理某酸浸液(主要含${Li+}$、${Fe^{2+}}$、${Cu^{2+}}$、${Al^{3+}}$)的部分流程如下:
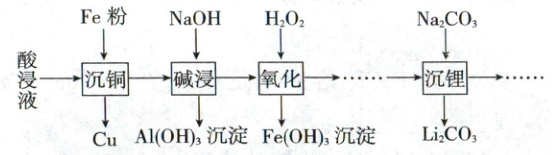
下列说法正确的是 (
A.“沉铜”过程中发生反应的离子方程式:${2Fe + 3Cu^{2+}\xlongequal{}3Cu + 2Fe^{3+}}$
B.“碱浸”过程中${NaOH}$固体加入量越多,${Al(OH)3}$沉淀越完全
C.“氧化”过程中铁元素化合价降低
D.“沉锂”过程利用了${Li2CO3}$的溶解度比${Na2CO3}$小的性质

下列说法正确的是 (
D
)A.“沉铜”过程中发生反应的离子方程式:${2Fe + 3Cu^{2+}\xlongequal{}3Cu + 2Fe^{3+}}$
B.“碱浸”过程中${NaOH}$固体加入量越多,${Al(OH)3}$沉淀越完全
C.“氧化”过程中铁元素化合价降低
D.“沉锂”过程利用了${Li2CO3}$的溶解度比${Na2CO3}$小的性质
答案:
1.D 无机工艺流程
【流程分析】
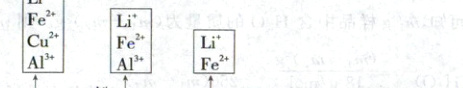
$\begin{matrix} Li^+、Fe^{2+}、Cu^{2+}、Al^{3+} & \overset{Fe粉}{\longrightarrow} & Li^+、Fe^{2+}、Al^{3+} & \overset{NaOH}{\longrightarrow} & Li^+、Fe^{2+} & \overset{H_2O_2}{\longrightarrow} & Li^+ & \overset{Na_2CO_3}{\longrightarrow} \\ 酸浸液 & & & \underset{Al(OH)_3沉淀}{ } & & \underset{Fe(OH)_3沉淀}{ } & & \underset{Li_2CO_3}{沉锂} \end{matrix}$
“沉铜”过程中发生反应的离子方程式为$Cu^{2+} + Fe\xlongequal{}Cu + Fe^{2+}$,A错误;$Al(OH)_3$具有两性,加入$NaOH$过量,$Al(OH)_3$会溶解,B错误;“氧化”过程中,溶液中$Fe^{2+}$被氧化为$Fe^{3+}$,最终转化为氢氧化铁沉淀除去,C错误;加入$Na_2CO_3$可将溶液中的$Li^+$转化为$Li_2CO_3$沉淀,说明$Li_2CO_3$的溶解度小于$Na_2CO_3$,D正确。
1.D 无机工艺流程
【流程分析】
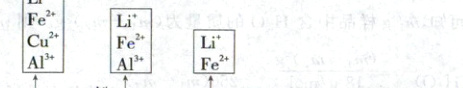
$\begin{matrix} Li^+、Fe^{2+}、Cu^{2+}、Al^{3+} & \overset{Fe粉}{\longrightarrow} & Li^+、Fe^{2+}、Al^{3+} & \overset{NaOH}{\longrightarrow} & Li^+、Fe^{2+} & \overset{H_2O_2}{\longrightarrow} & Li^+ & \overset{Na_2CO_3}{\longrightarrow} \\ 酸浸液 & & & \underset{Al(OH)_3沉淀}{ } & & \underset{Fe(OH)_3沉淀}{ } & & \underset{Li_2CO_3}{沉锂} \end{matrix}$
“沉铜”过程中发生反应的离子方程式为$Cu^{2+} + Fe\xlongequal{}Cu + Fe^{2+}$,A错误;$Al(OH)_3$具有两性,加入$NaOH$过量,$Al(OH)_3$会溶解,B错误;“氧化”过程中,溶液中$Fe^{2+}$被氧化为$Fe^{3+}$,最终转化为氢氧化铁沉淀除去,C错误;加入$Na_2CO_3$可将溶液中的$Li^+$转化为$Li_2CO_3$沉淀,说明$Li_2CO_3$的溶解度小于$Na_2CO_3$,D正确。
2. (2024·广东卷,4 分)部分含${Mg}$或${Al}$或${Fe}$物质的分类与相应化合价关系如图。下列推断合理的是 (

A.若${a}$在沸水中可生成${e}$,则${a→f}$的反应一定是化合反应
B.在${g→f→e→d}$转化过程中,一定存在物质颜色的变化
C.加热${c}$的饱和溶液,一定会形成能产生丁达尔效应的红棕色分散系
D.若${b}$和${d}$均能与同一物质反应生成${c}$,则组成${a}$的元素一定位于周期表${p}$区
B
)
A.若${a}$在沸水中可生成${e}$,则${a→f}$的反应一定是化合反应
B.在${g→f→e→d}$转化过程中,一定存在物质颜色的变化
C.加热${c}$的饱和溶液,一定会形成能产生丁达尔效应的红棕色分散系
D.若${b}$和${d}$均能与同一物质反应生成${c}$,则组成${a}$的元素一定位于周期表${p}$区
答案:
2.B 价类二维图 若a在沸水中可生成e,则a为$Mg$,e为$Mg(OH)_2$,f为镁盐,由$Mg$生成镁盐的反应不一定是化合反应,如$Mg + 2HCl\xlongequal{}MgCl_2 + H_2\uparrow$为置换反应,A错误;存在$g\longrightarrow f\longrightarrow e\longrightarrow d$的转化,说明为含$Fe$元素物质间转化,其中e为$Fe(OH)_3$,d为$Fe(OH)_2$,$Fe(OH)_2$呈白色,$Fe(OH)_3$呈红褐色,B正确;若c为铝盐或四羟基合铝酸盐,加热c的饱和溶液,不会形成能产生丁达尔效应的红棕色分散系,C错误;若b和d均能与同一物质反应生成c,可能为含$Al$元素物质,也可能是含$Fe$元素物质,如$Fe_2O_3$和$Fe(OH)_3$均能与盐酸反应生成$FeCl_3$,而$Fe$元素位于周期表d区,D错误。
3. (2024·福建卷,4 分)用${CuCl}$探究${Cu(Ⅰ)}$、${Cu(Ⅱ)}$性质,实验步骤及观察到的现象如下:

该过程中可能涉及的反应有:
①${CuCl + 2NH_{3}· H_{2}O\xlongequal{}[Cu(NH_{3})_{2}]^{+} + Cl^{-} + 2H_{2}O}$
②${2[Cu(NH_{3})_{2}]^{+}\xlongequal{}[Cu(NH_{3})_{4}]^{2+} + Cu\downarrow}$
③${[Cu(NH_{3})_{4}]^{2+} + Cu\xlongequal{}2[Cu(NH_{3})_{2}]^{+}}$
④${4[Cu(NH_{3})_{2}]^{+} + O_{2} + 8NH_{3}· H_{2}O\xlongequal{}4[Cu(NH_{3})_{4}]^{2+} + 4OH^{-} + 6H_{2}O}$
下列说法错误的是 (
A.与${Cu^{2+}}$的配位能力:${NH_{3} < OH^{-}}$
B.${[Cu(NH_{3})_{2}]^{+}(aq)}$无色
C.氧化性:${[Cu(NH_{3})_{2}]^{+} < [Cu(NH_{3})_{4}]^{2+}}$
D.探究过程未发生反应②

该过程中可能涉及的反应有:
①${CuCl + 2NH_{3}· H_{2}O\xlongequal{}[Cu(NH_{3})_{2}]^{+} + Cl^{-} + 2H_{2}O}$
②${2[Cu(NH_{3})_{2}]^{+}\xlongequal{}[Cu(NH_{3})_{4}]^{2+} + Cu\downarrow}$
③${[Cu(NH_{3})_{4}]^{2+} + Cu\xlongequal{}2[Cu(NH_{3})_{2}]^{+}}$
④${4[Cu(NH_{3})_{2}]^{+} + O_{2} + 8NH_{3}· H_{2}O\xlongequal{}4[Cu(NH_{3})_{4}]^{2+} + 4OH^{-} + 6H_{2}O}$
下列说法错误的是 (
A
)A.与${Cu^{2+}}$的配位能力:${NH_{3} < OH^{-}}$
B.${[Cu(NH_{3})_{2}]^{+}(aq)}$无色
C.氧化性:${[Cu(NH_{3})_{2}]^{+} < [Cu(NH_{3})_{4}]^{2+}}$
D.探究过程未发生反应②
答案:
3.A 简单配合物的制备
【实验剖析】根据实验步骤及观察到的现象可知,加过量氨水时发生反应①$CuCl + 2NH_3·H_2O\xlongequal{}[Cu(NH_3)_2]^+ + Cl^- + 2H_2O$;依据无色溶液露置在空气中变蓝且没有红色固体析出可知含$Cu(Ⅰ)$配合物阳离子被氧化,发生了反应④$4[Cu(NH_3)_2]^+ + O_2 + 8NH_3·H_2O\xlongequal{}4[Cu(NH_3)_4]^{2+} + 4OH^- + 6H_2O$;依据加适量铜粉振荡后变为无色溶液可知含$Cu(Ⅱ)$配合物阳离子被还原,发生了反应③$[Cu(NH_3)_4]^{2+} + Cu\xlongequal{}2[Cu(NH_3)_2]^+$。
由反应④产物中$[Cu(NH_3)_4]^{2+}$和$OH^-$稳定共存可知与$Cu^{2+}$的配位能力:$NH_3 > OH^-$,A错误;由反应①得到无色溶液可知$[Cu(NH_3)_2]^+(aq)$无色,B正确;反应③是氧化还原反应,其中$[Cu(NH_3)_4]^{2+}$作氧化剂,$[Cu(NH_3)_2]^+$为氧化产物,氧化性为$[Cu(NH_3)_4]^{2+} > [Cu(NH_3)_2]^+$,C正确;依据露置在空气中没有红色固体析出的现象可推断未发生反应②,D正确。
【实验剖析】根据实验步骤及观察到的现象可知,加过量氨水时发生反应①$CuCl + 2NH_3·H_2O\xlongequal{}[Cu(NH_3)_2]^+ + Cl^- + 2H_2O$;依据无色溶液露置在空气中变蓝且没有红色固体析出可知含$Cu(Ⅰ)$配合物阳离子被氧化,发生了反应④$4[Cu(NH_3)_2]^+ + O_2 + 8NH_3·H_2O\xlongequal{}4[Cu(NH_3)_4]^{2+} + 4OH^- + 6H_2O$;依据加适量铜粉振荡后变为无色溶液可知含$Cu(Ⅱ)$配合物阳离子被还原,发生了反应③$[Cu(NH_3)_4]^{2+} + Cu\xlongequal{}2[Cu(NH_3)_2]^+$。
由反应④产物中$[Cu(NH_3)_4]^{2+}$和$OH^-$稳定共存可知与$Cu^{2+}$的配位能力:$NH_3 > OH^-$,A错误;由反应①得到无色溶液可知$[Cu(NH_3)_2]^+(aq)$无色,B正确;反应③是氧化还原反应,其中$[Cu(NH_3)_4]^{2+}$作氧化剂,$[Cu(NH_3)_2]^+$为氧化产物,氧化性为$[Cu(NH_3)_4]^{2+} > [Cu(NH_3)_2]^+$,C正确;依据露置在空气中没有红色固体析出的现象可推断未发生反应②,D正确。
4. (2024·辽吉黑卷,3 分)某工厂利用铜屑脱除锌浸出液中的${Cl^{-}}$并制备${Zn}$,流程如下。“脱氯”步骤仅${Cu}$元素化合价发生改变。下列说法正确的是 (
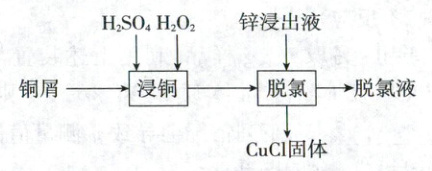
锌浸出液中相关成分(其他成分无干扰)

A.“浸铜”时应加入足量${H_{2}O_{2}}$,确保铜屑溶解完全
B.“浸铜”反应:${2Cu + 4H^{+} + H_{2}O_{2}\xlongequal{}2Cu^{2+} + H_{2}\uparrow + 2H_{2}O}$
C.“脱氯”反应:${Cu + Cu^{2+} + 2Cl^{-}\xlongequal{}2CuCl}$
D.脱氯液净化后电解,可在阳极得到${Zn}$
C
)
锌浸出液中相关成分(其他成分无干扰)

A.“浸铜”时应加入足量${H_{2}O_{2}}$,确保铜屑溶解完全
B.“浸铜”反应:${2Cu + 4H^{+} + H_{2}O_{2}\xlongequal{}2Cu^{2+} + H_{2}\uparrow + 2H_{2}O}$
C.“脱氯”反应:${Cu + Cu^{2+} + 2Cl^{-}\xlongequal{}2CuCl}$
D.脱氯液净化后电解,可在阳极得到${Zn}$
答案:
4.C 工艺流程、氧化还原反应、电解原理 结合整个流程分析,“浸铜”时应加入适量$H_2O_2$,使部分铜屑溶解,确保“脱氯”时$Cu$和$Cu^{2+}$的物质的量基本相同,A错误;“浸铜”反应为$Cu + 2H^+ + H_2O_2\xlongequal{}Cu^{2+} + 2H_2O$,B错误;“脱氯”反应为$Cu + Cu^{2+} + 2Cl^-\xlongequal{}2CuCl$,C正确;电解时$Zn^{2+}$在阴极得电子生成$Zn$,D错误。
5. (2023·广东卷,2 分)部分含${Na}$或含${Cu}$物质的分类与相应化合价关系如图所示。下列推断不合理的是 (
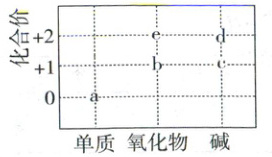
A.可存在${c→d→e}$的转化
B.能与${H_{2}O}$反应生成${c}$的物质只有${b}$
C.新制的${d}$可用于检验葡萄糖中的醛基
D.若${b}$能与${H_{2}O}$反应生成${O_{2}}$,则${b}$中含共价键
B
)
A.可存在${c→d→e}$的转化
B.能与${H_{2}O}$反应生成${c}$的物质只有${b}$
C.新制的${d}$可用于检验葡萄糖中的醛基
D.若${b}$能与${H_{2}O}$反应生成${O_{2}}$,则${b}$中含共价键
答案:
5.B 价类二维图
【思路分析】结合价类二维图可知a为$Na$或$Cu$;b为$Na_2O$、$Na_2O_2$或$Cu_2O$;c为$NaOH$或$CuOH$;d为$Cu(OH)_2$;e为$CuO$。
若c为$NaOH$,$NaOH$可与铜盐如硫酸铜反应生成$Cu(OH)_2$,$Cu(OH)_2$受热分解可得到$CuO$,若c为$CuOH$,$CuOH$能与$O_2$、$H_2O$反应生成$Cu(OH)_2$,$Cu(OH)_2$受热分解可得到$CuO$,A正确;$Na$、$Na_2O$、$Na_2O_2$均能与水反应生成$NaOH$,B错误;新制$Cu(OH)_2$可用于检验葡萄糖中的醛基,C正确;若b能与$H_2O$反应生成$O_2$,则b为$Na_2O_2$,$Na_2O_2$中存在$O—O$共价键,D正确。
【思路分析】结合价类二维图可知a为$Na$或$Cu$;b为$Na_2O$、$Na_2O_2$或$Cu_2O$;c为$NaOH$或$CuOH$;d为$Cu(OH)_2$;e为$CuO$。
若c为$NaOH$,$NaOH$可与铜盐如硫酸铜反应生成$Cu(OH)_2$,$Cu(OH)_2$受热分解可得到$CuO$,若c为$CuOH$,$CuOH$能与$O_2$、$H_2O$反应生成$Cu(OH)_2$,$Cu(OH)_2$受热分解可得到$CuO$,A正确;$Na$、$Na_2O$、$Na_2O_2$均能与水反应生成$NaOH$,B错误;新制$Cu(OH)_2$可用于检验葡萄糖中的醛基,C正确;若b能与$H_2O$反应生成$O_2$,则b为$Na_2O_2$,$Na_2O_2$中存在$O—O$共价键,D正确。
查看更多完整答案,请扫码查看


