2025年天利38套五年真题高考试题分类化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年天利38套五年真题高考试题分类化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第55页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
1. (2025·湖北卷,3分)某电池的正极材料为${LiFePO_{4}}$,负极材料为嵌锂石墨。利用人工智能筛选出的补锂试剂${LiSO_{2}CF_{3}}$,能使失活的电池再生并延长寿命,且保持电池原结构。将${LiSO_{2}CF_{3}}$注入电池后充电补锂,过程中${[SO_{2}CF_{3}]^{-}}$转化为气体离去。下列有关充电补锂的说法错误的是 (
A.${[SO_{2}CF_{3}]^{-}}$在阳极失去电子
B.生成气体中含有氟代烃
C.过程中铁元素的价态降低
D.${[SO_{2}CF_{3}]^{-}}$反应并离去是该电池保持原结构的原因
C
)A.${[SO_{2}CF_{3}]^{-}}$在阳极失去电子
B.生成气体中含有氟代烃
C.过程中铁元素的价态降低
D.${[SO_{2}CF_{3}]^{-}}$反应并离去是该电池保持原结构的原因
答案:
1.C 电化学 电解池中反应物在阳极上失电子,A正确;根据原子守恒,生成气体中含有氟代烃和硫化物,B正确;补充充锂的过程中[SO₂CF₃]⁻在阳极反应,LiFePO₄不参与反应,故铁元素化合价不变,C错误;[SO₂CF₃]⁻转化为气体离去,不改变正极材料的同时给嵌锂石墨补充锂单质,从而可以保持电池原结构,D正确。
2. (2025·辽吉黑内蒙古卷,3分)一种基于${Cu_{2}O}$的储氯电池装置如图,放电过程中a、b极均增重。若将b极换成${Ag/AgCl}$电极,b极仍增重。关于图中装置所示电池,下列说法错误的是 (
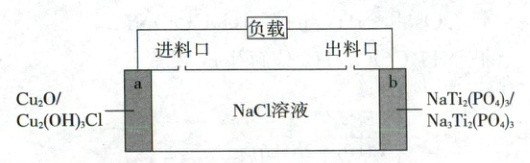
A.放电时${Na^{+}}$向b极迁移
B.该电池可用于海水脱盐
C.a极反应:${Cu_{2}O + 2H_{2}O + Cl^{-} - 2e^{-}\xlongequal{}Cu_{2}(OH)_{3}Cl + H^{+}}$
D.若以${Ag/AgCl}$电极代替a极,电池将失去储氯能力
D
)
A.放电时${Na^{+}}$向b极迁移
B.该电池可用于海水脱盐
C.a极反应:${Cu_{2}O + 2H_{2}O + Cl^{-} - 2e^{-}\xlongequal{}Cu_{2}(OH)_{3}Cl + H^{+}}$
D.若以${Ag/AgCl}$电极代替a极,电池将失去储氯能力
答案:
2.D 原电池工作原理
【电池分析】
负
CuO/
Cu(OH)₃Cl
CuO−2e⁻+2H₂O+Cl⁻=Cu(OH)₃Cl
NaTi₂(PO₄)₃+2e⁻=
放电时,阳离子向正极迁移,A正确;由电极反应可知该电池工作时可消耗NaCl,可用于海水脱盐,B正确;由【电池分析】可知,C正确;由题意可知若将b极换成Ag/AgCl电极,b极仍增重,说明此时b极为负极,电极反应为Ag−e⁻+Cl⁻=AgCl,若以Ag/AgCl电极代替a极,a极仍为负极,仍具有储氯功能,D错误。
【电池分析】
负
CuO/
Cu(OH)₃Cl
CuO−2e⁻+2H₂O+Cl⁻=Cu(OH)₃Cl
NaTi₂(PO₄)₃+2e⁻=
放电时,阳离子向正极迁移,A正确;由电极反应可知该电池工作时可消耗NaCl,可用于海水脱盐,B正确;由【电池分析】可知,C正确;由题意可知若将b极换成Ag/AgCl电极,b极仍增重,说明此时b极为负极,电极反应为Ag−e⁻+Cl⁻=AgCl,若以Ag/AgCl电极代替a极,a极仍为负极,仍具有储氯功能,D错误。
3. (2025·北京卷,3分)用电解${Na_{2}SO_{4}}$溶液(图1)后的石墨电极1、2探究氢氧燃料电池,重新取${Na_{2}SO_{4}}$溶液并用图2装置按ⅰ$\to$ⅳ顺序依次完成实验。
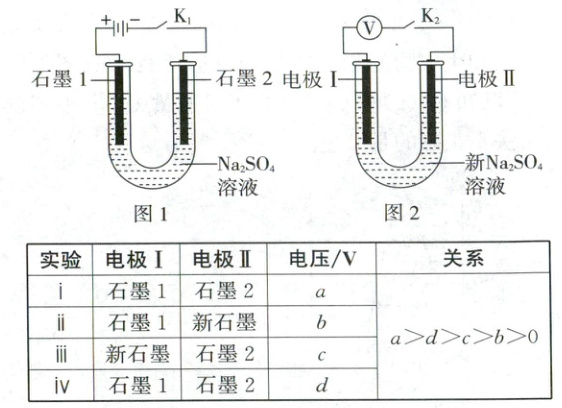
下列分析不正确的是 (
A.$a > 0$,说明实验ⅰ中形成原电池,反应为${2H_{2} + O_{2}\xlongequal{}2H_{2}O}$
B.$b < d$,是因为ⅱ中电极Ⅱ上缺少${H_{2}}$作为还原剂
C.$c > 0$,说明ⅲ中电极Ⅰ上有${O_{2}}$发生反应
D.$d > c$,是因为电极Ⅱ上吸附${H_{2}}$的量:ⅳ$ > $ⅲ

下列分析不正确的是 (
D
)A.$a > 0$,说明实验ⅰ中形成原电池,反应为${2H_{2} + O_{2}\xlongequal{}2H_{2}O}$
B.$b < d$,是因为ⅱ中电极Ⅱ上缺少${H_{2}}$作为还原剂
C.$c > 0$,说明ⅲ中电极Ⅰ上有${O_{2}}$发生反应
D.$d > c$,是因为电极Ⅱ上吸附${H_{2}}$的量:ⅳ$ > $ⅲ
答案:
3.D 氢氧燃料电池
【实验剖析】电解Na₂SO₄溶液过程中,石墨1为阳极,石墨2为阴极,电解过程中生成的氧气和氢气分别附着在石墨1、石墨2电极上,然后用吸附有氧气的石墨1电极、吸附有氢气的石墨2电极和新石墨电极依次完成实验i→iv,据此分析。
实验i中a>0,说明形成了原电池,即氢氧燃料电池,反应为2H₂+O₂=2H₂O,A正确;实验ii与实验iv的区别在于电极Ⅱ,实验ii中新石墨电极上缺少还原剂H₂,故电压较实验iv中小,B正确;实验iii中电压c>0,说明形成了原电池,石墨2电极上有氢气被氧化,则电极I(即新石墨电极)上有氧气被还原,C正确;实验iii与实验iv的主要区别在于电极I不同,实验iv中石墨1电极上吸附氧气的量远大于实验iii中的新石墨电极,使得实验iv电压大于实验iii,由于实验iv在实验iii之后进行,故电极Ⅱ上吸附氢气的量iv<iii,D错误。
【实验剖析】电解Na₂SO₄溶液过程中,石墨1为阳极,石墨2为阴极,电解过程中生成的氧气和氢气分别附着在石墨1、石墨2电极上,然后用吸附有氧气的石墨1电极、吸附有氢气的石墨2电极和新石墨电极依次完成实验i→iv,据此分析。
实验i中a>0,说明形成了原电池,即氢氧燃料电池,反应为2H₂+O₂=2H₂O,A正确;实验ii与实验iv的区别在于电极Ⅱ,实验ii中新石墨电极上缺少还原剂H₂,故电压较实验iv中小,B正确;实验iii中电压c>0,说明形成了原电池,石墨2电极上有氢气被氧化,则电极I(即新石墨电极)上有氧气被还原,C正确;实验iii与实验iv的主要区别在于电极I不同,实验iv中石墨1电极上吸附氧气的量远大于实验iii中的新石墨电极,使得实验iv电压大于实验iii,由于实验iv在实验iii之后进行,故电极Ⅱ上吸附氢气的量iv<iii,D错误。
4. (2025·安徽卷,3分)研究人员开发出一种锂-氢可充电电池(如图所示),使用前需先充电,其固体电解质仅允许${Li^{+}}$通过。下列说法正确的是 (
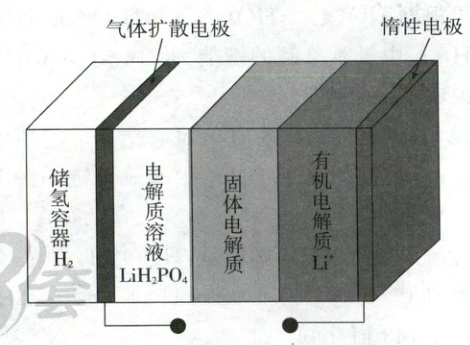
A.放电时电解质溶液质量减小
B.放电时电池总反应为${H_{2} + 2Li\xlongequal{}2LiH}$
C.充电时${Li^{+}}$移向惰性电极
D.充电时每转移$1\ mol$电子,$c{(H^{+})}$降低$1\ mol/L$
C
)
A.放电时电解质溶液质量减小
B.放电时电池总反应为${H_{2} + 2Li\xlongequal{}2LiH}$
C.充电时${Li^{+}}$移向惰性电极
D.充电时每转移$1\ mol$电子,$c{(H^{+})}$降低$1\ mol/L$
答案:
4.C 电化学原理
【电池分析】
充H₂放2H₂−电e⁻+2H₃PO₄=2H₂PO₄⁻+H₂↑
放充Li⁺电+e⁻=Li
放电时,每转移2mole⁻,正极电解质溶液生成1molH₂的同时,有2molLi⁺由负极区迁移至电解质溶液中,则电解质溶液质量增大,A错误;放电时电池的总反应为2Li+2H₃PO₄=2LiH₂PO₄+H₂↑,B错误;充电时Li⁺向阴极即惰性电极迁移,C正确;充电时电解质溶液中c(H⁺)增大,但电解质溶液体积未知且H₃PO₄为中强酸,c(H⁺)的变化量无法计算,D错误。
【电池分析】
充H₂放2H₂−电e⁻+2H₃PO₄=2H₂PO₄⁻+H₂↑
放充Li⁺电+e⁻=Li
放电时,每转移2mole⁻,正极电解质溶液生成1molH₂的同时,有2molLi⁺由负极区迁移至电解质溶液中,则电解质溶液质量增大,A错误;放电时电池的总反应为2Li+2H₃PO₄=2LiH₂PO₄+H₂↑,B错误;充电时Li⁺向阴极即惰性电极迁移,C正确;充电时电解质溶液中c(H⁺)增大,但电解质溶液体积未知且H₃PO₄为中强酸,c(H⁺)的变化量无法计算,D错误。
查看更多完整答案,请扫码查看


