2025年天利38套五年真题高考试题分类化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年天利38套五年真题高考试题分类化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第56页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
5. (2024·北京卷,3分)酸性锌锰干电池的构造示意图如下。关于该电池及其工作原理,下列说法正确的是 (
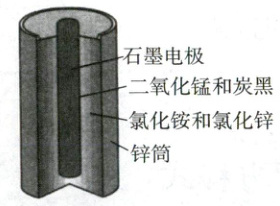
A.石墨作电池的负极材料
B.电池工作时,${NH^{+}_{4}}$向负极方向移动
C.${MnO_{2}}$发生氧化反应
D.锌筒发生的电极反应为${Zn - 2e^{-}\xlongequal{}Zn^{2+}}$
D
)
A.石墨作电池的负极材料
B.电池工作时,${NH^{+}_{4}}$向负极方向移动
C.${MnO_{2}}$发生氧化反应
D.锌筒发生的电极反应为${Zn - 2e^{-}\xlongequal{}Zn^{2+}}$
答案:
5.D 化学电源 酸性锌锰干电池,锌筒为负极,石墨电极为正极,负极发生失电子的氧化反应Zn−2e⁻=Zn²⁺,A错误,D正确;原电池工作时,阳离子向正极(石墨电极)方向移动,B错误;MnO₂发生得电子的还原反应,C错误。
6. 【创新试题】(2024·新课标卷,6分)一种可植入体内的微型电池工作原理如图所示,通过${CuO}$催化消耗血糖发电,从而控制血糖浓度。当传感器检测到血糖浓度高于标准,电池启动。血糖浓度下降至标准,电池停止工作。(血糖浓度以葡萄糖浓度计)
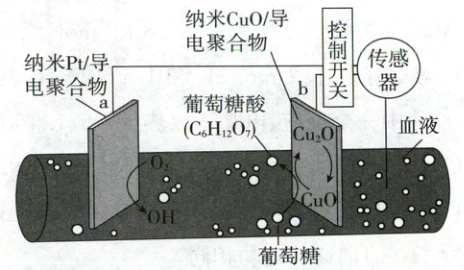
电池工作时,下列叙述错误的是 (
A.电池总反应为:${2C_{6}H_{12}O_{6} + O_{2}\xlongequal{}2C_{6}H_{12}O_{7}}$
B.b电极上${CuO}$通过${Cu}$(Ⅱ)和${Cu}$(Ⅰ)相互转变起催化作用
C.消耗$18\ mg$葡萄糖,理论上a电极有$0.4\ mmol$电子流入
D.两电极间血液中的${Na^{+}}$在电场驱动下的迁移方向为b\toa

电池工作时,下列叙述错误的是 (
C
)A.电池总反应为:${2C_{6}H_{12}O_{6} + O_{2}\xlongequal{}2C_{6}H_{12}O_{7}}$
B.b电极上${CuO}$通过${Cu}$(Ⅱ)和${Cu}$(Ⅰ)相互转变起催化作用
C.消耗$18\ mg$葡萄糖,理论上a电极有$0.4\ mmol$电子流入
D.两电极间血液中的${Na^{+}}$在电场驱动下的迁移方向为b\toa
答案:
6.C 原电池原理
【电池分析】b电极发生的反应属于协同反应,表面上看是Cu₂O失电子,实际上真正的负极活性物质是葡萄糖。
电极 电极反应式
正极(a电极) O₂+4e⁻+2H₂O=4OH⁻
负极(b电极) 2CuO+C₆H₁₂O₆=Cu₂O+C₆H₁₂O₇
Cu₂O−2e⁻+2OH⁻=2CuO+H₂O
每消耗一个葡萄糖分子会转移两个电子,18mg葡萄糖物质的量为0.1mmol,转移电子的物质的量为0.2mmol,理论上a电极流入0.2mmol电子,C错误。
【电池分析】b电极发生的反应属于协同反应,表面上看是Cu₂O失电子,实际上真正的负极活性物质是葡萄糖。
电极 电极反应式
正极(a电极) O₂+4e⁻+2H₂O=4OH⁻
负极(b电极) 2CuO+C₆H₁₂O₆=Cu₂O+C₆H₁₂O₇
Cu₂O−2e⁻+2OH⁻=2CuO+H₂O
每消耗一个葡萄糖分子会转移两个电子,18mg葡萄糖物质的量为0.1mmol,转移电子的物质的量为0.2mmol,理论上a电极流入0.2mmol电子,C错误。
7. (2024·江西卷,3分)我国学者发明了一种新型多功能甲醛-硝酸盐电池,可同时处理废水中的甲醛和硝酸根离子(如图)。下列说法正确的是 (
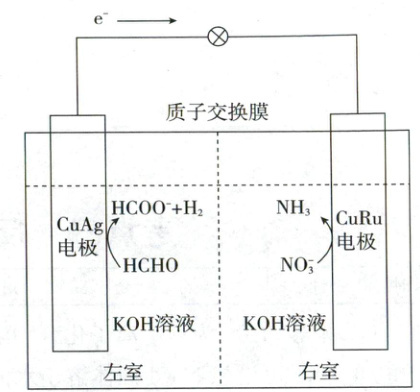
A.${CuAg}$电极反应为${2HCHO + 2H_{2}O - 4e^{-}\xlongequal{}2HCOO^{-} + H_{2}\uparrow + 2OH^{-}}$
B.${CuRu}$电极反应为${NO^{-}_{3} + 6H_{2}O + 8e^{-}\xlongequal{}NH_{3}\uparrow + 9OH^{-}}$
C.放电过程中,${OH^{-}}$通过质子交换膜从左室传递到右室
D.处理废水过程中溶液${pH}$不变,无需补加${KOH}$
B
)
A.${CuAg}$电极反应为${2HCHO + 2H_{2}O - 4e^{-}\xlongequal{}2HCOO^{-} + H_{2}\uparrow + 2OH^{-}}$
B.${CuRu}$电极反应为${NO^{-}_{3} + 6H_{2}O + 8e^{-}\xlongequal{}NH_{3}\uparrow + 9OH^{-}}$
C.放电过程中,${OH^{-}}$通过质子交换膜从左室传递到右室
D.处理废水过程中溶液${pH}$不变,无需补加${KOH}$
答案:
7.B 新型化学电源
【电池分析】
电极 电极反应式
正极(CuRu电极) NO₃⁻+6H₂O+8e⁻=NH₃↑+9OH⁻
负极(CuAg电极) 2HCHO−2e⁻+4OH⁻=2HCOO⁻+H₂↑+2H₂O
总反应 8HCHO+7OH⁻+NO₃⁻=NH₃↑+4H₂↑+8HCOO⁻+2H₂O
由【电池分析】可知,A错误、B正确;质子交换膜不允许OH⁻通过,C错误;处理废水过程中溶液pH发生变化且总反应会消耗OH⁻,需要补加KOH,D错误。
【电池分析】
电极 电极反应式
正极(CuRu电极) NO₃⁻+6H₂O+8e⁻=NH₃↑+9OH⁻
负极(CuAg电极) 2HCHO−2e⁻+4OH⁻=2HCOO⁻+H₂↑+2H₂O
总反应 8HCHO+7OH⁻+NO₃⁻=NH₃↑+4H₂↑+8HCOO⁻+2H₂O
由【电池分析】可知,A错误、B正确;质子交换膜不允许OH⁻通过,C错误;处理废水过程中溶液pH发生变化且总反应会消耗OH⁻,需要补加KOH,D错误。
8. (2023·海南卷,2分)利用金属${Al}$、海水及其中的溶解氧可组成电池,如图所示。下列说法正确的是 (
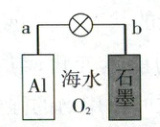
A.b电极为电池正极
B.电池工作时,海水中的${Na^{+}}$向a电极移动
C.电池工作时,紧邻a电极区域的海水呈强碱性
D.每消耗$1\ kg\ {Al}$,电池最多向外提供$37\ mol$电子的电量
A
)
A.b电极为电池正极
B.电池工作时,海水中的${Na^{+}}$向a电极移动
C.电池工作时,紧邻a电极区域的海水呈强碱性
D.每消耗$1\ kg\ {Al}$,电池最多向外提供$37\ mol$电子的电量
答案:
8.A 原电池原理
【电池分析】利用金属Al、石墨、海水及其中的溶解氧构成的原电池中,Al为活泼金属,失电子,发生氧化反应,则a电极为电池负极,电极反应式为Al−3e⁻=Al³⁺,b电极为电池正极,电极反应式为O₂+4e⁻+2H₂O=4OH⁻。
由分析可知,a电极为电池负极,b电极为电池正极,故A正确;原电池工作时,阳离子向正极移动,即海水中的Na⁺向b电极移动,故B错误;原电池工作时,a电极为负极,负极反应式为Al−3e⁻=Al³⁺,a电极区域Al³⁺水解使海水呈弱酸性,故C错误;负极反应式为Al−3e⁻=Al³⁺,1kgAl的物质的量为$\frac{1000g}{27g/mol}≈37mol,$则电池最多向外提供37mol×3=111mol电子的电量,故D错误。
真题互鉴
与2022年湖南卷,8题有相互借鉴的价值,两道题都是以海水−金属−电池为命题背景,海水为电解质溶液、活泼金属为负极、氧气在正极得电子,考查点均涉及正负极判断、电极反应式、离子移动方向等。
答33
【电池分析】利用金属Al、石墨、海水及其中的溶解氧构成的原电池中,Al为活泼金属,失电子,发生氧化反应,则a电极为电池负极,电极反应式为Al−3e⁻=Al³⁺,b电极为电池正极,电极反应式为O₂+4e⁻+2H₂O=4OH⁻。
由分析可知,a电极为电池负极,b电极为电池正极,故A正确;原电池工作时,阳离子向正极移动,即海水中的Na⁺向b电极移动,故B错误;原电池工作时,a电极为负极,负极反应式为Al−3e⁻=Al³⁺,a电极区域Al³⁺水解使海水呈弱酸性,故C错误;负极反应式为Al−3e⁻=Al³⁺,1kgAl的物质的量为$\frac{1000g}{27g/mol}≈37mol,$则电池最多向外提供37mol×3=111mol电子的电量,故D错误。
真题互鉴
与2022年湖南卷,8题有相互借鉴的价值,两道题都是以海水−金属−电池为命题背景,海水为电解质溶液、活泼金属为负极、氧气在正极得电子,考查点均涉及正负极判断、电极反应式、离子移动方向等。
答33
9. (2023·广东卷,2分)负载有${Pt}$和${Ag}$的活性炭,可选择性去除${Cl^{-}}$实现废酸的纯化,其工作原理如图。下列说法正确的是 (
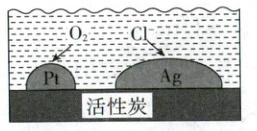
A.${Ag}$作原电池正极
B.电子由${Ag}$经活性炭流向${Pt}$
C.${Pt}$表面发生的电极反应:${O_{2} + 2H_{2}O + 4e^{-}\xlongequal{}4OH^{-}}$
D.每消耗标准状况下$11.2\ L$的${O_{2}}$,最多去除$1\ mol\ {Cl^{-}}$
B
)
A.${Ag}$作原电池正极
B.电子由${Ag}$经活性炭流向${Pt}$
C.${Pt}$表面发生的电极反应:${O_{2} + 2H_{2}O + 4e^{-}\xlongequal{}4OH^{-}}$
D.每消耗标准状况下$11.2\ L$的${O_{2}}$,最多去除$1\ mol\ {Cl^{-}}$
答案:
9.B 原电池原理
【电池分析】
Ag作原电池负极,A错误;原电池工作时,电子由负极经外电路流向正极,即电子由Ag经活性炭流向Pt,B正确;废酸纯化,电解质溶液呈酸性,Pt表面发生的电极反应式为O₂+4e⁻+4H⁺=2H₂O,C错误;每消耗标准状况下11.2L的O₂,电路中转移2mole⁻,最多去除2molCl⁻,D错误。
【电池分析】
Ag作原电池负极,A错误;原电池工作时,电子由负极经外电路流向正极,即电子由Ag经活性炭流向Pt,B正确;废酸纯化,电解质溶液呈酸性,Pt表面发生的电极反应式为O₂+4e⁻+4H⁺=2H₂O,C错误;每消耗标准状况下11.2L的O₂,电路中转移2mole⁻,最多去除2molCl⁻,D错误。
查看更多完整答案,请扫码查看


