第63页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
3.(舟山重点中学自主招生)镁将成为21世纪重要的轻型环保材料,我国含有非常丰富的镁资源。
(1)金属镁是一种较活泼的金属,在二氧化碳气体中也能燃烧。燃烧的化学方程式为${2Mg + CO2 \xlongequal{点燃} C + 2MgO}$,此反应类型属于
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)镁铝合金广泛用于火箭、导弹和飞机制造业等。某兴趣小组为探究镁铝合金的组成,取7.8 g镁铝合金样品,投入足量的稀硫酸中,共收集得到0.8 g氢气,则该合金中,镁和铝的质量比为
(3)老师每次进行有关镁的实验时都会强调镁是一种银白色、有金属光泽的金属,但拿出的镁总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是${MgO}$;小亮认为可能是${Mg2(OH)2CO3}$;小龙认为可能是${Mg(OH)2}$。
小龙认为小明的猜想是错误的,其理由是
实验探究:小亮按如图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时受热的试管内产生了白色固体。
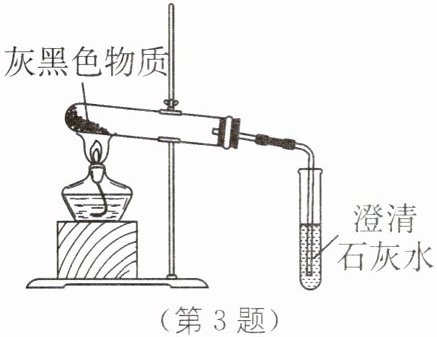
实验分析:实验后,小亮认为小龙的猜测也是错误的,其理由是
查阅资料得出结论:${Mg2(OH)2CO3}和{Mg(OH)2}$都可以受热分解,产物均为氧化物,据此请你写出${Mg2(OH)2CO3}$受热分解的化学方程式:
(4)将一些氧化铜粉末加入100 g质量分数为26.13%的硫酸中,微热至氧化铜全部溶解,再向该溶液中加入20 g镁粉,充分反应后,过滤、烘干,得到干燥的固体物质仍为20 g。求得到的固体中铜的质量。(不考虑镁与水的反应)
解:设反应中消耗镁的质量为x。
H₂SO₄~MgSO₄~Mg
98 24
100 g×26.13% x
$\frac{98}{24}$=$\frac{100\ \text{g}×26.13\%}{x}$ x≈6.4 g
由题意得,生成铜的质量与减少的镁的质量相等,所以Cu的质量为6.4 g。
答:得到的固体中铜的质量为6.4 g。
(1)金属镁是一种较活泼的金属,在二氧化碳气体中也能燃烧。燃烧的化学方程式为${2Mg + CO2 \xlongequal{点燃} C + 2MgO}$,此反应类型属于
C
(填字母)。A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)镁铝合金广泛用于火箭、导弹和飞机制造业等。某兴趣小组为探究镁铝合金的组成,取7.8 g镁铝合金样品,投入足量的稀硫酸中,共收集得到0.8 g氢气,则该合金中,镁和铝的质量比为
4:9
。(3)老师每次进行有关镁的实验时都会强调镁是一种银白色、有金属光泽的金属,但拿出的镁总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是${MgO}$;小亮认为可能是${Mg2(OH)2CO3}$;小龙认为可能是${Mg(OH)2}$。
小龙认为小明的猜想是错误的,其理由是
MgO是白色固体,不是灰黑色
。实验探究:小亮按如图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时受热的试管内产生了白色固体。

实验分析:实验后,小亮认为小龙的猜测也是错误的,其理由是
Mg(OH)₂中不含碳元素,加热分解不可能产生二氧化碳
。查阅资料得出结论:${Mg2(OH)2CO3}和{Mg(OH)2}$都可以受热分解,产物均为氧化物,据此请你写出${Mg2(OH)2CO3}$受热分解的化学方程式:
Mg₂(OH)₂CO₃$\stackrel{\triangle}{=}$2MgO+H₂O+CO₂↑
。(4)将一些氧化铜粉末加入100 g质量分数为26.13%的硫酸中,微热至氧化铜全部溶解,再向该溶液中加入20 g镁粉,充分反应后,过滤、烘干,得到干燥的固体物质仍为20 g。求得到的固体中铜的质量。(不考虑镁与水的反应)
解:设反应中消耗镁的质量为x。
H₂SO₄~MgSO₄~Mg
98 24
100 g×26.13% x
$\frac{98}{24}$=$\frac{100\ \text{g}×26.13\%}{x}$ x≈6.4 g
由题意得,生成铜的质量与减少的镁的质量相等,所以Cu的质量为6.4 g。
答:得到的固体中铜的质量为6.4 g。
答案:
3.
(1)C
(2)4:9
(3)MgO是白色固体,不是灰黑色 Mg(OH)₂中不含碳元素,加热分解不可能产生二氧化碳 Mg₂(OH)₂CO₃$\stackrel{\triangle}{=}$2MgO+H₂O+CO₂↑
(4)解:设反应中消耗镁的质量为x。
H₂SO₄~MgSO₄~Mg
98 24
100 g×26.13% x
$\frac{98}{24}$=$\frac{100\ \text{g}×26.13\%}{x}$ x≈6.4 g
由题意得,生成铜的质量与减少的镁的质量相等,所以Cu的质量为6.4 g。
答:得到的固体中铜的质量为6.4 g。
(1)C
(2)4:9
(3)MgO是白色固体,不是灰黑色 Mg(OH)₂中不含碳元素,加热分解不可能产生二氧化碳 Mg₂(OH)₂CO₃$\stackrel{\triangle}{=}$2MgO+H₂O+CO₂↑
(4)解:设反应中消耗镁的质量为x。
H₂SO₄~MgSO₄~Mg
98 24
100 g×26.13% x
$\frac{98}{24}$=$\frac{100\ \text{g}×26.13\%}{x}$ x≈6.4 g
由题意得,生成铜的质量与减少的镁的质量相等,所以Cu的质量为6.4 g。
答:得到的固体中铜的质量为6.4 g。
查看更多完整答案,请扫码查看


