第34页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
6.(2025·浙共体学能诊断)物质的结构与功能相适应,其性质与现象具有关联性。甲是初中科学中的常见物质,请根据下列叙述回答问题。
(1)若甲能与稀硫酸反应生成一种在标准状况下密度最小的气体,可知甲在常见的金属活动性顺序中的位置为
(2)若甲是一种红色的氧化物,能溶于稀盐酸,得到黄色溶液,则甲的化学式为
(3)若甲能与水反应,将少量甲加入澄清石灰水中,溶液变浑浊,则下列说法正确的是
A. 甲可能是二氧化碳
B. 甲可能是氧化钙
C. 反应前后溶剂的质量保持不变
D. 反应前后溶质的质量一定减小
(1)若甲能与稀硫酸反应生成一种在标准状况下密度最小的气体,可知甲在常见的金属活动性顺序中的位置为
氢之前
(填“氢之前”或“氢之后”)的金属。(2)若甲是一种红色的氧化物,能溶于稀盐酸,得到黄色溶液,则甲的化学式为
Fe₂O₃
。(3)若甲能与水反应,将少量甲加入澄清石灰水中,溶液变浑浊,则下列说法正确的是
ABD
(填字母)。A. 甲可能是二氧化碳
B. 甲可能是氧化钙
C. 反应前后溶剂的质量保持不变
D. 反应前后溶质的质量一定减小
答案:
(1)氢之前
(2)Fe₂O₃
(3)ABD
[解析]
(1)标准状况下密度最小的气体为氢气,金属活动性在氢前面的金属可以与酸反应产生氢气,甲能与稀硫酸反应生成氢气,所以甲是氢前面的金属。
(2)铁离子在溶液中显黄色,甲是一种红色的氧化物,能溶于稀盐酸,得到黄色溶液,故红色氧化物为氧化铁,其化学式为Fe₂O₃。
(3)二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀,澄清石灰水变浑浊,A正确;氧化钙与反应水生成氢氧化钙,反应消耗水且剧烈放热,温度升高,氢氧化钙的溶解度减小,有晶体析出,溶液变浑浊,B正确;若甲为氧化钙,氧化钙与水反应生成氢氧化钙,会导致溶剂质量减小,C错误;若甲为二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,溶液中的溶质质量减小,若甲为氧化钙,氧化钙与水反应生成氢氧化钙,水的质量减小,且该反应放热,氢氧化钙的溶解度随温度升高而下降,所以溶解的氢氧化钙减少,所以溶液中的溶质质量减小,D正确。
(1)氢之前
(2)Fe₂O₃
(3)ABD
[解析]
(1)标准状况下密度最小的气体为氢气,金属活动性在氢前面的金属可以与酸反应产生氢气,甲能与稀硫酸反应生成氢气,所以甲是氢前面的金属。
(2)铁离子在溶液中显黄色,甲是一种红色的氧化物,能溶于稀盐酸,得到黄色溶液,故红色氧化物为氧化铁,其化学式为Fe₂O₃。
(3)二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀,澄清石灰水变浑浊,A正确;氧化钙与反应水生成氢氧化钙,反应消耗水且剧烈放热,温度升高,氢氧化钙的溶解度减小,有晶体析出,溶液变浑浊,B正确;若甲为氧化钙,氧化钙与水反应生成氢氧化钙,会导致溶剂质量减小,C错误;若甲为二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,溶液中的溶质质量减小,若甲为氧化钙,氧化钙与水反应生成氢氧化钙,水的质量减小,且该反应放热,氢氧化钙的溶解度随温度升高而下降,所以溶解的氢氧化钙减少,所以溶液中的溶质质量减小,D正确。
7. 兴趣小组为探究Fe、Cu、Ag三种金属的活动性,将铜片放入硝酸银溶液中,观察到铜片表面出现银白色物质。一段时间后将图1试管中的物质过滤,向滤液中加铁片,析出固体的质量随时间变化如图2所示,下列说法错误的是(
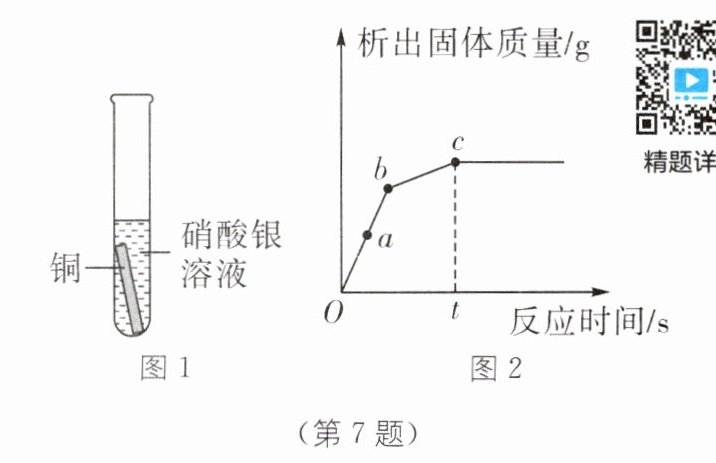
A.该实验可以证明金属的活动性:Fe>Cu>Ag
B.试管中的物质过滤后,滤液中的溶质有两种
C.a点对应的溶质有$Cu(NO_3)_2、$$AgNO_3$
D.bc段析出的固体是铜
C
)。
A.该实验可以证明金属的活动性:Fe>Cu>Ag
B.试管中的物质过滤后,滤液中的溶质有两种
C.a点对应的溶质有$Cu(NO_3)_2、$$AgNO_3$
D.bc段析出的固体是铜
答案:
C [解析]硝酸银与铜反应生成银和硝酸铜,则反应后的图1试管中的物质一定含有硝酸铜,可能含有硝酸银;向滤液中加铁片,铁的金属活动性比银、铜强,若滤液含硝酸银,铁先与硝酸银反应生成硝酸亚铁和银,待硝酸银反应完全后,若还有铁,铁才能与硝酸铜反应生成硝酸亚铁和铜,由图2可知,Ob段发生铁与硝酸银的反应,bc段发生的是铁与硝酸铜反应生成硝酸亚铁和铜,将铜片放入硝酸银溶液中,观察到铜片表面出现银白色物质,说明金属活动性:铜>银;向滤液中加铁片,根据图2中析出固体的质量可以看出,铁先与硝酸银反应,再与硝酸铜反应,说明金属活动性:Fe>Cu>Ag,A正确;由图2可知,图2有两个拐点,说明加入铁后有两个反应发生,试管中的物质过滤后,滤液中的溶质有两种,为硝酸铜和硝酸银,B正确;a点对应铁与部分硝酸银反应,溶液中所含的溶质是剩余的硝酸银、硝酸铜和生成的硝酸亚铁,C错误;bc段发生的是铁与硝酸铜反应生成硝酸亚铁和铜,析出的固体是铜,D正确。
8.(2024·陕西中考)化学课堂上,老师为同学们演示了如下图所示的实验。

(1)铜丝插入$AgNO_3$溶液一段时间后,观察到的两个现象分别是
(2)铝丝表面析出红色固体时,试管内溶液中的溶质一定有

(1)铜丝插入$AgNO_3$溶液一段时间后,观察到的两个现象分别是
铜丝表面出现银白色固体,溶液由无色变成蓝色
,发生反应的化学方程式是Cu+2AgNO₃=Cu(NO₃)₂+2Ag
。(2)铝丝表面析出红色固体时,试管内溶液中的溶质一定有
硝酸铝
。
答案:
(1)铜丝表面出现银白色固体,溶液由无色变成蓝色根据金属活动性顺序,结合Cu²⁺在溶液中为蓝色进行作答。
Cu+2AgNO₃=Cu(NO₃)₂+2Ag
(2)硝酸铝
[解析]
(1)铜和硝酸银反应生成银和硝酸铜,反应的现象为铜丝表面出现银白色固体,溶液由无色变成蓝色;反应的化学方程式是Cu+2AgNO₃=Cu(NO₃)₂+2Ag。
(2)铝丝表面析出红色固体是因为铝和硝酸铜反应生成了铜和硝酸铝,所以试管内溶液中的溶质一定有硝酸铝。
(1)铜丝表面出现银白色固体,溶液由无色变成蓝色根据金属活动性顺序,结合Cu²⁺在溶液中为蓝色进行作答。
Cu+2AgNO₃=Cu(NO₃)₂+2Ag
(2)硝酸铝
[解析]
(1)铜和硝酸银反应生成银和硝酸铜,反应的现象为铜丝表面出现银白色固体,溶液由无色变成蓝色;反应的化学方程式是Cu+2AgNO₃=Cu(NO₃)₂+2Ag。
(2)铝丝表面析出红色固体是因为铝和硝酸铜反应生成了铜和硝酸铝,所以试管内溶液中的溶质一定有硝酸铝。
9.(2024·黑龙江中考)金属材料在人类发展的历史长河中起着非常重要的作用。
(1)探究Mg、Fe、Cu的金属活动性顺序,下列试剂的选择方案正确的是
A. Mg、Cu、$FeSO_4$溶液
B. Fe、$MgSO_4$溶液、$CuSO_4$溶液
C. Mg、Fe、Cu、稀盐酸
D. Cu、$MgSO_4$溶液、$FeSO_4$溶液
(2)向$Cu(NO_3)_2$溶液中加入Mg、Zn、Ag三种金属,充分反应后过滤,得到无色滤液和滤渣。一定发生反应的化学方程式为
(1)探究Mg、Fe、Cu的金属活动性顺序,下列试剂的选择方案正确的是
ABC
(填字母)。A. Mg、Cu、$FeSO_4$溶液
B. Fe、$MgSO_4$溶液、$CuSO_4$溶液
C. Mg、Fe、Cu、稀盐酸
D. Cu、$MgSO_4$溶液、$FeSO_4$溶液
(2)向$Cu(NO_3)_2$溶液中加入Mg、Zn、Ag三种金属,充分反应后过滤,得到无色滤液和滤渣。一定发生反应的化学方程式为
Cu(NO₃)₂+Mg=Cu+Mg(NO₃)₂
。向滤渣中加入一定量的稀盐酸,有气泡产生,滤渣中一定有 Zn、Cu、Ag
(填化学式,下同),滤液中可能含有的溶质是 Zn(NO₃)₂
。
答案:
(1)ABC
(2)Cu(NO₃)₂+Mg=Cu+Mg(NO₃)₂ Zn、Cu、Ag Zn(NO₃)₂
[解析]
(1)镁能与硫酸亚铁反应生成硫酸镁和铁,有黑色固体析出,说明镁比铁活泼,铜与硫酸亚铁不反应,无明显现象,说明铁比铜活泼,可以探究三种金属的活动性顺序,A符合题意;铁与硫酸镁不反应,无明显现象,说明镁比铁活泼,铁与硫酸铜反应生成硫酸亚铁和铜,有红色固体析出,说明铁比铜活泼,可以探究三种金属的活动性顺序,B符合题意;镁、铁均能与稀盐酸反应生成氢气,且镁与酸反应速率较快,铁与酸反应速率较慢,说明在金属活动性顺序里,镁、铁排在氢前,且镁比铁活泼,铜与稀盐酸不反应,无明显现象,说明铜排在氢后,可以探究三种金属的活动性顺序,C符合题意;铜与硫酸镁不反应,无明显现象,说明镁比铜活泼,铜与硫酸亚铁不反应,无明显现象,说明铁比铜活泼,但是无法探究镁和铁的金属活动性顺序,D不符合题意。
(2)金属活动性:Mg>Zn>Cu>Ag,向硝酸铜溶液中加入镁、锌、银三种金属,镁先与硝酸铜反应生成硝酸镁和铜,待镁完全反应后,锌和硝酸铜反应生成硝酸锌和铜,银和硝酸铜不反应,充分反应后过滤,得到无色滤液和滤渣,说明硝酸铜已经完全反应。由分析可知,一定发生的反应为镁和硝酸铜反应生成硝酸镁和铜,该反应的化学方程式为Cu(NO₃)₂+Mg=Cu+Mg(NO₃)₂;向滤渣中加入一定量的稀盐酸,有气泡产生,则滤渣中一定含锌,镁一定与硝酸铜反应生成铜,银不参与反应,则滤渣中一定有Zn、Cu、Ag;镁一定与硝酸铜反应生成了硝酸镁,硝酸铜完全反应,故滤液中一定含硝酸镁,一定不含硝酸铜,锌可能参与反应,也可能没有参与反应,故滤液中可能含有的溶质是Zn(NO₃)₂。
(1)ABC
(2)Cu(NO₃)₂+Mg=Cu+Mg(NO₃)₂ Zn、Cu、Ag Zn(NO₃)₂
[解析]
(1)镁能与硫酸亚铁反应生成硫酸镁和铁,有黑色固体析出,说明镁比铁活泼,铜与硫酸亚铁不反应,无明显现象,说明铁比铜活泼,可以探究三种金属的活动性顺序,A符合题意;铁与硫酸镁不反应,无明显现象,说明镁比铁活泼,铁与硫酸铜反应生成硫酸亚铁和铜,有红色固体析出,说明铁比铜活泼,可以探究三种金属的活动性顺序,B符合题意;镁、铁均能与稀盐酸反应生成氢气,且镁与酸反应速率较快,铁与酸反应速率较慢,说明在金属活动性顺序里,镁、铁排在氢前,且镁比铁活泼,铜与稀盐酸不反应,无明显现象,说明铜排在氢后,可以探究三种金属的活动性顺序,C符合题意;铜与硫酸镁不反应,无明显现象,说明镁比铜活泼,铜与硫酸亚铁不反应,无明显现象,说明铁比铜活泼,但是无法探究镁和铁的金属活动性顺序,D不符合题意。
(2)金属活动性:Mg>Zn>Cu>Ag,向硝酸铜溶液中加入镁、锌、银三种金属,镁先与硝酸铜反应生成硝酸镁和铜,待镁完全反应后,锌和硝酸铜反应生成硝酸锌和铜,银和硝酸铜不反应,充分反应后过滤,得到无色滤液和滤渣,说明硝酸铜已经完全反应。由分析可知,一定发生的反应为镁和硝酸铜反应生成硝酸镁和铜,该反应的化学方程式为Cu(NO₃)₂+Mg=Cu+Mg(NO₃)₂;向滤渣中加入一定量的稀盐酸,有气泡产生,则滤渣中一定含锌,镁一定与硝酸铜反应生成铜,银不参与反应,则滤渣中一定有Zn、Cu、Ag;镁一定与硝酸铜反应生成了硝酸镁,硝酸铜完全反应,故滤液中一定含硝酸镁,一定不含硝酸铜,锌可能参与反应,也可能没有参与反应,故滤液中可能含有的溶质是Zn(NO₃)₂。
查看更多完整答案,请扫码查看


