2025年与名师对话高中新教材同步导练案化学C选择性必修1
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年与名师对话高中新教材同步导练案化学C选择性必修1 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第45页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1.下列过程为自发过程的是 ( )
①铵盐溶解 ②烧碱与盐酸的反应 ③锌与稀硫酸的反应 ④氢气在氧气中燃烧 ⑤镁在空气中燃烧 ⑥铝热反应 ⑦墨水在水中扩散 ⑧电解熔融氯化钠
A.①②③⑦
B.⑤⑥⑦⑧
C.②④⑥⑧
D.①②③④⑤⑥⑦
①铵盐溶解 ②烧碱与盐酸的反应 ③锌与稀硫酸的反应 ④氢气在氧气中燃烧 ⑤镁在空气中燃烧 ⑥铝热反应 ⑦墨水在水中扩散 ⑧电解熔融氯化钠
A.①②③⑦
B.⑤⑥⑦⑧
C.②④⑥⑧
D.①②③④⑤⑥⑦
答案:
A 自发过程是不借助任何外界条件即可发生的过程,①铵盐溶解吸收热量,混乱程度增大,是自发过程,②烧碱与盐酸的反应是中和反应,释放热量,是自发过程,③锌与稀硫酸的反应是自发过程,④氢气在氧气中燃烧需要点燃,不是自发过程,⑤镁在空气中燃烧需要点燃,不是自发过程,⑥铝热反应需要高温条件,不是自发过程,⑦墨水在水中扩散是自发过程,⑧电解熔融氯化钠需要通电,不是自发过程。
2.下列说法正确的是 ( )
A.所有自发进行的化学反应都是放热反应
B.熵减小的化学反应不能自发进行
C.有气体生成的反应一定是熵增大的反应
D.“冰,水为之,而寒于水”,水结冰过程中ΔH<0,ΔS<0
A.所有自发进行的化学反应都是放热反应
B.熵减小的化学反应不能自发进行
C.有气体生成的反应一定是熵增大的反应
D.“冰,水为之,而寒于水”,水结冰过程中ΔH<0,ΔS<0
答案:
D 反应能否自发进行取决于焓变和熵变的复合判据,对于吸热反应,在一定温度下也能自发进行,A错误;反应自发与否由焓变与熵变共同决定,熵减小的化学反应也可能自发进行,B错误;有气体生成的反应,反应前后气体不一定增多,不一定是熵增大的反应,C错误;同种物质,液态的能量大于固态,水结成冰的过程是熵减小的过程,即ΔS<0,且该过程是放热过程,即ΔH<0,D正确。
3.下列自发反应可用焓判据来解释的是 ( )
A.2N₂O₅(g)===4NO₂(g)+O₂(g) ΔH=+56.7 kJ·mol⁻¹
B.(NH₄)₂CO₃(s)===NH₄HCO₃(s)+NH₃(g) ΔH=+74.9 kJ·mol⁻¹
C.2H₂(g)+O₂(g)===2H₂O(l) ΔH=-286 kJ·mol⁻¹
D.CaCO₃(s)===CaO(s)+CO₂(g) ΔH=+178.2 kJ·mol⁻¹
A.2N₂O₅(g)===4NO₂(g)+O₂(g) ΔH=+56.7 kJ·mol⁻¹
B.(NH₄)₂CO₃(s)===NH₄HCO₃(s)+NH₃(g) ΔH=+74.9 kJ·mol⁻¹
C.2H₂(g)+O₂(g)===2H₂O(l) ΔH=-286 kJ·mol⁻¹
D.CaCO₃(s)===CaO(s)+CO₂(g) ΔH=+178.2 kJ·mol⁻¹
答案:
C 从焓变的角度分析,化学反应有由高能状态向低能状态转化,使体系能量降低的趋势,表现为放热反应较易进行。
4.下列对熵的理解不正确的是 ( )
A.同种物质气态时熵值最大,固态时熵值最小
B.体系越有序,熵值越小;越混乱,熵值越大
C.与外界隔离的体系,自发过程将导致体系的熵减小
D.25℃、1.01×10⁵ Pa时,2N₂O₅(g)===4NO₂(g)+O₂(g)是熵增反应
A.同种物质气态时熵值最大,固态时熵值最小
B.体系越有序,熵值越小;越混乱,熵值越大
C.与外界隔离的体系,自发过程将导致体系的熵减小
D.25℃、1.01×10⁵ Pa时,2N₂O₅(g)===4NO₂(g)+O₂(g)是熵增反应
答案:
C C项,体系都有从有序自发转变为无序的倾向,此过程为熵增过程,故错误。
5.已知在等温等压条件下,化学反应方向的判据为:
ΔH-TΔS<0 反应能自发进行
ΔH-TΔS=0 反应达到平衡状态
ΔH-TΔS>0 反应不能自发进行
设反应A ===D+E ΔH-TΔS=(-4500+11T)J·mol⁻¹,要防止反应发生,温度必须( )
A.高于409 K
B.低于136 K
C.高于136 K而低于409 K
D.低于409 K
ΔH-TΔS<0 反应能自发进行
ΔH-TΔS=0 反应达到平衡状态
ΔH-TΔS>0 反应不能自发进行
设反应A ===D+E ΔH-TΔS=(-4500+11T)J·mol⁻¹,要防止反应发生,温度必须( )
A.高于409 K
B.低于136 K
C.高于136 K而低于409 K
D.低于409 K
答案:
A 要防止反应发生需满足ΔH - TΔS>0的条件,解不等式得T>409 K,A正确。
6.下列对化学反应方向的说法,正确的是 ( )
A.同一物质的固、液、气三种状态的熵值递减
B.常温下反应2Na₂SO₃(s)+O₂(g)===2Na₂SO₄(s)能自发进行,则ΔH<0
C.CaCO₃(s)=高温=CaO(s)+CO₂(g) ΔH>0,ΔS>0,不论在何种条件下都不可能自发进行
D.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为判断反应能否自发进行的判据
A.同一物质的固、液、气三种状态的熵值递减
B.常温下反应2Na₂SO₃(s)+O₂(g)===2Na₂SO₄(s)能自发进行,则ΔH<0
C.CaCO₃(s)=高温=CaO(s)+CO₂(g) ΔH>0,ΔS>0,不论在何种条件下都不可能自发进行
D.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为判断反应能否自发进行的判据
答案:
B 同一物质的固、液、气三种状态的熵值递增,故A错误;反应的ΔS<0,由ΔG = ΔH - T·ΔS<0,反应可自发进行可知,ΔH<0,故B正确;能自发进行,应满足ΔH - T·ΔS<0,ΔH>0,ΔS>0,则应在高温下进行,故C错误;在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向,ΔH - TΔS<0,则能自发进行;ΔH - TΔS>0,则不能自发进行,故D错误。
7.橡皮筋在拉伸和收缩状态时结构如图。在其拉伸过程中有放热现象。
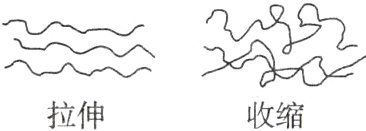
25℃、101 kPa时,下列过程的焓变、熵变和自发性与橡皮筋从拉伸状态到收缩状态一致的是( )
A.CaCO₃=高温=CaO+CO₂↑
B.NaOH的溶解
C.2H₂+O₂===2H₂O
D.Ba(OH)₂·8H₂O+2NH₄Cl===BaCl₂+2NH₃↑+10H₂O

25℃、101 kPa时,下列过程的焓变、熵变和自发性与橡皮筋从拉伸状态到收缩状态一致的是( )
A.CaCO₃=高温=CaO+CO₂↑
B.NaOH的溶解
C.2H₂+O₂===2H₂O
D.Ba(OH)₂·8H₂O+2NH₄Cl===BaCl₂+2NH₃↑+10H₂O
答案:
D 橡皮筋拉伸过程中有放热现象,则橡皮筋从拉伸状态变为收缩状态是吸热过程,混乱度增加,属于熵增过程且其在25℃、101 kPa时自发进行。CaCO₃分解是吸热反应,且熵增加,但CaCO₃在25℃、101 kPa时不会自发分解,A错误;NaOH溶解时放热,B错误;H₂在O₂中燃烧放热,C错误;该反应是吸热反应,且熵增加,在25℃、101 kPa时能自发进行,D正确。
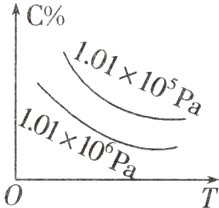
8.在一定条件下,对于反应mA(g)+nB(g)⇌cC(g)+dD(g),C物质的浓度(C%)与温度、压强的关系如图所示,下列判断正确的是 ( )
A.ΔH<0 ΔS>0
B.ΔH>0 ΔS<0
C.ΔH>0 ΔS>0
D.ΔH<0 ΔS<0

A.ΔH<0 ΔS>0
B.ΔH>0 ΔS<0
C.ΔH>0 ΔS>0
D.ΔH<0 ΔS<0
答案:
A 根据图像可知,在压强不变时,升高温度,C的含量降低,说明平衡逆向移动,逆反应方向是吸热反应,正反应是放热反应,ΔH<0;在温度不变时,增大压强,C的含量降低,说明增大压强,平衡逆向移动,逆反应方向是气体体积减小的方向,则正反应是气体体积增大的反应,ΔS>0。
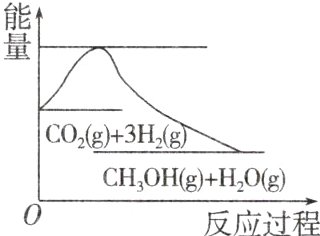
9.实现“节能减排”和“低碳经济”的一个重要课题就是如何将CO₂转化为可利用的资源。目前工业上有一种方法是用CO₂来生产燃料甲醇。一定条件下发生反应:CO₂(g)+3H₂(g)⇌CH₃OH(g)+H₂O(g),如图表示该反应过程中能量(单位为kJ·mol⁻¹)的变化。关于该反应的下列说法中,正确的是 ( )
A.ΔH>0,ΔS>0
B.ΔH>0,ΔS<0
C.ΔH<0,ΔS<0
D.ΔH<0,ΔS>0

A.ΔH>0,ΔS>0
B.ΔH>0,ΔS<0
C.ΔH<0,ΔS<0
D.ΔH<0,ΔS>0
答案:
C 根据反应过程中能量变化的情况可知反应物的总能量高于生成物的总能量,反应放热,ΔH<0;该反应发生后气体的物质的量减小,ΔS<0。
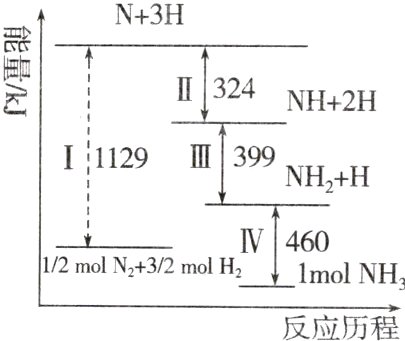
10.N₂(g)与H₂(g)在一定条件下经历如下过程生成NH₃(g),下列说法正确的是 ( )
A.Ⅰ中破坏了离子键
B.Ⅱ、Ⅲ、Ⅳ均为放热过程
C.Ⅳ中表示NH₂与H₂生成NH₃
D.N₂(g)+3H₂(g)2NH₃(g)是吸热反应

A.Ⅰ中破坏了离子键
B.Ⅱ、Ⅲ、Ⅳ均为放热过程
C.Ⅳ中表示NH₂与H₂生成NH₃
D.N₂(g)+3H₂(g)2NH₃(g)是吸热反应
答案:
B Ⅰ中,N₂转化为N,H₂转化为H,都是破坏了分子内原子间的共价键,A不正确;Ⅱ、Ⅲ、Ⅳ三个过程中,生成物的总能量都比反应物的总能量低,所以均为放热过程,B正确;从图中可以看出,Ⅳ中表示NH₂与H反应生成NH₃,C不正确;对于反应N₂(g) + 3H₂(g)⇌2NH₃(g),生成物的总能量低于反应物的总能量,所以是放热反应,D不正确。
查看更多完整答案,请扫码查看


