2025年5年高考3年模拟高中化学全一册人教B版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年5年高考3年模拟高中化学全一册人教B版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第65页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
- 第189页
- 第190页
- 第191页
- 第192页
- 第193页
- 第194页
- 第195页
- 第196页
- 第197页
- 第198页
- 第199页
- 第200页
- 第201页
- 第202页
- 第203页
- 第204页
- 第205页
- 第206页
- 第207页
- 第208页
- 第209页
- 第210页
- 第211页
- 第212页
- 第213页
- 第214页
- 第215页
- 第216页
- 第217页
- 第218页
- 第219页
- 第220页
- 第221页
- 第222页
- 第223页
- 第224页
- 第225页
- 第226页
- 第227页
- 第228页
- 第229页
- 第230页
- 第231页
- 第232页
- 第233页
- 第234页
- 第235页
- 第236页
- 第237页
- 第238页
- 第239页
- 第240页
- 第241页
- 第242页
- 第243页
- 第244页
- 第245页
- 第246页
- 第247页
- 第248页
- 第249页
- 第250页
- 第251页
- 第252页
- 第253页
- 第254页
- 第255页
- 第256页
- 第257页
- 第258页
- 第259页
- 第260页
- 第261页
- 第262页
- 第263页
- 第264页
- 第265页
- 第266页
- 第267页
- 第268页
- 第269页
33.(2024安徽,14,3分)研究人员制备了一种具有锂离子通道的导电氧化物($Li_{x}La_{y}TiO_{3}$),其立方晶胞和导电时$Li^{+}$迁移过程如下图所示。已知该氧化物中Ti为 + 4价,La为 + 3价。下列说法错误的是 ( )

.Ti

A.导电时,Ti和La的价态不变
B.若$x = \frac{1}{3}$,$Li^{+}$与空位的数目相等
C.与体心最邻近的O原子数为12
D.导电时,空位移动方向与电流方向相反

.Ti

A.导电时,Ti和La的价态不变
B.若$x = \frac{1}{3}$,$Li^{+}$与空位的数目相等
C.与体心最邻近的O原子数为12
D.导电时,空位移动方向与电流方向相反
答案:
A项,导电时,Li⁺和空位发生迁移,Ti和La的价态不变,正确;B项,根据均摊法,1个LiₓLaᵧTiO₃晶胞中含Ti原子的个数为8×$\frac{1}{8}$=1,含O原子的个数为12×$\frac{1}{4}$=3,含La或Li或空位的个数为1,则1个晶胞中含1个LiₓLaᵧTiO₃,根据化合物中各元素正、负化合价的代数和为0,x + 3y + 4 = 6,x=$\frac{1}{3}$时,y=$\frac{5}{9}$,则空位数为1-$\frac{1}{3}$-$\frac{5}{9}$=$\frac{1}{9}$,Li⁺与空位的数目不相等,错误;C项,由LiₓLaᵧTiO₃的晶胞图可知,12条棱心的氧原子离体心位置最近且距离相等,即与体心最邻近的O原子数为12,正确;D项,导电时,Li⁺的迁移方向与空位移动方向相反,阳离子(Li⁺)移动方向为电流方向,即空位移动方向与电流方向相反,正确。
34.(2023湖北,11,3分)物质结构决定物质性质。下列性质差异与结构因素匹配错误的是 ( )


答案:
正戊烷与新戊烷均为分子晶体,互为同分异构体,新戊烷有支链,分子间作用力:正戊烷>新戊烷,沸点:正戊烷>新戊烷,A正确;AlF₃为离子晶体,AlCl₃为分子晶体,熔点:AlF₃>AlCl₃,B正确;羧基中羟基极性越大越易电离出H⁺,酸性越强,C正确;Na₂CO₃与NaHCO₃中阴离子电荷不同,离子键大小不同,熔点不同,与溶解度无关,D错误。
归纳总结:羟基所连的基团吸引电子能力越强,羟基的极性越强。
归纳总结:羟基所连的基团吸引电子能力越强,羟基的极性越强。
35.(2023北京,1,3分)中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是 ( )
A.三种物质中均有碳原子间的$\sigma$键
B.三种物质中的碳原子都是$sp^{3}$杂化
C.三种物质的晶体类型相同
D.三种物质均能导电

下列关于金刚石、石墨、石墨炔的说法正确的是 ( )
A.三种物质中均有碳原子间的$\sigma$键
B.三种物质中的碳原子都是$sp^{3}$杂化
C.三种物质的晶体类型相同
D.三种物质均能导电
答案:
金刚石、石墨和石墨炔中均有碳碳原子间的σ键,A正确;石墨中的碳原子采用sp²杂化,石墨炔中的碳原子采用sp²和sp杂化,B错误;金刚石为共价晶体,石墨为混合型晶体,C错误;金刚石不能导电,D错误。
36.(2023辽宁,14,3分)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是 ( )
ooCl或Br

A.图1晶体密度为$\frac{72.5}{N_{A}\times a^{3}\times10^{-30}}$ $g\cdot cm^{-3}$
B.图1中O原子的配位数为6
C.图2表示的化学式为$LiMg_{2}OCl_{x}Br_{1 - x}$
D.$Mg^{2 + }$取代产生的空位有利于$Li^{+}$传导
ooCl或Br

A.图1晶体密度为$\frac{72.5}{N_{A}\times a^{3}\times10^{-30}}$ $g\cdot cm^{-3}$
B.图1中O原子的配位数为6
C.图2表示的化学式为$LiMg_{2}OCl_{x}Br_{1 - x}$
D.$Mg^{2 + }$取代产生的空位有利于$Li^{+}$传导
答案:
A项,利用均摊法可得图1晶胞中有1个Cl,1个O,3个Li,则晶体密度为$\frac{35.5 + 16 + 7×3}{N_{A}(a×10^{-10})^{3}}$g·cm⁻³=$\frac{72.5}{N_{A}×a^{3}×10^{-30}}$g·cm⁻³,正确;B项,图1中与氧原子距离最近($\frac{a}{2}$pm)的Li有6个,则O原子的配位数为6,正确;C项,利用均摊法,图2晶胞中含有1个Li,Mg或空位共2个,1个O,Cl或Br共1个,根据化合物中各元素正负化合价代数和为0,得Mg有1个,化学式为LiMgOClₓBr₁₋ₓ,错误;D项,Mg²⁺取代Li⁺后,产生的空位可供Li⁺移动传导电荷,增强导电性,正确。
37.(2023重庆,9,3分)配合物$[MA_{2}L_{2}]$的分子结构以及分子在晶胞中的位置如图所示,下列说法错误的是 ( )
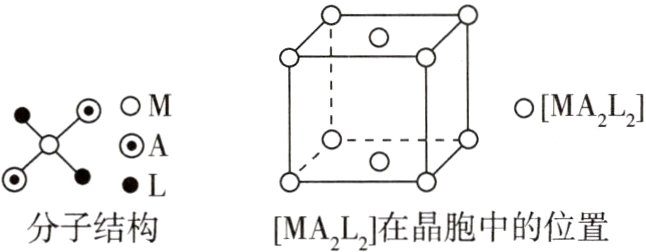
A.中心原子的配位数是4
B.晶胞中配合物分子的数目为2
C.晶体中相邻分子间存在范德华力
D.该晶体属于混合型晶体

A.中心原子的配位数是4
B.晶胞中配合物分子的数目为2
C.晶体中相邻分子间存在范德华力
D.该晶体属于混合型晶体
答案:
由题图中分子结构可知M周围有4条共价键,则其配位数为4。根据均摊法,晶胞中配合物的分子数目为8×$\frac{1}{8}$+2×$\frac{1}{2}$=2。配合物[MA₂L₂]由分子构成,则其晶体是分子晶体,相邻分子间存在范德华力。综上可知选D。
查看更多完整答案,请扫码查看


