2026年新高考5年真题化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年新高考5年真题化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第86页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
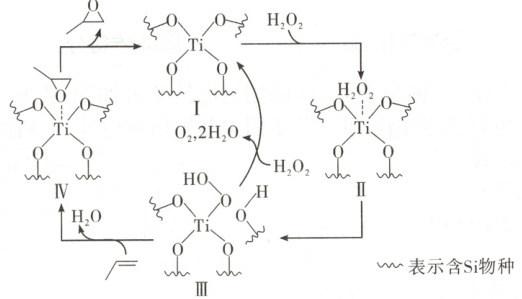
5. [2025·湖南卷,14T,3分]环氧化合物是重要的有机合成中间体。以钛掺杂沸石为催化剂,由丙烯(${/}$)为原料生产环氧丙烷(${\triangle}$)的反应机理如图所示。下列说法正确的是(
A.过程中Ⅱ是催化剂
B.过程中有极性键和非极性键的断裂和形成
C.过程中${Ti}$元素的化合价发生了变化
D.丙烯与双氧水反应生成环氧丙烷的原子利用率为$100\%$
B
)
A.过程中Ⅱ是催化剂
B.过程中有极性键和非极性键的断裂和形成
C.过程中${Ti}$元素的化合价发生了变化
D.丙烯与双氧水反应生成环氧丙烷的原子利用率为$100\%$
答案:
5. 参考答案 B
命题意图 本题以生产环氧丙烷的反应机理为情境,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路 根据反应机理可知,过程中I先消耗后生成,是催化剂,III先生成后消耗,是中间产物,A项错误。过程中存在${O-O}$、${C-C}$非极性键的断裂,以及${O-O}$非极性键的形成,还存在${O-H}$极性键、${Ti-O}$键的断裂,以及${O-C}$极性键的形成,B项正确。过程中${Ti-O}$键的个数始终是$4$,与${H_{2}O_{2}}$、${AO}$形成的配位键不会改变${Ti}$的化合价,故${Ti}$元素的化合价不变,C项错误。根据反应机理可知,丙烯与双氧水反应生成环氧丙烷和水,即生成环氧丙烷的原子利用率小于$100\%$,D项错误。
命题意图 本题以生产环氧丙烷的反应机理为情境,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路 根据反应机理可知,过程中I先消耗后生成,是催化剂,III先生成后消耗,是中间产物,A项错误。过程中存在${O-O}$、${C-C}$非极性键的断裂,以及${O-O}$非极性键的形成,还存在${O-H}$极性键、${Ti-O}$键的断裂,以及${O-C}$极性键的形成,B项正确。过程中${Ti-O}$键的个数始终是$4$,与${H_{2}O_{2}}$、${AO}$形成的配位键不会改变${Ti}$的化合价,故${Ti}$元素的化合价不变,C项错误。根据反应机理可知,丙烯与双氧水反应生成环氧丙烷和水,即生成环氧丙烷的原子利用率小于$100\%$,D项错误。
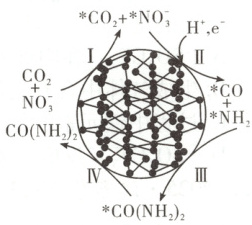
6. [2025·江苏卷,10T,3分]${CO_{2}}$与${NO^{-}_{3}}$通过电催化反应生成${CO(NH_{2})_{2}}$,可能的反应机理如图所示(图中吸附在催化剂表面的物种用“$*$”标注)。
下列说法正确的是(
A.过程Ⅱ和过程Ⅲ都有极性共价键形成
B.过程Ⅱ中${NO^{-}_{3}}$发生了氧化反应
C.电催化${CO_{2}}$与${NO^{-}_{3}}$生成${CO(NH_{2})_{2}}$的反应方程式:${CO_{2} + 2NO^{-}_{3} + 18H^{+}\xlongequal[催化剂]{通电}CO(NH_{2})_{2} + 7H_{2}O}$
D.常温常压、无催化剂条件下,${CO_{2}}$与${NH_{3}· H_{2}O}$反应可生产${CO(NH_{2})_{2}}$
下列说法正确的是(
A
)
A.过程Ⅱ和过程Ⅲ都有极性共价键形成
B.过程Ⅱ中${NO^{-}_{3}}$发生了氧化反应
C.电催化${CO_{2}}$与${NO^{-}_{3}}$生成${CO(NH_{2})_{2}}$的反应方程式:${CO_{2} + 2NO^{-}_{3} + 18H^{+}\xlongequal[催化剂]{通电}CO(NH_{2})_{2} + 7H_{2}O}$
D.常温常压、无催化剂条件下,${CO_{2}}$与${NH_{3}· H_{2}O}$反应可生产${CO(NH_{2})_{2}}$
答案:
6. 参考答案 A
命题意图 本题借助电催化反应机理图,分析反应历程中化学键的变化与氧化还原过程,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路 过程II中${CO_{2}}$和${NO}$在酸性条件下被还原为${CO}$和${NH_{4}^{+}}$,生成了${N-H}$极性共价键;过程III中${CO}$与${NH_{2}^{-}}$生成${CO(NH_{2})_{2}}$,生成了${C-N}$极性共价键,A项正确。过程II中NO₃⁻转化为${NH_{2}^{-}}$,发生了得电子的还原反应,氮元素的化合价降低,B项错误。所给反应方程式电荷不守恒,根据反应机理图可知,电催化过程需要外界提供电子,则正确的反应方程式为${CO_{2}} + 2{NO} + 18{H^{+}} + 16{e^{-}}\xlongequal[ 催化剂]{ 通电}{CO(NH_{2})_{2}} + 7{H_{2}O}$,C项错误。常温常压、无催化剂条件下,${CO_{2}}$与${NH_{3}· H_{2}O}$反应生成${(NH_{4})_{2}CO_{3}}$或${NH_{4}HCO_{3}}$,不能得到${CO(NH_{2})_{2}}$,D项错误。
命题意图 本题借助电催化反应机理图,分析反应历程中化学键的变化与氧化还原过程,体现了“证据推理与模型认知”等化学学科核心素养。
解题思路 过程II中${CO_{2}}$和${NO}$在酸性条件下被还原为${CO}$和${NH_{4}^{+}}$,生成了${N-H}$极性共价键;过程III中${CO}$与${NH_{2}^{-}}$生成${CO(NH_{2})_{2}}$,生成了${C-N}$极性共价键,A项正确。过程II中NO₃⁻转化为${NH_{2}^{-}}$,发生了得电子的还原反应,氮元素的化合价降低,B项错误。所给反应方程式电荷不守恒,根据反应机理图可知,电催化过程需要外界提供电子,则正确的反应方程式为${CO_{2}} + 2{NO} + 18{H^{+}} + 16{e^{-}}\xlongequal[ 催化剂]{ 通电}{CO(NH_{2})_{2}} + 7{H_{2}O}$,C项错误。常温常压、无催化剂条件下,${CO_{2}}$与${NH_{3}· H_{2}O}$反应生成${(NH_{4})_{2}CO_{3}}$或${NH_{4}HCO_{3}}$,不能得到${CO(NH_{2})_{2}}$,D项错误。
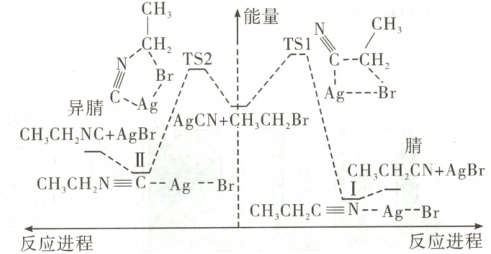
7. [2024·贵州卷,14T,3分]${AgCN}$与${CH_{3}CH_{2}Br}$可发生取代反应,反应过程中${CN^{-}}$的${C}$原子和${N}$原子均可进攻${CH_{3}CH_{2}Br}$,分别生成腈(${CH_{3}CH_{2}CN}$)和异腈(${CH_{3}CH_{2}NC}$)两种产物。通过量子化学计算得到的反应历程及能量变化如图(${TS}$为过渡态,Ⅰ、Ⅱ为后续物)。
由图示信息,下列说法错误的是(
A.从${CH_{3}CH_{2}Br}$生成${CH_{3}CH_{2}CN}$和${CH_{3}CH_{2}NC}$的反应都是放热反应
B.过渡态${TS1}$是由${CN^{-}}$的${C}$原子进攻${CH_{3}CH_{2}Br}$的$\alpha -{C}$而形成的
C.Ⅰ中“${N--Ag}$”之间的作用力比Ⅱ中“${C--Ag}$”之间的作用力弱
D.生成${CH_{3}CH_{2}CN}$放热更多,低温时${CH_{3}CH_{2}CN}$是主要产物

由图示信息,下列说法错误的是(
D
)A.从${CH_{3}CH_{2}Br}$生成${CH_{3}CH_{2}CN}$和${CH_{3}CH_{2}NC}$的反应都是放热反应
B.过渡态${TS1}$是由${CN^{-}}$的${C}$原子进攻${CH_{3}CH_{2}Br}$的$\alpha -{C}$而形成的
C.Ⅰ中“${N--Ag}$”之间的作用力比Ⅱ中“${C--Ag}$”之间的作用力弱
D.生成${CH_{3}CH_{2}CN}$放热更多,低温时${CH_{3}CH_{2}CN}$是主要产物
答案:
7. 参考答案 D
命题意图 本题考查反应历程中的能量变化,意在考查考生的理解分析能力,体现了“证据推理与模型认知”化学学科核心素养。
解题思路 由图可知,${AgCN}$与${CH_{2}=CHBr}$分别生成${CH_{2}=CH_{2}CN}$和${CH_{2}=CH_{2}NC}$的反应均是反应物总能量大于生成物总能量的反应,均为放热反应,A项正确。由图可知,过渡态${TS1}$是由${CN^{-}}$的${C}$原子进攻${CH_{2}=CHBr}$的$\alpha -C$而形成的,B项正确。由图可知,I$\to{CH_{2}=CHCN}$和III$\to{CH_{2}=CHNC}$均为吸热过程,但I$\to{CH_{2}=CHCN}$吸收的热量较少,说明I中“${N - Ag}$”断裂所需能量少,故I中“${N - Ag}$”之间的作用力比III中“${C - Ag}$”之间的作用力弱,C项正确。生成${CH_{2}=CHCN}$的反应和生成${CH_{2}=CHNC}$的反应均为放热反应,低温对二者的生成都有利,但生成${CH_{2}=CHCN}$的活化能比生成${CH_{2}=CHNC}$的活化能大,则低温时${CH_{2}=CHNC}$是主要产物,D项错误。
命题意图 本题考查反应历程中的能量变化,意在考查考生的理解分析能力,体现了“证据推理与模型认知”化学学科核心素养。
解题思路 由图可知,${AgCN}$与${CH_{2}=CHBr}$分别生成${CH_{2}=CH_{2}CN}$和${CH_{2}=CH_{2}NC}$的反应均是反应物总能量大于生成物总能量的反应,均为放热反应,A项正确。由图可知,过渡态${TS1}$是由${CN^{-}}$的${C}$原子进攻${CH_{2}=CHBr}$的$\alpha -C$而形成的,B项正确。由图可知,I$\to{CH_{2}=CHCN}$和III$\to{CH_{2}=CHNC}$均为吸热过程,但I$\to{CH_{2}=CHCN}$吸收的热量较少,说明I中“${N - Ag}$”断裂所需能量少,故I中“${N - Ag}$”之间的作用力比III中“${C - Ag}$”之间的作用力弱,C项正确。生成${CH_{2}=CHCN}$的反应和生成${CH_{2}=CHNC}$的反应均为放热反应,低温对二者的生成都有利,但生成${CH_{2}=CHCN}$的活化能比生成${CH_{2}=CHNC}$的活化能大,则低温时${CH_{2}=CHNC}$是主要产物,D项错误。
查看更多完整答案,请扫码查看


