2026年新高考5年真题化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年新高考5年真题化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第63页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
9. [2024·浙江 1 月卷,2T,3 分]工业上将 $ {Cl_{2}} $ 通入冷的 NaOH 溶液中制得漂白液,下列说法不正确的是(
A.漂白液的有效成分是 NaClO
B.$ {ClO^{-}} $ 水解生成 HClO 使漂白液呈酸性
C.通入 $ {CO_{2}} $ 后的漂白液消毒能力增强
D.NaClO 溶液比 HClO 溶液稳定
B
)A.漂白液的有效成分是 NaClO
B.$ {ClO^{-}} $ 水解生成 HClO 使漂白液呈酸性
C.通入 $ {CO_{2}} $ 后的漂白液消毒能力增强
D.NaClO 溶液比 HClO 溶液稳定
答案:
9. 参考答案 B
命题意图 本题考查漂白液的相关性质,侧重考查考生对基础知识的积累。
解题思路 漂白液的主要成分是 ${NaClO}$ 和 ${NaCl}$,有效成分是 ${NaClO}$,A 项正确。${ClO^{-}}$ 水解生成 ${HClO}$ 和 ${OH^{-}}$,水解方程式为 ${ClO^{-} + H_{2}O \rightleftharpoons HClO + OH^{-}}$,使漂白液呈碱性,B 项错误。通入 ${CO_{2}}$ 后,发生反应 ${NaClO + CO_{2} + H_{2}O = NaHCO_{3} + HClO}$,${HClO}$ 浓度增大,漂白液消毒能力增强,C 项正确。${HClO}$ 不稳定,易分解,次氯酸盐稳定,所以稳定性 ${NaClO > HClO}$,D 项正确。
命题意图 本题考查漂白液的相关性质,侧重考查考生对基础知识的积累。
解题思路 漂白液的主要成分是 ${NaClO}$ 和 ${NaCl}$,有效成分是 ${NaClO}$,A 项正确。${ClO^{-}}$ 水解生成 ${HClO}$ 和 ${OH^{-}}$,水解方程式为 ${ClO^{-} + H_{2}O \rightleftharpoons HClO + OH^{-}}$,使漂白液呈碱性,B 项错误。通入 ${CO_{2}}$ 后,发生反应 ${NaClO + CO_{2} + H_{2}O = NaHCO_{3} + HClO}$,${HClO}$ 浓度增大,漂白液消毒能力增强,C 项正确。${HClO}$ 不稳定,易分解,次氯酸盐稳定,所以稳定性 ${NaClO > HClO}$,D 项正确。
10. [2024·辽宁卷,6T,3 分]$ {H_{2}O_{2}} $ 分解的“碘钟”反应美轮美奂。将一定浓度的三种溶液(①$ {H_{2}O_{2}} $ 溶液;②淀粉、丙二酸和 $ {MnSO_{4}} $ 混合溶液;③$ {KIO_{3}} $、稀硫酸混合溶液)混合,溶液颜色在无色和蓝色之间来回振荡,周期性变色;几分钟后,稳定为蓝色。下列说法错误的是(
A.无色→蓝色:生成 $ {I_{2}} $
B.蓝色→无色:$ {I_{2}} $ 转化为化合态
C.$ {H_{2}O_{2}} $ 起漂白作用
D.淀粉作指示剂
C
)A.无色→蓝色:生成 $ {I_{2}} $
B.蓝色→无色:$ {I_{2}} $ 转化为化合态
C.$ {H_{2}O_{2}} $ 起漂白作用
D.淀粉作指示剂
答案:
10. 参考答案 C
命题意图 本题以 ${H_{2}O_{2}}$ 分解的“碘钟”反应为素材,涉及氧化还原反应、指示剂等知识,意在考查考生的知识迁移能力,体现了“证据推理与模型认知”化学学科核心素养。
解题思路 “碘钟”反应的原理:${KIO_{3}}$ 和 ${H_{2}O_{2}}$ 在酸性条件和 ${Mn^{2+}}$ 催化下生成 ${O_{2}}$ 和 ${I_{2}}$,淀粉遇 ${I_{2}}$ 变蓝,化学方程式为 ${2KIO_{3} + H_{2}SO_{4} + 5H_{2}O_{2} \xlongequal{Mn^{2+}} 5O_{2}↑ + I_{2} + K_{2}SO_{4} + 6H_{2}O}$;${I_{2}}$ 与丙二酸反应,使蓝色的溶液褪色,如此循环进行,几分钟后,溶液稳定为蓝色。无色→蓝色是由于生成了 ${I_{2}}$,淀粉遇 ${I_{2}}$ 变蓝,A 项正确。蓝色→无色是由于 ${I_{2}}$ 被氧化成了 ${KIO_{3}}$,B 项正确。在该过程中,${H_{2}O_{2}}$ 没有体现漂白性,C 项错误。在生成 ${I_{2}}$ 时,淀粉变蓝,在 ${I_{2}}$ 消耗时,溶液呈无色,故淀粉为指示剂,D 项正确。
命题意图 本题以 ${H_{2}O_{2}}$ 分解的“碘钟”反应为素材,涉及氧化还原反应、指示剂等知识,意在考查考生的知识迁移能力,体现了“证据推理与模型认知”化学学科核心素养。
解题思路 “碘钟”反应的原理:${KIO_{3}}$ 和 ${H_{2}O_{2}}$ 在酸性条件和 ${Mn^{2+}}$ 催化下生成 ${O_{2}}$ 和 ${I_{2}}$,淀粉遇 ${I_{2}}$ 变蓝,化学方程式为 ${2KIO_{3} + H_{2}SO_{4} + 5H_{2}O_{2} \xlongequal{Mn^{2+}} 5O_{2}↑ + I_{2} + K_{2}SO_{4} + 6H_{2}O}$;${I_{2}}$ 与丙二酸反应,使蓝色的溶液褪色,如此循环进行,几分钟后,溶液稳定为蓝色。无色→蓝色是由于生成了 ${I_{2}}$,淀粉遇 ${I_{2}}$ 变蓝,A 项正确。蓝色→无色是由于 ${I_{2}}$ 被氧化成了 ${KIO_{3}}$,B 项正确。在该过程中,${H_{2}O_{2}}$ 没有体现漂白性,C 项错误。在生成 ${I_{2}}$ 时,淀粉变蓝,在 ${I_{2}}$ 消耗时,溶液呈无色,故淀粉为指示剂,D 项正确。
11. [2024·北京卷,7T,3 分]硫酸是重要化工原料,工业生产制取硫酸的原理示意图如图。
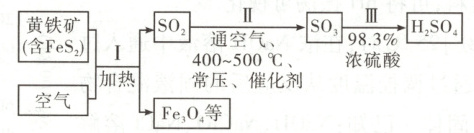
下列说法不正确的是(
A.Ⅰ的化学方程式:$ {3FeS_{2} + 8O_{2}\xlongequal{\Delta}Fe_{3}O_{4} + 6SO_{2}} $
B.Ⅱ中的反应条件都是为了提高 $ {SO_{2}} $ 平衡转化率
C.将黄铁矿换成硫黄可以减少废渣的产生
D.生产过程中产生的尾气可用碱液吸收

下列说法不正确的是(
B
)A.Ⅰ的化学方程式:$ {3FeS_{2} + 8O_{2}\xlongequal{\Delta}Fe_{3}O_{4} + 6SO_{2}} $
B.Ⅱ中的反应条件都是为了提高 $ {SO_{2}} $ 平衡转化率
C.将黄铁矿换成硫黄可以减少废渣的产生
D.生产过程中产生的尾气可用碱液吸收
答案:
11. 参考答案 B
命题意图 本题以制取硫酸的工业流程为素材,意在考查考生的分析判断能力,体现了“宏观辨识与微观探析”“证据推理与模型认知”化学学科核心素养。
解题思路 根据原理示意图可知,黄铁矿(含 ${FeS_{2}}$)在空气中加热生成 ${SO_{2}}$、${Fe_{3}O_{4}}$,A 项正确。反应Ⅱ条件要兼顾平衡转化率和反应速率,还要考虑生产成本,如Ⅱ中“常压”主要是从生产成本方面考虑,“通空气”可使平衡正向移动,提高 ${SO_{2}}$ 平衡转化率,“$400\sim 500^{\circ} C$、催化剂”是为了提高反应速率,B 项错误。将黄铁矿换成硫黄,则发生的反应为 ${S + O_{2} \xlongequal{ 点燃} SO_{2}}$,不再产生 ${Fe_{3}O_{4}}$,即可以减少废渣产生,C 项正确。硫酸工业产生的尾气为 ${SO_{2}}$、${SO_{3}}$,两者均为酸性气体,均可以用碱液吸收,D 项正确。
命题意图 本题以制取硫酸的工业流程为素材,意在考查考生的分析判断能力,体现了“宏观辨识与微观探析”“证据推理与模型认知”化学学科核心素养。
解题思路 根据原理示意图可知,黄铁矿(含 ${FeS_{2}}$)在空气中加热生成 ${SO_{2}}$、${Fe_{3}O_{4}}$,A 项正确。反应Ⅱ条件要兼顾平衡转化率和反应速率,还要考虑生产成本,如Ⅱ中“常压”主要是从生产成本方面考虑,“通空气”可使平衡正向移动,提高 ${SO_{2}}$ 平衡转化率,“$400\sim 500^{\circ} C$、催化剂”是为了提高反应速率,B 项错误。将黄铁矿换成硫黄,则发生的反应为 ${S + O_{2} \xlongequal{ 点燃} SO_{2}}$,不再产生 ${Fe_{3}O_{4}}$,即可以减少废渣产生,C 项正确。硫酸工业产生的尾气为 ${SO_{2}}$、${SO_{3}}$,两者均为酸性气体,均可以用碱液吸收,D 项正确。
12. [2023·辽宁卷,3T,3 分]下列有关物质的工业制备反应错误的是(
A.合成氨:$ {N_{2} + 3H_{2}\underset{催化剂}{\overset{高温高压}{⇌}}2NH_{3}} $
B.制 HCl:$ {H_{2} + Cl_{2}\xlongequal{点燃}2HCl} $
C.制粗硅:$ {SiO_{2} + 2C\xlongequal{高温}Si + 2CO\uparrow} $
D.冶炼镁:$ {2MgO\xlongequal{通电}2Mg + O_{2}\uparrow} $
D
)A.合成氨:$ {N_{2} + 3H_{2}\underset{催化剂}{\overset{高温高压}{⇌}}2NH_{3}} $
B.制 HCl:$ {H_{2} + Cl_{2}\xlongequal{点燃}2HCl} $
C.制粗硅:$ {SiO_{2} + 2C\xlongequal{高温}Si + 2CO\uparrow} $
D.冶炼镁:$ {2MgO\xlongequal{通电}2Mg + O_{2}\uparrow} $
答案:
12. 参考答案 D
命题意图 本题以物质的制备为载体,考查元素及其化合物的性质,体现了“宏观辨识与微观探析”化学学科核心素养。
解题思路 合成氨工业为氮气和氢气在高温高压、催化剂条件下反应生成氨气,A 项正确。工业制备 ${HCl}$ 的反应为氢气和氯气在点燃时反应生成 ${HCl}$,B 项正确。工业制备粗硅的反应为石英和焦炭在高温条件下反应生成单质硅和 ${CO}$,C 项正确。工业冶炼镁的反应为电解熔融氯化镁生成镁和氯气,${MgO}$ 的熔点很高,一般不用于冶炼镁,D 项错误。
命题意图 本题以物质的制备为载体,考查元素及其化合物的性质,体现了“宏观辨识与微观探析”化学学科核心素养。
解题思路 合成氨工业为氮气和氢气在高温高压、催化剂条件下反应生成氨气,A 项正确。工业制备 ${HCl}$ 的反应为氢气和氯气在点燃时反应生成 ${HCl}$,B 项正确。工业制备粗硅的反应为石英和焦炭在高温条件下反应生成单质硅和 ${CO}$,C 项正确。工业冶炼镁的反应为电解熔融氯化镁生成镁和氯气,${MgO}$ 的熔点很高,一般不用于冶炼镁,D 项错误。
13. [2023·北京卷,7T,3 分]蔗糖与浓硫酸发生作用的过程如图所示。
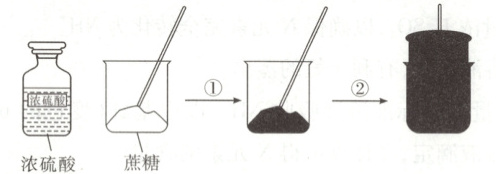
下列关于该过程的分析不正确的是(
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂

下列关于该过程的分析不正确的是(
C
)A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂
答案:
13. 参考答案 C
命题意图 本题考查浓硫酸与蔗糖的实验,掌握浓硫酸的性质是解题关键,考查考生的理解分析能力,体现了“科学探究与创新意识”化学学科核心素养。
解题思路 浓硫酸具有脱水性,能将有机物中的 H 原子和 O 原子按数目比为 $2:1$ 的比例脱去,得到碳单质,向蔗糖中加入浓硫酸,白色固体变黑,体现了浓硫酸的脱水性,A 项正确。蔗糖脱水放出大量热,得到的黑色固体为碳单质,C 可与浓硫酸发生反应 ${C + 2H_{2}SO_{4}(浓) \xlongequal{\Delta} CO_{2}↑ + 2SO_{2}↑ + 2H_{2}O}$,产生大量的气体,使固体体积膨胀,B 项正确。产生的能使品红溶液褪色的气体为 ${SO_{2}}$,S 元素化合价降低,体现浓硫酸的强氧化性,C 项错误。该过程中蔗糖发生了化学变化,存在化学键的断裂,D 项正确。
命题意图 本题考查浓硫酸与蔗糖的实验,掌握浓硫酸的性质是解题关键,考查考生的理解分析能力,体现了“科学探究与创新意识”化学学科核心素养。
解题思路 浓硫酸具有脱水性,能将有机物中的 H 原子和 O 原子按数目比为 $2:1$ 的比例脱去,得到碳单质,向蔗糖中加入浓硫酸,白色固体变黑,体现了浓硫酸的脱水性,A 项正确。蔗糖脱水放出大量热,得到的黑色固体为碳单质,C 可与浓硫酸发生反应 ${C + 2H_{2}SO_{4}(浓) \xlongequal{\Delta} CO_{2}↑ + 2SO_{2}↑ + 2H_{2}O}$,产生大量的气体,使固体体积膨胀,B 项正确。产生的能使品红溶液褪色的气体为 ${SO_{2}}$,S 元素化合价降低,体现浓硫酸的强氧化性,C 项错误。该过程中蔗糖发生了化学变化,存在化学键的断裂,D 项正确。
14. [2023·江苏卷,8T,3 分]氮及其化合物的转化具有重要应用。下列说法不正确的是(
A.实验室探究稀硝酸与铜反应的气态产物:$ {HNO_{3}(稀)\xrightarrow{Cu}NO\xrightarrow{O_{2}}NO_{2}} $
B.工业制硝酸过程中的物质转化:${:N_{2}\xrightarrow[放电或高温]{O_{2}}NO\xrightarrow[]{H_{2}O}HNO_{3}}$
C.汽车尾气催化转化器中发生的主要反应:$ {2NO + 2CO\xlongequal{催化剂}N_{2} + 2CO_{2}} $
D.实验室制备少量 $ {NH_{3}} $ 的原理:$ {2NH_{4}Cl + Ca(OH)_{2}\xlongequal{\Delta}CaCl_{2} + 2NH_{3}\uparrow + 2H_{2}O} $
B
)A.实验室探究稀硝酸与铜反应的气态产物:$ {HNO_{3}(稀)\xrightarrow{Cu}NO\xrightarrow{O_{2}}NO_{2}} $
B.工业制硝酸过程中的物质转化:${:N_{2}\xrightarrow[放电或高温]{O_{2}}NO\xrightarrow[]{H_{2}O}HNO_{3}}$
C.汽车尾气催化转化器中发生的主要反应:$ {2NO + 2CO\xlongequal{催化剂}N_{2} + 2CO_{2}} $
D.实验室制备少量 $ {NH_{3}} $ 的原理:$ {2NH_{4}Cl + Ca(OH)_{2}\xlongequal{\Delta}CaCl_{2} + 2NH_{3}\uparrow + 2H_{2}O} $
答案:
14. 参考答案 B
命题意图 本题以氮及其化合物的转化为载体,涉及物质的转化、方程式的书写等知识,体现了“宏观辨识与微观探析”化学学科核心素养。
解题思路 稀硝酸与 Cu 反应生成 NO,NO 遇 ${O_{2}}$ 生成 ${NO_{2}}$,A 项正确。NO 不与水反应,B 项错误。在汽车尾气催化转化器中大气污染物 NO 和 CO 转化为 ${N_{2}}$ 和 ${CO_{2}}$,C 项正确。实验室可用铵盐(${NH_{4}Cl}$)和碱 ${[Ca(OH)_{2}]}$ 共热制取氨气,D 项正确。
命题意图 本题以氮及其化合物的转化为载体,涉及物质的转化、方程式的书写等知识,体现了“宏观辨识与微观探析”化学学科核心素养。
解题思路 稀硝酸与 Cu 反应生成 NO,NO 遇 ${O_{2}}$ 生成 ${NO_{2}}$,A 项正确。NO 不与水反应,B 项错误。在汽车尾气催化转化器中大气污染物 NO 和 CO 转化为 ${N_{2}}$ 和 ${CO_{2}}$,C 项正确。实验室可用铵盐(${NH_{4}Cl}$)和碱 ${[Ca(OH)_{2}]}$ 共热制取氨气,D 项正确。
查看更多完整答案,请扫码查看


