2026年新高考5年真题化学河北专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年新高考5年真题化学河北专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第25页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
1. 定窑是宋代五大名窑之一,其生产的白瓷闻名于世。下列说法正确的是(
A.传统陶瓷是典型的绝缘材料
B.陶瓷主要成分为SiO₂和MgO
C.陶瓷烧制的过程为物理变化
D.白瓷的白色是因铁含量较高
A
)A.传统陶瓷是典型的绝缘材料
B.陶瓷主要成分为SiO₂和MgO
C.陶瓷烧制的过程为物理变化
D.白瓷的白色是因铁含量较高
答案:
1.参考答案A
命题意图本题以白瓷为载体,考查化学基本常识,意在考查考生对基础知识的掌握以及其在生活中的应用,体现了“科学态度与社会责任”化学学科核心素养。
解题思路传统陶瓷是良好的绝缘体,A项正确。陶瓷主要成分为硅酸盐,B项错误。陶瓷以黏土为主要原料,经高温烧结而成,烧制过程有新物质生成,发生了化学变化,C项错误。由于${Fe^{2+}}$、${Fe^{3+}}$和铁的氧化物均有颜色,陶瓷中铁含量越高时瓷器颜色越深,D项错误。
命题意图本题以白瓷为载体,考查化学基本常识,意在考查考生对基础知识的掌握以及其在生活中的应用,体现了“科学态度与社会责任”化学学科核心素养。
解题思路传统陶瓷是良好的绝缘体,A项正确。陶瓷主要成分为硅酸盐,B项错误。陶瓷以黏土为主要原料,经高温烧结而成,烧制过程有新物质生成,发生了化学变化,C项错误。由于${Fe^{2+}}$、${Fe^{3+}}$和铁的氧化物均有颜色,陶瓷中铁含量越高时瓷器颜色越深,D项错误。
2. 茯苓新酸DM是从茯苓中提取的一种天然产物,具有一定的生理活性,其结构简式如图。关于该化合物,下列说法错误的是(
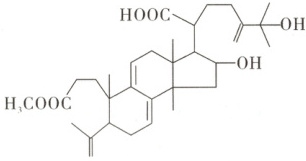
A.可使酸性KMnO₄溶液褪色
B.可发生取代反应和加成反应
C.可与金属钠反应放出H₂
D.分子中含有3种官能团
D
)
A.可使酸性KMnO₄溶液褪色
B.可发生取代反应和加成反应
C.可与金属钠反应放出H₂
D.分子中含有3种官能团
答案:
2.参考答案D
命题意图本题以茯苓新酸为载体,考查考生有机化学相关知识,涉及官能团性质及种类判断,侧重于考查考生的综合分析及运用能力,体现了“宏观辨识与微观探析”化学学科核心素养。
解题思路该分子中含有碳碳双键、羟基,能与酸性高锰酸钾溶液发生氧化反应而使溶液褪色,A项正确。分子中含有羧基和羟基能发生酯化反应(属于取代反应),含有酯基,能发生水解反应(属于取代反应),含有碳碳双键,能发生加成反应,B项正确。分子中含有羟基、羧基,能和金属钠发生反应放出${H_{2}}$,C项正确。分子中含有酯基、羟基、羧基、碳碳双键4种官能团,D项错误。
命题意图本题以茯苓新酸为载体,考查考生有机化学相关知识,涉及官能团性质及种类判断,侧重于考查考生的综合分析及运用能力,体现了“宏观辨识与微观探析”化学学科核心素养。
解题思路该分子中含有碳碳双键、羟基,能与酸性高锰酸钾溶液发生氧化反应而使溶液褪色,A项正确。分子中含有羧基和羟基能发生酯化反应(属于取代反应),含有酯基,能发生水解反应(属于取代反应),含有碳碳双键,能发生加成反应,B项正确。分子中含有羟基、羧基,能和金属钠发生反应放出${H_{2}}$,C项正确。分子中含有酯基、羟基、羧基、碳碳双键4种官能团,D项错误。
3. 化学是材料科学的基础。下列说法错误的是(
A.制造5G芯片的氮化铝晶圆属于无机非金属材料
B.制造阻燃或防火线缆的橡胶不能由加聚反应合成
C.制造特种防护服的芳纶纤维属于有机高分子材料
D.可降解聚乳酸塑料的推广应用可减少“白色污染”
B
)A.制造5G芯片的氮化铝晶圆属于无机非金属材料
B.制造阻燃或防火线缆的橡胶不能由加聚反应合成
C.制造特种防护服的芳纶纤维属于有机高分子材料
D.可降解聚乳酸塑料的推广应用可减少“白色污染”
答案:
3.参考答案B
命题意图本题考查化学与生活,以生活中常见的材料为载体,涉及材料种类的判断、橡胶的合成等知识,侧重于考查考生将化学与生活相结合的能力,体现了“科学态度与社会责任”化学学科核心素养。
解题思路氮化铝是一种新型陶瓷材料,属于无机非金属材料,A项正确。橡胶可以由异戊二烯为单体通过加聚反应合成,B项错误。芳纶为合成纤维,属于有机高分子材料,C项正确。可降解聚乳酸塑料的推广应用,可以减少难降解塑料的使用,从而减少“白色污染”,D项正确。
命题意图本题考查化学与生活,以生活中常见的材料为载体,涉及材料种类的判断、橡胶的合成等知识,侧重于考查考生将化学与生活相结合的能力,体现了“科学态度与社会责任”化学学科核心素养。
解题思路氮化铝是一种新型陶瓷材料,属于无机非金属材料,A项正确。橡胶可以由异戊二烯为单体通过加聚反应合成,B项错误。芳纶为合成纤维,属于有机高分子材料,C项正确。可降解聚乳酸塑料的推广应用,可以减少难降解塑料的使用,从而减少“白色污染”,D项正确。
4. $N_{A}$是阿伏加德罗常数的值。下列说法正确的是(
A.3.9g Na₂O₂与足量水反应,转移电子个数为0.1$N_{A}$
B.1.2g Mg在空气中燃烧生成MgO和Mg₃N₂,转移电子个数为0.1$N_{A}$
C.2.7g Al与足量NaOH溶液反应,生成H₂的个数为0.1$N_{A}$
D.6.0g SiO₂与足量NaOH溶液反应,所得溶液中SiO₃²⁻的个数为0.1$N_{A}$
B
)A.3.9g Na₂O₂与足量水反应,转移电子个数为0.1$N_{A}$
B.1.2g Mg在空气中燃烧生成MgO和Mg₃N₂,转移电子个数为0.1$N_{A}$
C.2.7g Al与足量NaOH溶液反应,生成H₂的个数为0.1$N_{A}$
D.6.0g SiO₂与足量NaOH溶液反应,所得溶液中SiO₃²⁻的个数为0.1$N_{A}$
答案:
4.参考答案B
命题意图本题以阿伏加德罗常数为载体,考查氧化还原反应中电子转移的数目以及盐类水解等知识,体现了“宏观辨识与微观探析”化学学科核心素养。
解题思路${2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2} \uparrow}$中,$1\ mol\ {Na_{2}O_{2}}$参与反应转移$1\ mol\ {e^{-}}$,则$3.9\ g(0.05\ mol){Na_{2}O_{2}}$参与反应,转移电子个数为$0.05N_{ A}$,A项错误;$1.2\ g\ {Mg}$为$0.05\ mol$,${MgO}$、${Mg_{3}N_{2}}$中${Mg}$元素均是$+2$价,故转移电子个数为$0.1N_{ A}$,B项正确。$2.7\ g\ {Al}$为$0.1\ mol$,与足量${NaOH}$溶液发生的反应为${2Al + 2NaOH + 2H_{2}O = 2NaAlO_{2} + 3H_{2} \uparrow}$,生成${H_{2}}$的个数为$0.15N_{ A}$,C项错误。$6.0\ g\ {SiO_{2}}$为$0.1\ mol$,与足量${NaOH}$反应得到$0.1\ mol\ {Na_{2}SiO_{3}}$,${SiO^{2-}_{3}}$因水解个数少于$0.1N_{ A}$,D项错误。
命题意图本题以阿伏加德罗常数为载体,考查氧化还原反应中电子转移的数目以及盐类水解等知识,体现了“宏观辨识与微观探析”化学学科核心素养。
解题思路${2Na_{2}O_{2} + 2H_{2}O = 4NaOH + O_{2} \uparrow}$中,$1\ mol\ {Na_{2}O_{2}}$参与反应转移$1\ mol\ {e^{-}}$,则$3.9\ g(0.05\ mol){Na_{2}O_{2}}$参与反应,转移电子个数为$0.05N_{ A}$,A项错误;$1.2\ g\ {Mg}$为$0.05\ mol$,${MgO}$、${Mg_{3}N_{2}}$中${Mg}$元素均是$+2$价,故转移电子个数为$0.1N_{ A}$,B项正确。$2.7\ g\ {Al}$为$0.1\ mol$,与足量${NaOH}$溶液发生的反应为${2Al + 2NaOH + 2H_{2}O = 2NaAlO_{2} + 3H_{2} \uparrow}$,生成${H_{2}}$的个数为$0.15N_{ A}$,C项错误。$6.0\ g\ {SiO_{2}}$为$0.1\ mol$,与足量${NaOH}$反应得到$0.1\ mol\ {Na_{2}SiO_{3}}$,${SiO^{2-}_{3}}$因水解个数少于$0.1N_{ A}$,D项错误。
5. 下列图示装置不能达到实验目的的是(


D
)

答案:
5.参考答案D
命题意图本题考查考生对基础实验操作的掌握,涉及萃取、气体除杂、物质制备等实验操作,侧重考查考生对物质性质的了解及实验中的运用能力,体现了“科学探究与创新意识”化学学科核心素养。
解题思路${Br_{2}}$在${CCl_{4}}$中的溶解度比在${H_{2}O}$中的大,且${CCl_{4}}$不溶于水,故可用${CCl_{4}}$萃取溴水中的${Br_{2}}$,A项不符合题意。由于同离子效应,${Cl_{2}}$在饱和${NaCl}$溶液中的溶解度很小,${HCl}$极易溶于水,浓硫酸可用于干燥酸性气体${Cl_{2}}$,B项不符合题意。若铁发生吸氧腐蚀,则试管中压强减小,烧杯中的红墨水会沿导管上升,C项不符合题意。收集${NH_{3}}$的导管应插入倒立的试管底部,且收集${NH_{3}}$的装置中没有排气口,会造成试管因压强过大而破裂,不能达到实验目的,D项符合题意。
命题意图本题考查考生对基础实验操作的掌握,涉及萃取、气体除杂、物质制备等实验操作,侧重考查考生对物质性质的了解及实验中的运用能力,体现了“科学探究与创新意识”化学学科核心素养。
解题思路${Br_{2}}$在${CCl_{4}}$中的溶解度比在${H_{2}O}$中的大,且${CCl_{4}}$不溶于水,故可用${CCl_{4}}$萃取溴水中的${Br_{2}}$,A项不符合题意。由于同离子效应,${Cl_{2}}$在饱和${NaCl}$溶液中的溶解度很小,${HCl}$极易溶于水,浓硫酸可用于干燥酸性气体${Cl_{2}}$,B项不符合题意。若铁发生吸氧腐蚀,则试管中压强减小,烧杯中的红墨水会沿导管上升,C项不符合题意。收集${NH_{3}}$的导管应插入倒立的试管底部,且收集${NH_{3}}$的装置中没有排气口,会造成试管因压强过大而破裂,不能达到实验目的,D项符合题意。
查看更多完整答案,请扫码查看


