2026年天利38套中考试题分类九年级化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年天利38套中考试题分类九年级化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第69页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
- 第189页
- 第190页
- 第191页
- 第192页
- 第193页
- 第194页
- 第195页
- 第196页
- 第197页
- 第198页
- 第199页
- 第200页
- 第201页
- 第202页
- 第203页
- 第204页
- 第205页
- 第206页
- 第207页
- 第208页
- 第209页
- 第210页
- 第211页
- 第212页
7. (2025·贵州)氯化钠是维持人的正常生理活动必不可少的物质。高盐饮食与心血管疾病密切相关,科学摄入氯化钠有益健康。
查阅资料:NaCl在唾液中溶解,钠离子转移到味蕾,使人们感知咸味。NaCl粒径越小,钠离子能越快转移到味蕾,从而避免NaCl摄入过多。NaCl结晶时,水分蒸发速度越快,晶体粒径越小。
(1)味蕾通过NaCl溶液中的离子感知咸味。
(2)减小NaCl晶体的粒径,其溶解速度变化是。
(3)提纯NaCl常采用蒸发结晶的方法,当析出晶体时,过滤,滤液是NaCl的(填“饱和”或“不饱和”)溶液。
(4)20℃时,配制100g质量分数为16%的NaCl溶液,需要NaClg。
(5)将含有大量NaCl、少量的MgCl₂和MgSO₄的固体混合物放入饱和NaCl溶液中,搅拌,过滤,能得到纯净的NaCl。解释用该方法提纯NaCl的原因是______。
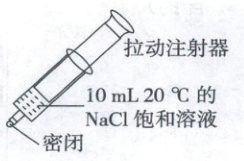
(6)按图示实验,拉动注射器,有晶体析出。同温同体积的饱和NaCl溶液在真空下蒸干和自然蒸干,判断哪一种方式析出的小粒径晶体更多并说明理由______。
查阅资料:NaCl在唾液中溶解,钠离子转移到味蕾,使人们感知咸味。NaCl粒径越小,钠离子能越快转移到味蕾,从而避免NaCl摄入过多。NaCl结晶时,水分蒸发速度越快,晶体粒径越小。
(1)味蕾通过NaCl溶液中的离子感知咸味。
(2)减小NaCl晶体的粒径,其溶解速度变化是。
(3)提纯NaCl常采用蒸发结晶的方法,当析出晶体时,过滤,滤液是NaCl的(填“饱和”或“不饱和”)溶液。
(4)20℃时,配制100g质量分数为16%的NaCl溶液,需要NaClg。
(5)将含有大量NaCl、少量的MgCl₂和MgSO₄的固体混合物放入饱和NaCl溶液中,搅拌,过滤,能得到纯净的NaCl。解释用该方法提纯NaCl的原因是______。
(6)按图示实验,拉动注射器,有晶体析出。同温同体积的饱和NaCl溶液在真空下蒸干和自然蒸干,判断哪一种方式析出的小粒径晶体更多并说明理由______。

答案:
7.
(1)钠
(2)加快
(3)饱和
(4)16
(5)少量$\mathrm{MgCl_2}$和$\mathrm{MgSO_4}$固体会溶解在饱和$\mathrm{NaCl}$溶液中,$\mathrm{NaCl}$固体不会再溶解,过滤后得到的是纯净的$\mathrm{NaCl}$
(6)真空蒸干析出小粒径晶体更多,因为真空状态下,系统压强减小,水的沸点降低,蒸发速度更快
【解析】溶解速率的影响因素+饱和溶液和不饱和溶液+一定质量分数的溶液的配制+物质的提纯
(1)$\mathrm{NaCl}$在溶液中解离为$\mathrm{Na^+}$和$\mathrm{Cl^-}$,结合资料“钠离子转移到味蕾,使人们感知咸味”,故味蕾通过$\mathrm{Na^+}$感知咸味。
(2)由$\mathrm{NaCl}$粒径越小,钠离子转移越快可知,粒径减小会加快溶解速度。
(3)蒸发结晶时,溶液达到饱和后才会析出晶体,过滤后的滤液仍为饱和溶液。
(4)配制$100\ g$质量分数为$16\%$的$\mathrm{NaCl}$溶液,需要$\mathrm{NaCl}$的质量为$100\ g × 16\% = 16\ g$。
(5)某物质的饱和溶液不能再溶解该溶质,但能溶解其他物质,所以将含有大量$\mathrm{NaCl}$、少量$\mathrm{MgCl_2}$和$\mathrm{MgSO_4}$的固体混合物加入饱和$\mathrm{NaCl}$溶液中,饱和$\mathrm{NaCl}$溶液不能溶解$\mathrm{NaCl}$,但能溶解$\mathrm{MgCl_2}$和$\mathrm{MgSO_4}$,故可提纯$\mathrm{NaCl}$。
(1)钠
(2)加快
(3)饱和
(4)16
(5)少量$\mathrm{MgCl_2}$和$\mathrm{MgSO_4}$固体会溶解在饱和$\mathrm{NaCl}$溶液中,$\mathrm{NaCl}$固体不会再溶解,过滤后得到的是纯净的$\mathrm{NaCl}$
(6)真空蒸干析出小粒径晶体更多,因为真空状态下,系统压强减小,水的沸点降低,蒸发速度更快
【解析】溶解速率的影响因素+饱和溶液和不饱和溶液+一定质量分数的溶液的配制+物质的提纯
(1)$\mathrm{NaCl}$在溶液中解离为$\mathrm{Na^+}$和$\mathrm{Cl^-}$,结合资料“钠离子转移到味蕾,使人们感知咸味”,故味蕾通过$\mathrm{Na^+}$感知咸味。
(2)由$\mathrm{NaCl}$粒径越小,钠离子转移越快可知,粒径减小会加快溶解速度。
(3)蒸发结晶时,溶液达到饱和后才会析出晶体,过滤后的滤液仍为饱和溶液。
(4)配制$100\ g$质量分数为$16\%$的$\mathrm{NaCl}$溶液,需要$\mathrm{NaCl}$的质量为$100\ g × 16\% = 16\ g$。
(5)某物质的饱和溶液不能再溶解该溶质,但能溶解其他物质,所以将含有大量$\mathrm{NaCl}$、少量$\mathrm{MgCl_2}$和$\mathrm{MgSO_4}$的固体混合物加入饱和$\mathrm{NaCl}$溶液中,饱和$\mathrm{NaCl}$溶液不能溶解$\mathrm{NaCl}$,但能溶解$\mathrm{MgCl_2}$和$\mathrm{MgSO_4}$,故可提纯$\mathrm{NaCl}$。
8. 【新素材·日常生活情境】(2025·新疆)为应对冬季降雪给交通带来的不便,各地常采取机械除雪、人工除雪、融雪剂撒布等方式开展除雪保通工作。项目小组对融雪剂融雪原理、融雪剂成分及对环境的影响产生兴趣并开展探究。
任务一:了解融雪剂融雪原理
【实践调研】小组同学经过实地走访了解到,常见融雪剂的主要成分是氯盐,本地使用的某种融雪剂可能由氯化钠、硝酸钠、氯化钙、硫酸铜中的两种或两种以上的物质组成。撒融雪剂融雪的原理是所形成的溶液凝固点①
任务二:探究融雪剂成分
小组同学为探究上述融雪剂成分,设计并完成了以下实验。
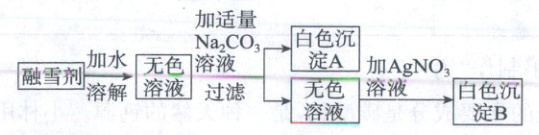
已知:氯化银为白色沉淀。
(1)该融雪剂一定含有②
(2)生成白色沉淀A的化学方程式是④______,白色沉淀B的化学式是⑤______。
任务三:调查融雪剂对环境的影响
【查阅资料】常见融雪剂的危害如表
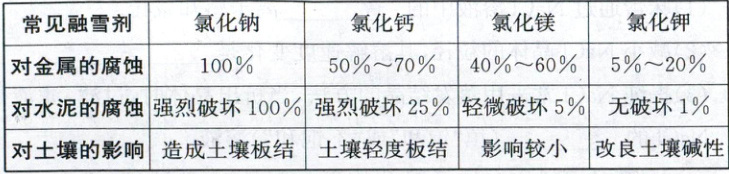
【反思评价】常见融雪剂中危害最大的成分是⑥
任务一:了解融雪剂融雪原理
【实践调研】小组同学经过实地走访了解到,常见融雪剂的主要成分是氯盐,本地使用的某种融雪剂可能由氯化钠、硝酸钠、氯化钙、硫酸铜中的两种或两种以上的物质组成。撒融雪剂融雪的原理是所形成的溶液凝固点①
降低
(填“升高”或“降低”)。任务二:探究融雪剂成分
小组同学为探究上述融雪剂成分,设计并完成了以下实验。

已知:氯化银为白色沉淀。
(1)该融雪剂一定含有②
氯化钙
,一定不含有③硫酸铜
。(2)生成白色沉淀A的化学方程式是④______,白色沉淀B的化学式是⑤______。
任务三:调查融雪剂对环境的影响
【查阅资料】常见融雪剂的危害如表

【反思评价】常见融雪剂中危害最大的成分是⑥
$\mathrm{NaCl}$
,你对道路除雪行动提出的一点建议是⑦减少融雪剂的使用(或选用危害小的融雪剂;机械除雪、人工除雪与融雪剂结合使用,降低融雪剂对环境的破坏等合理答案)
。
答案:
8.任务一 降低
任务二
(1)氯化钙 硫酸铜
(2)$\mathrm{CaCl_2 + Na_2CO_3 \xlongequal\ CaCO_3 \downarrow + 2NaCl}$ $\mathrm{AgCl}$
【反思评价】$\mathrm{NaCl}$ 减少融雪剂的使用(或选用危害小的融雪剂;机械除雪、人工除雪与融雪剂结合使用,降低融雪剂对环境的破坏等合理答案)
【解析】融雪剂成分的探究 任务一 撒融雪剂后,雪水形成溶液,使溶液的凝固点降低,低于$0\ {^{\circ}C}$,使雪在较低温度下融化,达到融雪目的。任务二 融雪剂加水溶解得无色溶液,说明不含$\mathrm{CuSO_4}$,$\mathrm{CuSO_4}$溶液呈蓝色;加适量$\mathrm{Na_2CO_3}$溶液产生白色沉淀A,说明含$\mathrm{CaCl_2}$,发生的化学反应为$\mathrm{CaCl_2 + Na_2CO_3 \xlongequal\ CaCO_3 \downarrow + 2NaCl}$,$\mathrm{CaCO_3}$是白色沉淀;无色溶液加$\mathrm{AgNO_3}$溶液产生白色沉淀B,因溶液中含氯离子($\mathrm{CaCl_2}$或可能含有的氯化钠),银离子和氯离子反应产生氯化银白色沉淀,无法确定融雪剂中是否含$\mathrm{NaCl}$、$\mathrm{NaNO_3}$。
(1)由上述分析可知,该融雪剂一定含有$\mathrm{CaCl_2}$,一定不含有$\mathrm{CuSO_4}$。
(2)生成白色沉淀A的化学方程式为$\mathrm{CaCl_2 + Na_2CO_3 \xlongequal\ CaCO_3 \downarrow + 2NaCl}$,白色沉淀B是$\mathrm{AgCl}$。【反思评价】分析表格数据,氯化钠对金属的腐蚀、对水泥的腐蚀均为$100\%$,对土壤的影响是造成土壤板结,因此危害最大的成分是氯化钠。
任务二
(1)氯化钙 硫酸铜
(2)$\mathrm{CaCl_2 + Na_2CO_3 \xlongequal\ CaCO_3 \downarrow + 2NaCl}$ $\mathrm{AgCl}$
【反思评价】$\mathrm{NaCl}$ 减少融雪剂的使用(或选用危害小的融雪剂;机械除雪、人工除雪与融雪剂结合使用,降低融雪剂对环境的破坏等合理答案)
【解析】融雪剂成分的探究 任务一 撒融雪剂后,雪水形成溶液,使溶液的凝固点降低,低于$0\ {^{\circ}C}$,使雪在较低温度下融化,达到融雪目的。任务二 融雪剂加水溶解得无色溶液,说明不含$\mathrm{CuSO_4}$,$\mathrm{CuSO_4}$溶液呈蓝色;加适量$\mathrm{Na_2CO_3}$溶液产生白色沉淀A,说明含$\mathrm{CaCl_2}$,发生的化学反应为$\mathrm{CaCl_2 + Na_2CO_3 \xlongequal\ CaCO_3 \downarrow + 2NaCl}$,$\mathrm{CaCO_3}$是白色沉淀;无色溶液加$\mathrm{AgNO_3}$溶液产生白色沉淀B,因溶液中含氯离子($\mathrm{CaCl_2}$或可能含有的氯化钠),银离子和氯离子反应产生氯化银白色沉淀,无法确定融雪剂中是否含$\mathrm{NaCl}$、$\mathrm{NaNO_3}$。
(1)由上述分析可知,该融雪剂一定含有$\mathrm{CaCl_2}$,一定不含有$\mathrm{CuSO_4}$。
(2)生成白色沉淀A的化学方程式为$\mathrm{CaCl_2 + Na_2CO_3 \xlongequal\ CaCO_3 \downarrow + 2NaCl}$,白色沉淀B是$\mathrm{AgCl}$。【反思评价】分析表格数据,氯化钠对金属的腐蚀、对水泥的腐蚀均为$100\%$,对土壤的影响是造成土壤板结,因此危害最大的成分是氯化钠。
查看更多完整答案,请扫码查看


