2026年天利38套中考试题分类九年级化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年天利38套中考试题分类九年级化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第53页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
- 第189页
- 第190页
- 第191页
- 第192页
- 第193页
- 第194页
- 第195页
- 第196页
- 第197页
- 第198页
- 第199页
- 第200页
- 第201页
- 第202页
- 第203页
- 第204页
- 第205页
- 第206页
- 第207页
- 第208页
- 第209页
- 第210页
- 第211页
- 第212页
35.(2025·贵州)在推进中国式现代化建设的进程中,桥梁是贵州一张亮丽的名片。金属材料在桥梁建造中发挥着重要作用。
(1)桥梁的金属材料
①建造桥梁使用的金属材料主要有铁、锌、铝、钢丝、镀锌钢丝、镀锌铝钢丝等。其中属于合金的是(填一种)。
②将赤铁矿(Fe₂O₃)、焦炭和石灰石一起加入高炉。在高温下,炉内CO和Fe₂O₃反应得到Fe,反应的化学方程式为____。
(2)金属材料的制造
一种超高强度锌铝合金镀层钢丝生产的主要工序如图甲所示:
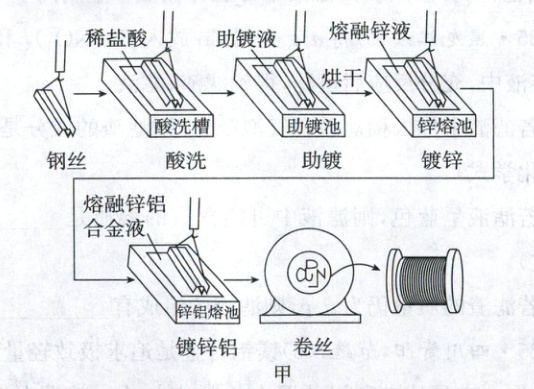
①“酸洗”时,将钢丝放入酸洗槽中除去钢丝表面的铁锈。若“酸洗”时间过长,铁会被稀盐酸腐蚀,原理是____(用化学方程式表示)。
②“镀锌”利用了锌的活动性强于铁为钢丝提供保护。验证金属活动性Zn>Fe选用的试剂是。
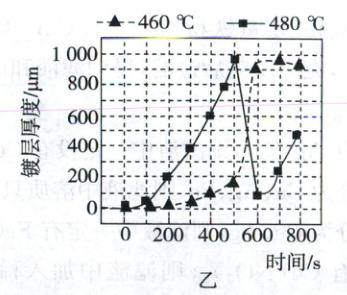
③“镀锌铝”时,镀层厚度随浸镀时间和温度变化关系如图乙,若需生产镀层厚度900μm的锌铝镀层钢丝,最好控制时间和温度为。
(3)金属材料腐蚀及防护
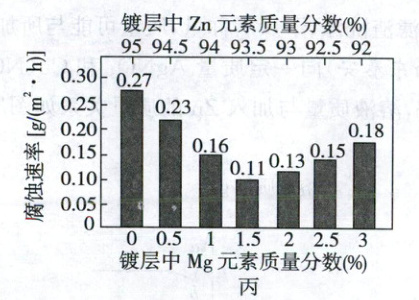
①在ZnAl镀层中加入适量Mg可调节镀层的耐腐蚀性能。取含Al质量分数为5%的ZnAlMg镀层测试镀层腐蚀速率的结果如图丙,镀层的腐蚀速率随镀层中不同Zn、Mg质量分数变化的规律是____。
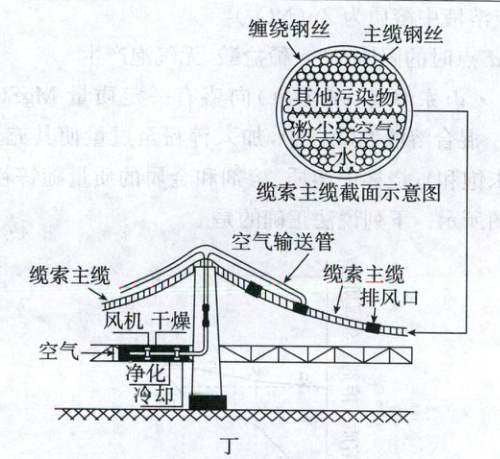
②某桥梁主缆采用ZnAlMg钢丝,工程师为了缆索主缆不被腐蚀,设计了桥梁干燥系统如图丁。说明缆索主缆的防护原理____。
(1)桥梁的金属材料
①建造桥梁使用的金属材料主要有铁、锌、铝、钢丝、镀锌钢丝、镀锌铝钢丝等。其中属于合金的是(填一种)。
②将赤铁矿(Fe₂O₃)、焦炭和石灰石一起加入高炉。在高温下,炉内CO和Fe₂O₃反应得到Fe,反应的化学方程式为____。
(2)金属材料的制造
一种超高强度锌铝合金镀层钢丝生产的主要工序如图甲所示:

①“酸洗”时,将钢丝放入酸洗槽中除去钢丝表面的铁锈。若“酸洗”时间过长,铁会被稀盐酸腐蚀,原理是____(用化学方程式表示)。
②“镀锌”利用了锌的活动性强于铁为钢丝提供保护。验证金属活动性Zn>Fe选用的试剂是。
③“镀锌铝”时,镀层厚度随浸镀时间和温度变化关系如图乙,若需生产镀层厚度900μm的锌铝镀层钢丝,最好控制时间和温度为。

(3)金属材料腐蚀及防护
①在ZnAl镀层中加入适量Mg可调节镀层的耐腐蚀性能。取含Al质量分数为5%的ZnAlMg镀层测试镀层腐蚀速率的结果如图丙,镀层的腐蚀速率随镀层中不同Zn、Mg质量分数变化的规律是____。

②某桥梁主缆采用ZnAlMg钢丝,工程师为了缆索主缆不被腐蚀,设计了桥梁干燥系统如图丁。说明缆索主缆的防护原理____。

答案:
35.
(1)①钢丝(或镀锌钢丝或镀锌铝钢丝$) ②3CO+Fe₂O₃\stackrel{高温}{=}2Fe+3CO₂$
(2)①Fe+2HCl=FeCl₂+H₂↑ ②铁片和硫酸锌溶液(或锌片和硫酸亚铁溶液,合理即可) ③600~800s,460℃
(3)①Zn质量分数由95%降低到93.5%、Mg质量分数由0增大到1.5%过程中,腐蚀速率下降;Zn质量分数由93.5%降低到92%,Mg质量分数由1.5%增大到3%过程中,腐蚀速率上升 ②利用干燥空气的流动,除去缆索主缆中的水、粉尘和其他污染物
【解析】金属材料+金属锈蚀与防护
(1)①铁、锌、铝属于纯金属,钢丝、镀锌钢丝、镀锌铝钢丝属于合金。②高温条件下CO与Fe₂O₃反应生成Fe和CO₂,化学方程式为$3CO+Fe₂O₃\stackrel{高温}{=}2Fe+3CO₂。$
(2)①酸洗时间过长,铁会被稀盐酸腐蚀,发生的是铁与盐酸生成氯化亚铁和氢气的反应,化学方程式为Fe+2HCl=FeCl₂+H₂↑。②利用金属能否与其他金属的盐溶液反应可验证金属的活动性顺序,要验证金属活动性Zn>Fe,可将锌片放入硫酸亚铁溶液中,通过溶液颜色变化来证明,或将铁片放入硫酸锌溶液中无明显现象来证明。③由图乙可知,若需生产镀层厚度900μm的锌铝镀层钢丝,最好控制时间和温度为600~800s,460℃。
(3)②金属锈蚀的条件是与水和氧气接触,该设计利用干燥空气的流动,除去缆索主缆中的水、粉尘和其他污染物,破坏锈蚀条件,实现防护。
(1)①钢丝(或镀锌钢丝或镀锌铝钢丝$) ②3CO+Fe₂O₃\stackrel{高温}{=}2Fe+3CO₂$
(2)①Fe+2HCl=FeCl₂+H₂↑ ②铁片和硫酸锌溶液(或锌片和硫酸亚铁溶液,合理即可) ③600~800s,460℃
(3)①Zn质量分数由95%降低到93.5%、Mg质量分数由0增大到1.5%过程中,腐蚀速率下降;Zn质量分数由93.5%降低到92%,Mg质量分数由1.5%增大到3%过程中,腐蚀速率上升 ②利用干燥空气的流动,除去缆索主缆中的水、粉尘和其他污染物
【解析】金属材料+金属锈蚀与防护
(1)①铁、锌、铝属于纯金属,钢丝、镀锌钢丝、镀锌铝钢丝属于合金。②高温条件下CO与Fe₂O₃反应生成Fe和CO₂,化学方程式为$3CO+Fe₂O₃\stackrel{高温}{=}2Fe+3CO₂。$
(2)①酸洗时间过长,铁会被稀盐酸腐蚀,发生的是铁与盐酸生成氯化亚铁和氢气的反应,化学方程式为Fe+2HCl=FeCl₂+H₂↑。②利用金属能否与其他金属的盐溶液反应可验证金属的活动性顺序,要验证金属活动性Zn>Fe,可将锌片放入硫酸亚铁溶液中,通过溶液颜色变化来证明,或将铁片放入硫酸锌溶液中无明显现象来证明。③由图乙可知,若需生产镀层厚度900μm的锌铝镀层钢丝,最好控制时间和温度为600~800s,460℃。
(3)②金属锈蚀的条件是与水和氧气接触,该设计利用干燥空气的流动,除去缆索主缆中的水、粉尘和其他污染物,破坏锈蚀条件,实现防护。
查看更多完整答案,请扫码查看


