2026年高中必刷题高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高中必刷题高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第6页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
5. [河北邯郸2025高一月考]蔗糖与浓硫酸发生反应的过程如图所示。
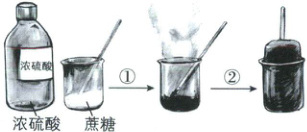
下列关于该过程的分析不正确的是(
A.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
B.过程①白色固体变黑,主要体现了浓硫酸的脱水性
C.过程②固体体积膨胀,与产生的大量气体有关
D.过程中蔗糖分子发生了化学键的断裂

下列关于该过程的分析不正确的是(
A
)A.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
B.过程①白色固体变黑,主要体现了浓硫酸的脱水性
C.过程②固体体积膨胀,与产生的大量气体有关
D.过程中蔗糖分子发生了化学键的断裂
答案:
5.A 【解析】浓硫酸与蔗糖脱水形成的炭黑反应生成的SO₂能使品红溶液褪色,体现浓硫酸的强氧化性,A符合题意;浓硫酸具有脱水性,能将蔗糖中的H原子和O原子按2:1的比例脱除,蔗糖中加入浓硫酸,白色固体变黑,体现浓硫酸的脱水性,B不符合题意;浓硫酸脱水过程中会释放大量热,发生反应:C + 2H₂SO₄(浓$) \xlongequal{△} CO₂↑ + 2SO₂↑ + 2H₂O,$产生大量气体,使固体体积膨胀,C不符合题意;该过程中,蔗糖发生化学反应,发生了化学键的断裂,D不符合题意。
6. [陕西安康2025高一期中联考]某学习小组设计如图所示的装置对浓硫酸与木炭的反应进行实验探究(部分夹持装置略)。下列说法不正确的是(
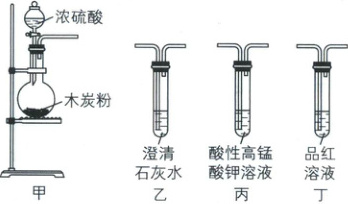
A.甲装置中还缺少加热仪器
B.用丙或丁装置均可探究SO₂的漂白性
C.按甲→丁→丙顺序连接装置,可证明浓硫酸的还原产物是SO₂
D.按甲→丁→丙→乙顺序连接装置(丙中溶液未变为无色),可证明木炭的氧化产物是CO₂
B
)
A.甲装置中还缺少加热仪器
B.用丙或丁装置均可探究SO₂的漂白性
C.按甲→丁→丙顺序连接装置,可证明浓硫酸的还原产物是SO₂
D.按甲→丁→丙→乙顺序连接装置(丙中溶液未变为无色),可证明木炭的氧化产物是CO₂
答案:
6.B 【解析】浓硫酸与木炭的反应需要在加热条件下进行,故甲装置中还缺少加热仪器,A正确;用丙装置探究SO₂的还原性,用丁装置探究SO₂的漂白性,B错误;按甲→丁→丙顺序连接装置,若丁装置中的品红溶液褪色,证明反应有SO₂生成,丙装置可进一步检验并吸收SO₂,C正确;按甲→丁(检验二氧化硫)→丙(除去二氧化硫,溶液颜色变浅)→乙(澄清石灰水变浑浊)顺序连接装置,可证明木炭的氧化产物是CO₂,D正确。
7. 教材变式[四川南充2024高一月考]下列区分浓硫酸和稀硫酸的方法中既绿色环保又简单可行的是(
A.取样,分别放入质量相同的铜片
B.取样,分别滴入紫色石蕊溶液中,观察颜色
C.用玻璃棒各蘸取少许涂在纸上
D.加入锌粒,观察是否有气体生成
C
)A.取样,分别放入质量相同的铜片
B.取样,分别滴入紫色石蕊溶液中,观察颜色
C.用玻璃棒各蘸取少许涂在纸上
D.加入锌粒,观察是否有气体生成
答案:
7.C 教材变式 本题是教材P10练习与应用第6题的变式题,教材考查了浓硫酸、稀硫酸的鉴别,变式题则给出了四种区分浓硫酸、稀硫酸的方法,考查实验方案的评价。
【解析】常温下,浓硫酸、稀硫酸和Cu都不反应,A错误;少量的浓硫酸、稀硫酸滴入紫色石蕊溶液中都能使紫色石蕊溶液变红,B错误;浓硫酸具有脱水性,浓硫酸能使纸炭化变黑,C正确;浓硫酸与Zn反应生成有毒的SO₂气体,不符合绿色环保的要求,D错误。
【解析】常温下,浓硫酸、稀硫酸和Cu都不反应,A错误;少量的浓硫酸、稀硫酸滴入紫色石蕊溶液中都能使紫色石蕊溶液变红,B错误;浓硫酸具有脱水性,浓硫酸能使纸炭化变黑,C正确;浓硫酸与Zn反应生成有毒的SO₂气体,不符合绿色环保的要求,D错误。
8. [辽宁重点中学2025高一期中联考]取少量试样,进行下列实验,能判断溶液中一定含有SO₄²⁻的操作是(
A.滴加BaCl₂溶液,产生白色沉淀
B.滴加盐酸酸化的BaCl₂溶液,产生白色沉淀
C.滴加BaCl₂溶液,产生白色沉淀,加稀盐酸沉淀不溶解
D.加入稀盐酸酸化,无明显现象,加入BaCl₂溶液,有白色沉淀生成
D
)A.滴加BaCl₂溶液,产生白色沉淀
B.滴加盐酸酸化的BaCl₂溶液,产生白色沉淀
C.滴加BaCl₂溶液,产生白色沉淀,加稀盐酸沉淀不溶解
D.加入稀盐酸酸化,无明显现象,加入BaCl₂溶液,有白色沉淀生成
答案:
8.D 【解析】滴加BaCl₂溶液,产生白色沉淀,该沉淀可能是BaSO₄,也可能是AgCl、BaCO₃、BaSO₃等,所以不能确定溶液中一定含有SO₄²⁻,A错误;滴加盐酸酸化的BaCl₂溶液,产生白色沉淀,同样不能排除Ag⁺的干扰,因为Ag⁺与Cl⁻在酸性条件下也会生成AgCl白色沉淀,B错误;滴加BaCl₂溶液,产生白色沉淀,加稀盐酸沉淀不溶解,还是不能排除AgCl沉淀的可能(AgCl沉淀不溶于酸),C错误;加入盐酸酸化,无明显现象,排除了CO₃²⁻(CO₃²⁻与H⁺反应会产生二氧化碳气体)、SO₃²⁻(SO₃²⁻与H⁺反应会产生二氧化硫气体)和Ag⁺(Ag⁺与Cl⁻反应会生成沉淀)等的干扰,再加入BaCl₂溶液,有白色沉淀生成,此沉淀只能是BaSO₄,所以能判断溶液中一定含有SO₄²⁻,D正确。
易错警示 SO₄²⁻检验的常见误区
(1)只加可溶性钡盐,不酸化。误将CO₃²⁻、PO₄³⁻、SO₃²⁻等干扰离子判断成SO₄²⁻。因上述离子会产生BaCO₃、Ba₃(PO₄)₂、BaSO₃等白色沉淀。
(2)误将Ag⁺判断成SO₄²⁻。如向待测液中滴加BaCl₂溶液有白色沉淀,再加稀盐酸白色沉淀不溶解便断定含SO₄²⁻。其错误是未注意溶液中不含SO₄²⁻,而含Ag⁺时也会产生同样的现象:Ag⁺ + Cl⁻ ══ AgCl↓(白色)。
(3)误将SO₃²⁻判断成SO₄²⁻。如向待测液中滴加用稀硝酸酸化的Ba(NO₃)₂溶液,生成白色沉淀,便误以为有SO₄²⁻。该错误是未注意NO₃⁻在酸性环境中具有强氧化性,发生反应:Ba²⁺ + SO₃²⁻ ══ BaSO₃↓(白色),3BaSO₃ + 2H⁺ + 2NO₃⁻ ══ 3BaSO₄(白色) + 2NO↑ + H₂O。
易错警示 SO₄²⁻检验的常见误区
(1)只加可溶性钡盐,不酸化。误将CO₃²⁻、PO₄³⁻、SO₃²⁻等干扰离子判断成SO₄²⁻。因上述离子会产生BaCO₃、Ba₃(PO₄)₂、BaSO₃等白色沉淀。
(2)误将Ag⁺判断成SO₄²⁻。如向待测液中滴加BaCl₂溶液有白色沉淀,再加稀盐酸白色沉淀不溶解便断定含SO₄²⁻。其错误是未注意溶液中不含SO₄²⁻,而含Ag⁺时也会产生同样的现象:Ag⁺ + Cl⁻ ══ AgCl↓(白色)。
(3)误将SO₃²⁻判断成SO₄²⁻。如向待测液中滴加用稀硝酸酸化的Ba(NO₃)₂溶液,生成白色沉淀,便误以为有SO₄²⁻。该错误是未注意NO₃⁻在酸性环境中具有强氧化性,发生反应:Ba²⁺ + SO₃²⁻ ══ BaSO₃↓(白色),3BaSO₃ + 2H⁺ + 2NO₃⁻ ══ 3BaSO₄(白色) + 2NO↑ + H₂O。
9. [湖南邵阳2024高一期末联考]某工业废水中存在大量的Na⁺、Cl⁻、Cu²⁺、SO₄²⁻,欲除去其中的Cu²⁺、SO₄²⁻,设计工艺流程如下所示:

下列有关说法错误的是(
A.NaOH的作用是除去Cu²⁺
B.试剂a为Na₂CO₃,试剂b为BaCl₂
C.操作x为过滤,试剂c为稀盐酸
D.检验SO₄²⁻是否除尽,可取适量待测溶液,先加入盐酸,再加入BaCl₂溶液

下列有关说法错误的是(
B
)A.NaOH的作用是除去Cu²⁺
B.试剂a为Na₂CO₃,试剂b为BaCl₂
C.操作x为过滤,试剂c为稀盐酸
D.检验SO₄²⁻是否除尽,可取适量待测溶液,先加入盐酸,再加入BaCl₂溶液
答案:
9.B 【解析】废水中只有Cu²⁺可以和NaOH反应,NaOH的作用是除去Cu²⁺,A正确;试剂a为BaCl₂,试剂b为Na₂CO₃,碳酸钠用于除去过量钡离子,B错误;题给流程图中操作x为过滤,滤液中含Na⁺、Cl⁻、CO₃²⁻、OH⁻,试剂c为稀盐酸,可除去CO₃²⁻、OH⁻,C正确;检验SO₄²⁻是否除尽,可取适量待测溶液,先加入盐酸,再加入BaCl₂溶液,如果没有白色沉淀生成,说明已经除尽,D正确。
10. [安徽宣城中学2025高一期中]下列关于硫酸盐说法错误的是(
A.美术教室里的各种塑像,主要是用硫酸钙制作完成的
B.进行消化系统X射线检查前,服用的“钡餐”中含有硫酸钡
C.检验无水酒精中是否真的没有水,常用胆矾晶体
D.船员打上来的黄河水比较浑浊,常加明矾使杂质沉降
C
)A.美术教室里的各种塑像,主要是用硫酸钙制作完成的
B.进行消化系统X射线检查前,服用的“钡餐”中含有硫酸钡
C.检验无水酒精中是否真的没有水,常用胆矾晶体
D.船员打上来的黄河水比较浑浊,常加明矾使杂质沉降
答案:
10.C 【解析】硫酸钙(熟石膏)常用于制作塑像,因其与水混合后很快凝固成型,A正确。硫酸钡不溶于水和酸,且不易被X射线透过,在医疗上可用作检查消化系统的内服药剂,俗称“钡餐”,B正确。检验水分常用无水硫酸铜(白色粉末),无水CuSO₄遇水转化为蓝色的胆矾(CuSO₄·5H₂O),胆矾本身无法检验水,C错误。明矾[KAl(SO₄)₂·12H₂O]溶于水后会生成Al(OH)₃胶体,可以吸附水中的悬浮物和杂质使其聚集而沉降,达到净水目的,D正确。
11. 将铜丝插入热的浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是(
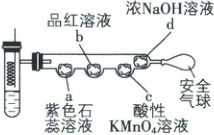
A.Cu与浓硫酸反应,体现浓H₂SO₄的酸性和强氧化性
B.a处变红,说明H₂SO₄具有挥发性
C.b或c处褪色,均说明SO₂具有漂白性
D.试管底部出现白色固体,说明浓硫酸具有脱水性
A
)
A.Cu与浓硫酸反应,体现浓H₂SO₄的酸性和强氧化性
B.a处变红,说明H₂SO₄具有挥发性
C.b或c处褪色,均说明SO₂具有漂白性
D.试管底部出现白色固体,说明浓硫酸具有脱水性
答案:
11.A 【解析】铜和浓硫酸反应过程中,生成CuSO₄体现浓硫酸的酸性,生成SO₂体现浓硫酸的强氧化性,A正确;a处的紫色石蕊溶液变红,其原因是反应生成的SO₂溶于水生成了H₂SO₃,H₂SO₃溶液显酸性,使紫色石蕊变红,硫酸是难挥发性酸,B错误;b处品红溶液褪色,其原因是SO₂具有漂白性,而c处酸性高锰酸钾溶液褪色,其原因是SO₂和KMnO₄发生氧化还原反应,SO₂体现还原性,C错误;实验过程中试管底部出现白色固体,其成分为无水CuSO₄,体现浓硫酸的吸水性,D错误。
易错警示 浓硫酸的强氧化性体现在硫元素的化合价降低(氧化还原反应);浓硫酸的脱水性表现为H、O原子按2:1的个数比脱离原物质(发生化学变化);吸水性的表现是原物质中的水分(包含结晶水)被浓硫酸吸收。
易错警示 浓硫酸的强氧化性体现在硫元素的化合价降低(氧化还原反应);浓硫酸的脱水性表现为H、O原子按2:1的个数比脱离原物质(发生化学变化);吸水性的表现是原物质中的水分(包含结晶水)被浓硫酸吸收。
查看更多完整答案,请扫码查看


