2026年高中必刷题高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高中必刷题高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第15页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1. [四川成都 2024 高一月考]氨广泛应用于化工、化肥、制药等领域,一种新型制备氨的方法如图。下列说法错误的是(

A.反应①属于氮的固定
B.反应②属于氧化还原反应
C.反应⑤在无水环境中进行时,有白烟产生
D.该转化过程总反应的反应物是 $ {N_{2}} $ 和 $ {H_{2}O} $,产物是 $ {NH_{3}} $ 和 $ {O_{2}} $
B
)
A.反应①属于氮的固定
B.反应②属于氧化还原反应
C.反应⑤在无水环境中进行时,有白烟产生
D.该转化过程总反应的反应物是 $ {N_{2}} $ 和 $ {H_{2}O} $,产物是 $ {NH_{3}} $ 和 $ {O_{2}} $
答案:
1.B [解析]反应①是氮气和镁化合生成氮化镁,N由游离态转化为化合态,属于人工固氮,A正确;反应②是氮化镁和氯化铵反应生成氯化镁和氨气,各元素的化合价均不变,属于非氧化还原反应,B错误;反应⑤是氨气和氯化氢反应生成氯化铵,在无水环境中进行时,有白烟产生,C正确;根据题图可判断该转化过程中总反应的反应物是$\mathrm{N_2}$和$\mathrm{H_2O}$,产物是$\mathrm{NH_3}$和$\mathrm{O_2}$,D正确。
2. [河北石家庄二中 2025 高一期中]氨法脱硫工艺是利用氨水吸收烟气中的 $ {SO_{2}} $ 生成亚硫酸铵溶液,并在富氧条件下将亚硫酸铵氧化成硫酸铵。已知酸性条件下 $ {NO^{-}_{3}} $ 具有强氧化性。关于该工艺的说法错误的是(
A.涉及反应的离子方程式为 $ {2NH_{3} · H_{2}O + SO_{2} \xlongequal{} 2NH^{+}_{4} + SO^{2-}_{3} + H_{2}O} $、$ {2SO^{2-}_{3} + O_{2} \xlongequal{} 2SO^{2-}_{4}} $
B.硫酸铵是农业上常用的化肥
C.可用盐酸酸化的硝酸钡溶液区分亚硫酸铵和硫酸铵溶液
D.进行检验 $ {NH^{+}_{4}} $ 的实验时,需通风并注意防烫伤
C
)A.涉及反应的离子方程式为 $ {2NH_{3} · H_{2}O + SO_{2} \xlongequal{} 2NH^{+}_{4} + SO^{2-}_{3} + H_{2}O} $、$ {2SO^{2-}_{3} + O_{2} \xlongequal{} 2SO^{2-}_{4}} $
B.硫酸铵是农业上常用的化肥
C.可用盐酸酸化的硝酸钡溶液区分亚硫酸铵和硫酸铵溶液
D.进行检验 $ {NH^{+}_{4}} $ 的实验时,需通风并注意防烫伤
答案:
2.C [解析]由“利用氨水吸收烟气中的$\mathrm{SO_2}$生成亚硫酸铵溶液,并在富氧条件下将亚硫酸铵氧化成硫酸铵”知,反应的离子方程式为$\mathrm{2NH_3· H_2O + SO_2 \xlongequal{} 2NH_4^+ + SO_3^{2-} + H_2O}$、$\mathrm{2SO_3^{2-} + O_2 \xlongequal{} 2SO_4^{2-}}$,A正确;农业上常用的氮肥主要有尿素、硫酸铵、氯化铵、碳酸氢铵等,B正确;$\mathrm{NO_3^-}$在酸性条件下具有强氧化性,盐酸酸化的硝酸钡溶液能将$\mathrm{SO_3^{2-}}$氧化为$\mathrm{SO_4^{2-}}$,两溶液反应后均生成$\mathrm{BaSO_4}$沉淀,无法区分,C错误;检验$\mathrm{NH_4^+}$需加热验证$\mathrm{NH_3}$的生成来进行,$\mathrm{NH_3}$有毒,因此需通风且注意防烫伤,D正确。
3. [江西部分学校 2025 高一联考]如图所示,同温同压下在两个相同的圆底烧瓶(容积为 $ V \ {L} $)中分别充满相应的气体后,打开止水夹并挤出胶头滴管中的水,都可产生“喷泉”,对两瓶“喷泉”的比较,下列说法错误的是(
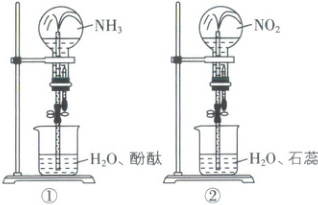
A.两烧瓶中气体颜色不同,两“喷泉”溶液都是红色
B.“喷泉”后烧瓶中溶液的 $ {pH} $:瓶①>瓶②
C.“喷泉”后烧瓶中溶液的体积:瓶①>瓶②
D.“喷泉”后烧瓶中溶液的物质的量浓度:瓶①>瓶②
D
)
A.两烧瓶中气体颜色不同,两“喷泉”溶液都是红色
B.“喷泉”后烧瓶中溶液的 $ {pH} $:瓶①>瓶②
C.“喷泉”后烧瓶中溶液的体积:瓶①>瓶②
D.“喷泉”后烧瓶中溶液的物质的量浓度:瓶①>瓶②
答案:
3.D [解析]氨气是无色气体,溶于水产生的氨水呈碱性,使酚酞溶液变红,$\mathrm{NO_2}$是红棕色气体,溶于水产生的硝酸呈酸性,使石蕊试液变红,故气体颜色不同,“喷泉”颜色都呈红色,A正确;氨气溶于水后溶液呈碱性,$\mathrm{NO_2}$与$\mathrm{H_2O}$反应后溶液呈酸性,前者pH大,B正确;瓶①中氨气完全溶解,溶液充满烧瓶,体积为V,瓶②中发生反应:$\mathrm{3NO_2 + H_2O \xlongequal{} 2HNO_3 + NO}$,生成的NO不溶于水,最终溶液体积等于初始$\mathrm{NO_2}$体积的$\frac{2}{3}$,即$\frac{2}{3}V$,C正确;结合C项分析知,瓶①中所得溶液浓度为$\frac{V\mathrm{L· mol^{-1}}}{VL} = \frac{1}{V_m}\mathrm{mol· L^{-1}}$,瓶②中所得溶液浓度为$\frac{\frac{2}{3}× V\mathrm{L· mol^{-1}}}{VL} = \frac{1}{V_m}\mathrm{mol· L^{-1}}$,故溶液的物质的量浓度:瓶①=瓶②,D错误。
4. 下列有关含氮化合物的实验装置和原理能达到相应实验目的的是(

A.已知铁与稀硝酸反应生成 $ {NO} $,实验室采用装置甲可证明 $ {NO} $ 能直接被 $ {NaOH} $ 溶液吸收
B.用装置乙分离氯化钠和氯化铵
C.用装置丙验证氨气溶于水显碱性
D.用装置丁吸收氨气尾气,可有效防止倒吸
B
)
A.已知铁与稀硝酸反应生成 $ {NO} $,实验室采用装置甲可证明 $ {NO} $ 能直接被 $ {NaOH} $ 溶液吸收
B.用装置乙分离氯化钠和氯化铵
C.用装置丙验证氨气溶于水显碱性
D.用装置丁吸收氨气尾气,可有效防止倒吸
答案:
4.B [解析]$\mathrm{NO}$不溶于水,且不与氢氧化钠反应,不能被氢氧化钠溶液吸收,A错误;氯化铵受热分解为氯化氢气体及氨气,遇冷后在烧瓶底部又重新生成氯化铵固体,能分离$\mathrm{NaCl}$和$\mathrm{NH_4Cl}$,B正确;氨气不能使蓝色石蕊试纸变色,验证氨气溶于水显碱性应用湿润的红色石蕊试纸,C错误;稀硫酸与氨气反应,能吸收$\mathrm{NH_3}$,但该装置不能防倒吸,应将煤油换为密度比稀硫酸大且不能溶解$\mathrm{NH_3}$的试剂(如有机溶剂$\mathrm{CCl_4}$),并将$\mathrm{NH_3}$通入该试剂中,D错误。
5. [宁夏吴忠中学 2025 高一月考]某科学探究小组为了制取氨气并探究其性质,设计了如图所示的实验装置。
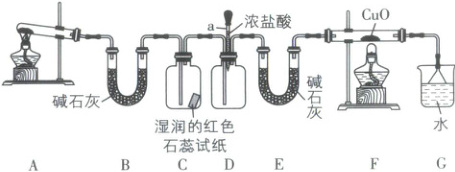
请回答下列问题:
(1) 仪器 $ a $ 的名称是
(2) 装置 $ C $ 中的现象是______;其原因是______(用离子方程式表示);一段时间后,挤压仪器 $ a $,滴入浓盐酸,$ D $ 中的现象是______;检验 $ D $ 中生成物的阳离子的操作和现象是取少量 $ D $ 中生成的固体物质于试管中,______。
(3) 实验进行一段时间后,装置 $ F $ 中硬质玻璃管中除生成单质铜外,还有两种无污染的物质生成,则硬质玻璃管中发生反应的化学方程式为

请回答下列问题:
(1) 仪器 $ a $ 的名称是
胶头滴管
;装置 $ G $ 中倒扣漏斗的目的是防止倒吸
。(2) 装置 $ C $ 中的现象是______;其原因是______(用离子方程式表示);一段时间后,挤压仪器 $ a $,滴入浓盐酸,$ D $ 中的现象是______;检验 $ D $ 中生成物的阳离子的操作和现象是取少量 $ D $ 中生成的固体物质于试管中,______。
(3) 实验进行一段时间后,装置 $ F $ 中硬质玻璃管中除生成单质铜外,还有两种无污染的物质生成,则硬质玻璃管中发生反应的化学方程式为
$\mathrm{2NH_3 + 3CuO \xlongequal{\Delta} 3Cu + N_2 + 3H_2O}$
。
答案:
5.
(1)胶头滴管 防止倒吸
(2)湿润的红色石蕊试纸变蓝 $\mathrm{NH_3 + H_2O \rightleftharpoons NH_3· H_2O}$、$\mathrm{NH_3· H_2O \rightleftharpoons NH_4^+ + OH^-}$ 产生白烟 向试管中加入浓$\mathrm{NaOH}$溶液并加热,将湿润的红色石蕊试纸放于试管口处,观察到湿润的红色石蕊试纸变蓝
(3)$\mathrm{2NH_3 + 3CuO \xlongequal{\Delta} 3Cu + N_2 + 3H_2O}$
思路导引A中氢氧化钙与氯化铵共热反应制备氨气,通过B中碱石灰干燥后,与C中湿润的红色石蕊试纸作用,试纸变蓝,装置D中胶头滴管装有浓盐酸,与氨气作用生成氯化铵,再通过E中碱石灰干燥,干燥的氨气与F中氧化铜共热反应生成铜、氮气和水,最后利用水吸收未反应的氨气,并用倒扣的漏斗防倒吸。
[解析]
(1)根据仪器的构造可知,仪器a的名称是胶头滴管;氨气极易溶于水,故装置G中倒扣漏斗的目的是防止倒吸。
(2)装置C中的现象是湿润的红色石蕊试纸变蓝;其原因是氨气与水反应生成的一水合氨电离出氢氧根离子:$\mathrm{NH_3 + H_2O \rightleftharpoons NH_3· H_2O}$、$\mathrm{NH_3· H_2O \rightleftharpoons NH_4^+ + OH^-}$;一段时间后,挤压仪器a,滴入浓盐酸,挥发出的$\mathrm{HCl}$和氨气反应生成氯化铵小颗粒,D中的现象是产生白烟;D中生成物的阳离子为$\mathrm{NH_4^+}$,$\mathrm{NH_4^+}$与浓$\mathrm{NaOH}$溶液等碱液在加热条件下反应时会生成$\mathrm{NH_3}$,$\mathrm{NH_3}$可使湿润的红色石蕊试纸变蓝,检验$\mathrm{NH_4^+}$可利用该性质,具体操作见答案。
(3)实验进行一段时间后,装置F中硬质玻璃管中除生成单质铜外,还有两种无污染的物质生成,铜元素化合价降低,结合元素守恒,生成的两种无污染物质为$\mathrm{N_2}$和水,则硬质玻璃管中发生反应的化学方程式为$\mathrm{2NH_3 + 3CuO \xlongequal{\Delta} 3Cu + N_2 + 3H_2O}$。
(1)胶头滴管 防止倒吸
(2)湿润的红色石蕊试纸变蓝 $\mathrm{NH_3 + H_2O \rightleftharpoons NH_3· H_2O}$、$\mathrm{NH_3· H_2O \rightleftharpoons NH_4^+ + OH^-}$ 产生白烟 向试管中加入浓$\mathrm{NaOH}$溶液并加热,将湿润的红色石蕊试纸放于试管口处,观察到湿润的红色石蕊试纸变蓝
(3)$\mathrm{2NH_3 + 3CuO \xlongequal{\Delta} 3Cu + N_2 + 3H_2O}$
思路导引A中氢氧化钙与氯化铵共热反应制备氨气,通过B中碱石灰干燥后,与C中湿润的红色石蕊试纸作用,试纸变蓝,装置D中胶头滴管装有浓盐酸,与氨气作用生成氯化铵,再通过E中碱石灰干燥,干燥的氨气与F中氧化铜共热反应生成铜、氮气和水,最后利用水吸收未反应的氨气,并用倒扣的漏斗防倒吸。
[解析]
(1)根据仪器的构造可知,仪器a的名称是胶头滴管;氨气极易溶于水,故装置G中倒扣漏斗的目的是防止倒吸。
(2)装置C中的现象是湿润的红色石蕊试纸变蓝;其原因是氨气与水反应生成的一水合氨电离出氢氧根离子:$\mathrm{NH_3 + H_2O \rightleftharpoons NH_3· H_2O}$、$\mathrm{NH_3· H_2O \rightleftharpoons NH_4^+ + OH^-}$;一段时间后,挤压仪器a,滴入浓盐酸,挥发出的$\mathrm{HCl}$和氨气反应生成氯化铵小颗粒,D中的现象是产生白烟;D中生成物的阳离子为$\mathrm{NH_4^+}$,$\mathrm{NH_4^+}$与浓$\mathrm{NaOH}$溶液等碱液在加热条件下反应时会生成$\mathrm{NH_3}$,$\mathrm{NH_3}$可使湿润的红色石蕊试纸变蓝,检验$\mathrm{NH_4^+}$可利用该性质,具体操作见答案。
(3)实验进行一段时间后,装置F中硬质玻璃管中除生成单质铜外,还有两种无污染的物质生成,铜元素化合价降低,结合元素守恒,生成的两种无污染物质为$\mathrm{N_2}$和水,则硬质玻璃管中发生反应的化学方程式为$\mathrm{2NH_3 + 3CuO \xlongequal{\Delta} 3Cu + N_2 + 3H_2O}$。
查看更多完整答案,请扫码查看


