2026年高中必刷题高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高中必刷题高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第80页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1. [江西抚州 2024 高一月考]在 $120^{\circ}C$、$101kPa$ 下,$a mL$ 由氢气、乙烯组成的混合气体在 $b mL$ 氧气中充分燃烧后,恢复到原温度和压强,已知 $b>3a$,且燃烧后气体体积缩小了 $\frac{b}{16}mL$,则乙烯的体积为(
A.$\frac{b}{16}mL$
B.$\frac{b}{8}mL$
C.$(a-\frac{b}{8})mL$
D.$(a-\frac{b}{16})mL$
C
)A.$\frac{b}{16}mL$
B.$\frac{b}{8}mL$
C.$(a-\frac{b}{8})mL$
D.$(a-\frac{b}{16})mL$
答案:
1.C 【解析】根据反应方程式:$2H_2+O_2\overset{点燃}=\!=\!=2H_2O(g)$、$C_2H_4+3O_2\overset{点燃}=\!=\!=2CO_2+2H_2O(g)$知,$C_2H_4$充分燃烧后气体体积无变化,故燃烧后气体体积缩小了$\frac{b}{16}mL$是$H_2$燃烧引起的,根据反应$2H_2+O_2\overset{点燃}=\!=\!=2H_2O(g)$可知,混合气体中氢气的体积为$\frac{b}{8}mL$,故$C_2H_4$的体积为$(a-\frac{b}{8})mL$,C正确。
2. [山西晋城一中 2025 高一期中]在 $105^{\circ}C$ 时,$1L$ 两种气态混合烃与 $9L$ 氧气混合,充分燃烧后恢复到原状态,所得气体体积为 $10.5L$,再将气体通过碱石灰,体积缩小 $6L$。则下列各组混合烃中符合此条件的是(
A.$CH_{4}$、$C_{4}H_{8}$
B.$CH_{4}$、$C_{4}H_{10}$
C.$C_{2}H_{4}$、$C_{3}H_{8}$
D.$C_{2}H_{2}$、$C_{4}H_{10}$
D
)A.$CH_{4}$、$C_{4}H_{8}$
B.$CH_{4}$、$C_{4}H_{10}$
C.$C_{2}H_{4}$、$C_{3}H_{8}$
D.$C_{2}H_{2}$、$C_{4}H_{10}$
答案:
2.D 【解析】$105\ \celsius $时,生成的$H_2O$是气体,设混合烃的平均分子式为$C_xH_y$,混合烃燃烧后气体体积增大了$10.5\ L-1\ L-9\ L=0.5\ L$,则
$C_xH_y+\frac{4x+y}{4}O_2\overset{点燃}=\!=\!=xCO_2+\frac{y}{2}H_2O(g)\ \ \ \Delta V$
$1L$ $10.5\ L-1\ L-9\ L=0.5\ L$
$(\frac{y}{4}-1)×1\ L=1×0.5\ L$,解得$y=6$,烃的平均分子式为$C_xH_6$,将$10.5\ L$气体通过碱石灰,体积缩小$6\ L$,则生成二氧化碳和$H_2O(g)$的体积为$6\ L$,即$x+\frac{y}{2}=6$,则$x=3$,即混合烃的平均分子式为$C_3H_6$。$CH_4$、$C_4H_8$的混合物的平均分子式中,$H$原子数一定大于$C$原子数的$2$倍,$A$不符合题意;$CH_4$、$C_4H_{10}$的混合物的平均分子式中,$H$原子数一定大于$C$原子数的$2$倍,$B$不符合题意;$C_2H_4$、$C_3H_8$的混合物的平均分子式中,$H$原子数一定大于$C$原子数的$2$倍,$C$不符合题意;$C_2H_2$、$C_4H_{10}$的混合物,当二者物质的量之比为$1:1$时,平均分子式为$C_3H_6$,符合题意。
$C_xH_y+\frac{4x+y}{4}O_2\overset{点燃}=\!=\!=xCO_2+\frac{y}{2}H_2O(g)\ \ \ \Delta V$
$1L$ $10.5\ L-1\ L-9\ L=0.5\ L$
$(\frac{y}{4}-1)×1\ L=1×0.5\ L$,解得$y=6$,烃的平均分子式为$C_xH_6$,将$10.5\ L$气体通过碱石灰,体积缩小$6\ L$,则生成二氧化碳和$H_2O(g)$的体积为$6\ L$,即$x+\frac{y}{2}=6$,则$x=3$,即混合烃的平均分子式为$C_3H_6$。$CH_4$、$C_4H_8$的混合物的平均分子式中,$H$原子数一定大于$C$原子数的$2$倍,$A$不符合题意;$CH_4$、$C_4H_{10}$的混合物的平均分子式中,$H$原子数一定大于$C$原子数的$2$倍,$B$不符合题意;$C_2H_4$、$C_3H_8$的混合物的平均分子式中,$H$原子数一定大于$C$原子数的$2$倍,$C$不符合题意;$C_2H_2$、$C_4H_{10}$的混合物,当二者物质的量之比为$1:1$时,平均分子式为$C_3H_6$,符合题意。
3. [宁夏银川一中 2025 高一期末]下列说法错误的是(
A.$C_{2}H_{5}OH$、$HOCH_{2}CH_{2}COOH$ 不论以什么比例混合,只要总物质的量一定,则完全燃烧时生成的水的质量和消耗氧气的质量不变
B.等质量的甲烷、乙烯、乙炔充分燃烧,消耗氧气的物质的量依次减少
C.乙酸和两种链状单烯烃混合物中氧的质量分数为 $a$,则碳的质量分数是 $\frac{6}{7}(1 - a)$
D.常温常压下,$10mL$ 无论以何种比例混合的两种气态烃的混合气,在 $50mL$ 的氧气中燃烧生成 $CO_{2}$ 和 $H_{2}O$,恢复到原状况所得气体的体积均为 $35mL$,则该混合物可能为 $C_{3}H_{6}$ 和 $C_{4}H_{8}$
D
)A.$C_{2}H_{5}OH$、$HOCH_{2}CH_{2}COOH$ 不论以什么比例混合,只要总物质的量一定,则完全燃烧时生成的水的质量和消耗氧气的质量不变
B.等质量的甲烷、乙烯、乙炔充分燃烧,消耗氧气的物质的量依次减少
C.乙酸和两种链状单烯烃混合物中氧的质量分数为 $a$,则碳的质量分数是 $\frac{6}{7}(1 - a)$
D.常温常压下,$10mL$ 无论以何种比例混合的两种气态烃的混合气,在 $50mL$ 的氧气中燃烧生成 $CO_{2}$ 和 $H_{2}O$,恢复到原状况所得气体的体积均为 $35mL$,则该混合物可能为 $C_{3}H_{6}$ 和 $C_{4}H_{8}$
答案:
3.D 【解析】有机物完全燃烧后,碳、氢元素分别转化成二氧化碳、水,设有机物化学式为$C_xH_yO_z$,若各物质的$(x+\frac{y}{4}-\frac{z}{2})$值相等,则不论以什么比例混合,只要总物质的量一定,完全燃烧时耗氧量相同,$C_2H_5OH$、$HOCH_2CH_2COOH$的$(x+\frac{y}{4}-\frac{z}{2})$值分别为$2+1.5-0.5=3$、$3+1.5-1.5=3$,且$1$个分子中的氢原子个数相同,所以二者总物质的量一定时,完全燃烧的耗氧量及生成水的质量相等,$A$正确;烃分子中氢元素的质量分数越大,等质量烃燃烧时耗氧量越多,三种物质中氢元素质量分数大小关系为甲烷>乙烯>乙炔,则等质量的甲烷、乙烯、乙炔充分燃烧,消耗的氧气的物质的量依次减少,$B$正确;乙酸的分子式为$C_2H_4O_2$,而链状单烯烃的通式为$C_nH_{2n}$,从化学式可以发现混合物中$C$、$H$数目比为$1:2$,质量比为$6:1$,氧的质量分数为$a$,碳、氢的质量分数一共为$(1-a)$,其中碳的质量分数为$\frac{6}{7}(1-a)$,$C$正确;令混合烃的平均分子式为$C_xH_y$,$10\ mL$混合烃在$50\ mL\ O_2$中充分燃烧并恢复到常温常压后,气体的体积均为$35\ mL$,可列式:
$C_xH_y+(x+\frac{y}{4})O_2\overset{点燃}=\!=\!=xCO_2+\frac{y}{2}H_2O\ \ \ \Delta V$
$\frac{1}{10\ mL}$ $\frac{1+\frac{y}{4}}{(60-35)\ mL=25\ mL}$
$\frac{1}{10\ mL}=\frac{1+\frac{y}{4}}{25\ mL}$,解得$y=6$,即混合物不可能为$C_3H_6$和$C_4H_8$,D错误。
$C_xH_y+(x+\frac{y}{4})O_2\overset{点燃}=\!=\!=xCO_2+\frac{y}{2}H_2O\ \ \ \Delta V$
$\frac{1}{10\ mL}$ $\frac{1+\frac{y}{4}}{(60-35)\ mL=25\ mL}$
$\frac{1}{10\ mL}=\frac{1+\frac{y}{4}}{25\ mL}$,解得$y=6$,即混合物不可能为$C_3H_6$和$C_4H_8$,D错误。
4. [河南信阳 2024 高一月考]现有下列各组物质:①乙烯和乙醇;②丙烯和 2 - 丁烯;③甲苯和邻二甲苯;④甲醛和葡萄糖,只要总质量一定,各组中的两种物质不论以何种比例混合,完全燃烧时生成水的质量也总是定值的是(
A.①②
B.②④
C.③④
D.都不是
B
)A.①②
B.②④
C.③④
D.都不是
答案:
4.B 【解析】有机物燃烧生成水的质量与其$H$的含量相关,根据反应$C_xH_yO_z+(x+\frac{y}{4}-\frac{z}{2})O_2\overset{点燃}=\!=\!=xCO_2+\frac{y}{2}H_2O$或$C_xH_y+(x+\frac{y}{4})O_2\overset{点燃}=\!=\!=xCO_2+\frac{y}{2}H_2O$,若两物质化学式中$H$元素质量分数相等或实验式相同,总质量一定时,其燃烧生成水的质量一定,与何种比例无关。乙烯$(C_2H_4)$和乙醇$(C_2H_6O)H$元素质量分数不相等,故①错误;丙烯$(C_3H_6)$和$2-$丁烯$(C_4H_8)$,实验式均为$CH_2$,故②正确;甲苯$(C_7H_8)$和邻二甲苯$(C_8H_{10})$实验式不相等,故③错误;甲醛$(CH_2O)$和葡萄糖$(C_6H_{12}O_6)$,其实验式均为$CH_2O$,符合,故④正确。综上,②④符合题意,选B。
5. [河北邯郸 2025 高一月考]通常将一定量的有机化合物充分燃烧转化为简单的无机化合物,根据产物的质量确定有机化合物的组成。下列是用燃烧法确定有机化合物分子式的常用装置。
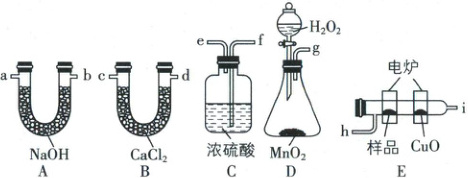
(1)使产生的 $O_{2}$ 从左到右流动,所选装置中各导管的正确连接顺序是
(2)C 装置中浓硫酸的作用是
(3)燃烧管中 $CuO$ 的作用是
(4)若有机物 A 中仅含有 C、H、O 三种元素,准确称取 $67g$ A,充分燃烧后,A 管质量增加 $88g$,B 管质量增加 $27g$,则该有机化合物的实验式为
(5)经测定 A 的相对分子质量为 $134$,又知 $1mol$ A 与足量的 $NaHCO_{3}$ 溶液充分反应可生成标准状况下 $44.8L CO_{2}$ 气体,$1mol$ A 与足量的 $Na$ 反应可生成 $1.5mol H_{2}$,则 A 分子中所含官能团的名称为

(1)使产生的 $O_{2}$ 从左到右流动,所选装置中各导管的正确连接顺序是
g→f→e→h→i→c(或d)→d(或c)→a(或b)→b(或a)
。(2)C 装置中浓硫酸的作用是
干燥氧气
。(3)燃烧管中 $CuO$ 的作用是
确保有机物中的碳元素全部转化为CO₂
。(4)若有机物 A 中仅含有 C、H、O 三种元素,准确称取 $67g$ A,充分燃烧后,A 管质量增加 $88g$,B 管质量增加 $27g$,则该有机化合物的实验式为
C₄H₆O₅
。若要确定 A 的分子式,还需要知道 A 的相对分子质量,测定物质的相对分子质量可以采用质谱
(填“质谱”或“红外光谱”)法。(5)经测定 A 的相对分子质量为 $134$,又知 $1mol$ A 与足量的 $NaHCO_{3}$ 溶液充分反应可生成标准状况下 $44.8L CO_{2}$ 气体,$1mol$ A 与足量的 $Na$ 反应可生成 $1.5mol H_{2}$,则 A 分子中所含官能团的名称为
羧基、羟基
。
答案:
5.
(1)$g\to f\to e\to h\to i\to c$(或$d)\to d$(或$c)\to a$(或$b)\to b$(或$a)$
(2)干燥氧气
(3)确保有机物中的碳元素全部转化为$CO_2$
(4)$C_4H_6O_5$ 质谱
(5)羧基、羟基
思路导引 测定一定质量的有机物完全燃烧时生成$CO_2$和$H_2O$的质量,为减少误差,将制得的$O_2$通入有机物中要先除杂(主要是除$H_2O$),故用$D$制得$O_2$后先用$C$干燥,再通人$E$中进行有机物的燃烧反应,$NaOH$能同时吸收$H_2O$和$CO_2$,则先用$B$来吸收水,测定生成水的质量,然后用$A$来吸收二氧化碳,测定生成二氧化碳的质量。为防止实验过程中有机物不完全燃烧产生$CO$,用$E$中$CuO$将可能生成的$CO$转化为$CO_2$。
【解析】
(1)由实验原理可知,产生的$O_2$从左到右流动过程中,各导管的正确连接顺序是$g\to f\to e\to h\to i\to c$(或$d)\to d$(或$c)\to a$(或$b)\to b$(或$a)$。
(2)$C$中浓硫酸可干燥氧气,防止影响水蒸气质量测定。
(3)燃烧管中$CuO$可与有机物不完全燃烧产生的$CO$反应生成$CO_2$,确保有机物中的碳元素全部转化为$CO_2$。
(4)$A$管增加的质量$88\ g$为生成的二氧化碳的质量,则$n(C)=n(CO_2)=\frac{88\ g}{44\ g· mol^{-1}}=2\ mol$,$67\ g\ A$中$m(C)=2\ mol×12\ g· mol^{-1}=24\ g$,$B$管增加的质量$27\ g$为生成的水的质量,$H$的物质的量$n(H)=2×\frac{27\ g}{18\ g· mol^{-1}}=3\ mol$,$67\ g\ A$中$m(H)=3\ mol×1\ g· mol^{-1}=3\ g$,有机物$A$中仅含有$C$、$H$、$O$三种元素,则$67\ g\ A$中$m(O)=67\ g-24\ g-3\ g=40\ g$,$n(O)=\frac{40\ g}{16\ g· mol^{-1}}=2.5\ mol$,则$n(C):n(H):n(O)=2\ mol:3\ mol:2.5\ mol=4:6:5$,故有机物的实验式为$C_4H_6O_5$。用质谱法可测定该有机物的相对分子质量。
(5)有机物的实验式为$C_4H_6O_5$,经测定$A$的相对分子质量为$134$,则$A$的分子式为$C_4H_6O_5$,又知$1\ mol\ A$与足量的$NaHCO_3$溶液充分反应可生成标准状况下$44.8\ L\ CO_2$气体,$n(CO_2)=\frac{44.8\ L}{22.4\ L· mol^{-1}}=2\ mol$,则$1$个$A$分子含有$2$个羧基;$1\ mol\ A$与足量的$Na$反应可生成$1.5\ mol\ H_2$,则$1$个$A$分子含有$2$个羧基和$1$个羟基。
(1)$g\to f\to e\to h\to i\to c$(或$d)\to d$(或$c)\to a$(或$b)\to b$(或$a)$
(2)干燥氧气
(3)确保有机物中的碳元素全部转化为$CO_2$
(4)$C_4H_6O_5$ 质谱
(5)羧基、羟基
思路导引 测定一定质量的有机物完全燃烧时生成$CO_2$和$H_2O$的质量,为减少误差,将制得的$O_2$通入有机物中要先除杂(主要是除$H_2O$),故用$D$制得$O_2$后先用$C$干燥,再通人$E$中进行有机物的燃烧反应,$NaOH$能同时吸收$H_2O$和$CO_2$,则先用$B$来吸收水,测定生成水的质量,然后用$A$来吸收二氧化碳,测定生成二氧化碳的质量。为防止实验过程中有机物不完全燃烧产生$CO$,用$E$中$CuO$将可能生成的$CO$转化为$CO_2$。
【解析】
(1)由实验原理可知,产生的$O_2$从左到右流动过程中,各导管的正确连接顺序是$g\to f\to e\to h\to i\to c$(或$d)\to d$(或$c)\to a$(或$b)\to b$(或$a)$。
(2)$C$中浓硫酸可干燥氧气,防止影响水蒸气质量测定。
(3)燃烧管中$CuO$可与有机物不完全燃烧产生的$CO$反应生成$CO_2$,确保有机物中的碳元素全部转化为$CO_2$。
(4)$A$管增加的质量$88\ g$为生成的二氧化碳的质量,则$n(C)=n(CO_2)=\frac{88\ g}{44\ g· mol^{-1}}=2\ mol$,$67\ g\ A$中$m(C)=2\ mol×12\ g· mol^{-1}=24\ g$,$B$管增加的质量$27\ g$为生成的水的质量,$H$的物质的量$n(H)=2×\frac{27\ g}{18\ g· mol^{-1}}=3\ mol$,$67\ g\ A$中$m(H)=3\ mol×1\ g· mol^{-1}=3\ g$,有机物$A$中仅含有$C$、$H$、$O$三种元素,则$67\ g\ A$中$m(O)=67\ g-24\ g-3\ g=40\ g$,$n(O)=\frac{40\ g}{16\ g· mol^{-1}}=2.5\ mol$,则$n(C):n(H):n(O)=2\ mol:3\ mol:2.5\ mol=4:6:5$,故有机物的实验式为$C_4H_6O_5$。用质谱法可测定该有机物的相对分子质量。
(5)有机物的实验式为$C_4H_6O_5$,经测定$A$的相对分子质量为$134$,则$A$的分子式为$C_4H_6O_5$,又知$1\ mol\ A$与足量的$NaHCO_3$溶液充分反应可生成标准状况下$44.8\ L\ CO_2$气体,$n(CO_2)=\frac{44.8\ L}{22.4\ L· mol^{-1}}=2\ mol$,则$1$个$A$分子含有$2$个羧基;$1\ mol\ A$与足量的$Na$反应可生成$1.5\ mol\ H_2$,则$1$个$A$分子含有$2$个羧基和$1$个羟基。
查看更多完整答案,请扫码查看


