2026年高中必刷题高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高中必刷题高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第32页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1. [安徽师大附中2024高一月考]下列变化中,属于放热反应的是(
①液氮汽化 ②氢氧化钠固体溶于水 ③氢氧化钠溶液与盐酸反应 ④KMnO₄分解制O₂ ⑤Ba(OH)₂·8H₂O晶体与NH₄Cl晶体混合 ⑥氢气在氧气中燃烧 ⑦CO₂ + C $\xlongequal{高温}$ 2CO ⑧生石灰和水反应生成熟石灰 ⑨钠块投入水中 ⑩锌与盐酸反应
A.①②③⑥⑦⑧⑨
B.①②⑥⑧⑨⑩
C.③⑥⑧⑨⑩
D.③④⑤⑧⑨⑩
C
)①液氮汽化 ②氢氧化钠固体溶于水 ③氢氧化钠溶液与盐酸反应 ④KMnO₄分解制O₂ ⑤Ba(OH)₂·8H₂O晶体与NH₄Cl晶体混合 ⑥氢气在氧气中燃烧 ⑦CO₂ + C $\xlongequal{高温}$ 2CO ⑧生石灰和水反应生成熟石灰 ⑨钠块投入水中 ⑩锌与盐酸反应
A.①②③⑥⑦⑧⑨
B.①②⑥⑧⑨⑩
C.③⑥⑧⑨⑩
D.③④⑤⑧⑨⑩
答案:
1.C [解析]液氮汽化是物理变化不是化学变化,①错误;氢氧化钠固体溶于水是物理变化不是化学变化,②错误;氢氧化钠溶液和盐酸的反应为酸碱中和反应,属于放热反应,③正确;高锰酸钾分解制取氧气,属于吸热反应,④错误;$\mathrm{Ba(OH)_2· 8H_2O}$晶体和氯化铵晶体的反应为吸热反应,⑤错误;氢气在氧气中燃烧放热,⑥正确;二氧化碳与C在高温下反应生成一氧化碳,属于吸热反应,⑦错误;生石灰与水反应生成熟石灰,属于放热反应,⑧正确;钠块投入水中,钠与水反应生成氢氧化钠和氢气,属于放热反应,⑨正确;锌与盐酸的反应为放热反应,⑩正确;故属于放热反应的是③⑥⑧⑨⑩,选C。
2. [陕西西安2025期中联考]下列反应的能量变化规律与图示相符的是(
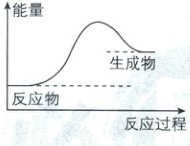
①氯化铵分解 ②镁条溶于稀盐酸 ③盐酸与碳酸氢钠固体反应 ④氢氧化钡与氯化铵反应 ⑤氢气在氯气中燃烧 ⑥硫酸和氢氧化钡溶液反应
A.①②⑤
B.①③④
C.③④⑤
D.②④⑥
B
)
①氯化铵分解 ②镁条溶于稀盐酸 ③盐酸与碳酸氢钠固体反应 ④氢氧化钡与氯化铵反应 ⑤氢气在氯气中燃烧 ⑥硫酸和氢氧化钡溶液反应
A.①②⑤
B.①③④
C.③④⑤
D.②④⑥
答案:
2.B [解析]如图所示,反应物的总能量低于生成物的总能量,则反应为吸热反应。①氯化铵分解为吸热反应,符合题意;②镁条溶于稀盐酸,发生放热反应,不符合题意;③盐酸与碳酸氢钠的反应为吸热反应,符合题意;④氢氧化钡与氯化铵的反应为吸热反应,符合题意;⑤氢气在氯气中燃烧,属于放热反应,不符合题意;⑥硫酸和氢氧化钡溶液的反应为放热反应,不符合题意。B正确。
3. [北京人大附中2025高一期中]用如下两种方法探究Na₂O₂与水反应的热效应,实验时发现Ⅱ烧杯中导管有气泡冒出。
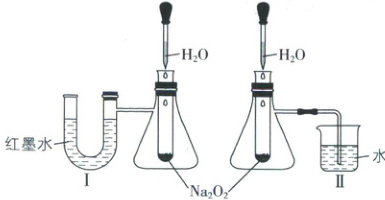
下列说法错误的是(
A.Ⅱ中气泡是锥形瓶内气压增大造成的
B.Ⅱ中气泡是Na₂O₂与水反应生成氧气造成的
C.若将温度计伸入试管,会观察到温度示数升高
D.预测实验时Ⅰ中U形管右侧液面下降

下列说法错误的是(
B
)A.Ⅱ中气泡是锥形瓶内气压增大造成的
B.Ⅱ中气泡是Na₂O₂与水反应生成氧气造成的
C.若将温度计伸入试管,会观察到温度示数升高
D.预测实验时Ⅰ中U形管右侧液面下降
答案:
3.B [解析]装置Ⅰ可通过U形管中红墨水液面的变化判断$\mathrm{Na_2O_2}$与水反应的热效应,装置Ⅱ可通过烧杯中是否产生气泡判断$\mathrm{Na_2O_2}$与水反应的热效应。Ⅱ中产生气泡是因为$\mathrm{Na_2O_2}$与水反应放热,使锥形瓶内气压增大,A正确;$\mathrm{Na_2O_2}$与水反应生成的氧气无法进入锥形瓶,B错误;$\mathrm{Na_2O_2}$与水的反应为放热反应,若将温度计伸入试管,会观察到温度示数升高,C正确;$\mathrm{Na_2O_2}$与水的反应为放热反应,使锥形瓶内压强增大,挤压U形管中的液体,故实验时Ⅰ中U形管右侧液面下降,左侧升高,D正确。
4. 下列说法正确的是(
A.化学键的断裂和形成是化学反应能量变化的主要原因
B.伴有能量变化的物质变化过程都是化学变化
C.在一个确定的化学反应中,反应物的总能量与生成物的总能量一定相同
D.在一个确定的化学反应中,反应物的总能量总是高于生成物的总能量
A
)A.化学键的断裂和形成是化学反应能量变化的主要原因
B.伴有能量变化的物质变化过程都是化学变化
C.在一个确定的化学反应中,反应物的总能量与生成物的总能量一定相同
D.在一个确定的化学反应中,反应物的总能量总是高于生成物的总能量
答案:
4.A [解析]化学反应过程中,反应物的化学键断裂要吸收能量,而生成物的化学键形成要放出能量,所以化学键的断裂和形成是化学反应能量变化的主要原因,A正确;伴有能量变化的物质变化过程不一定是化学变化,如液态水吸热形成水蒸气的过程属于物理变化,B错误;在一个确定的化学反应中,必定伴随着能量的变化,即反应物的总能量与生成物的总能量不可能相同,C错误;在一个确定的化学反应中,放热反应的反应物总能量高于生成物总能量,吸热反应的反应物总能量低于生成物总能量,D错误。
易错警示
(1)化学反应的本质是旧化学键断裂和新化学键形成,任何化学反应都具有热效应。
(2)不能根据反应条件判断反应是放热还是吸热,需要加热才能进行的反应不一定是吸热反应,不需要加热就能进行的反应也不一定是放热反应。
(3)有能量变化的物质转化过程不一定是发生放热反应或吸热反应,如液态水变成冰放热,但不属于放热反应。物质发生三态变化时,能量的变化:固态$\xrightarrow{吸热或放热}$液态$\xrightarrow{吸热或放热}$气态。
易错警示
(1)化学反应的本质是旧化学键断裂和新化学键形成,任何化学反应都具有热效应。
(2)不能根据反应条件判断反应是放热还是吸热,需要加热才能进行的反应不一定是吸热反应,不需要加热就能进行的反应也不一定是放热反应。
(3)有能量变化的物质转化过程不一定是发生放热反应或吸热反应,如液态水变成冰放热,但不属于放热反应。物质发生三态变化时,能量的变化:固态$\xrightarrow{吸热或放热}$液态$\xrightarrow{吸热或放热}$气态。
5. [湖南名校2025高一期中联考]氮氧化物是造成光化学烟雾的主要气体,含NO的烟气需要经过处理后才能排放。科学家研制了使用氢气还原NO的方法:2NO(g) + 2H₂(g) $\xrightleftharpoons{}$ N₂(g) + 2H₂O(g)。已知:1mol NO完全反应时放热333.0kJ,有关化学键键能(断开1mol化学键所吸收的能量或者形成1mol化学键所释放的能量)的数据如表所示。

下列说法正确的是(
A.将2mol NO和2mol H₂投入容器中发生该反应,可放热666.0kJ
B.相同状态的NO比N₂稳定
C.x的数值为630
D.当反应生成的水为1mol H₂O(l)时放热小于333.0kJ

下列说法正确的是(
C
)A.将2mol NO和2mol H₂投入容器中发生该反应,可放热666.0kJ
B.相同状态的NO比N₂稳定
C.x的数值为630
D.当反应生成的水为1mol H₂O(l)时放热小于333.0kJ
答案:
5.C [解析]该反应为可逆反应,投入的2molNO无法完全消耗,实际放热小于666.0kJ,A错误;根据$\Delta H$计算:断键吸收的总能量$(2x\ kJ+2×436\ kJ)-$成键放出的总能量$(946\ kJ+4×463\ kJ)=-666\ kJ$,解得$x = 630$,$\mathrm{N≡N}$键能$(946\ kJ·mol^{-1})$远高于NO中化学键的键能$(630\ kJ·mol^{-1})$,键能越大越稳定,所以$\mathrm{N_2}$更稳定,B错误、C正确;$\mathrm{H_2O(l)}$比$\mathrm{H_2O(g)}$能量更低,生成液态水时放热更多,应大于333.0kJ,D错误。
易错点:判断能量大小时,要关注反应物和生成物的状态。
易错点:判断能量大小时,要关注反应物和生成物的状态。
查看更多完整答案,请扫码查看


