2026年高中必刷题高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高中必刷题高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第70页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1. 教材变式[山西部分学校 2025 高一联考]古代典籍中记述的酿酒方法与近代酿酒法相似。以下说法错误的是(
A.在实验室可以用溴水鉴别乙醇和乙酸
B.乙醇是很好的溶剂,故可以用乙醇来提取某些中药中的有效成分
C.用谷物还可以酿醋,醋酸是酿造得到的酒精在醋酸菌的作用下,被空气氧化而成的
D.6.0g 乙酸与足量钠完全反应,得到 1.12L 氢气(标准状况)
A
)A.在实验室可以用溴水鉴别乙醇和乙酸
B.乙醇是很好的溶剂,故可以用乙醇来提取某些中药中的有效成分
C.用谷物还可以酿醋,醋酸是酿造得到的酒精在醋酸菌的作用下,被空气氧化而成的
D.6.0g 乙酸与足量钠完全反应,得到 1.12L 氢气(标准状况)
答案:
1.A
教材变式本题是教材P82练习与应用第4题的变式题,教材考查了鉴别乙醇和乙酸的试剂判断,变式题则加入了乙酸的化学性质、用途以及乙醇氧化至乙酸的过程考查。
[解析]乙醇和乙酸均不能与溴水反应,且均可与溴水互溶,溶液均不分层,现象相同,无法用溴水鉴别乙酸和乙醇,A错误;乙醇是很好的溶剂,故可以用乙醇来提取某些中药中的有效成分,B正确;醋酸是酿造得到的酒精在醋酸菌的作用下,被空气氧化而成的,C正确;6.0g乙酸的物质的量$n(CH_3COOH)=\frac{m(CH_3COOH)}{M(CH_3COOH)}=\frac{6.0g}{60g· mol^{-1}}=0.1mol$,与足量钠完全反应,得到氢气的物质的量为0.05mol,所以标准状况下$H_2$的体积为1.12L,D正确。
教材变式本题是教材P82练习与应用第4题的变式题,教材考查了鉴别乙醇和乙酸的试剂判断,变式题则加入了乙酸的化学性质、用途以及乙醇氧化至乙酸的过程考查。
[解析]乙醇和乙酸均不能与溴水反应,且均可与溴水互溶,溶液均不分层,现象相同,无法用溴水鉴别乙酸和乙醇,A错误;乙醇是很好的溶剂,故可以用乙醇来提取某些中药中的有效成分,B正确;醋酸是酿造得到的酒精在醋酸菌的作用下,被空气氧化而成的,C正确;6.0g乙酸的物质的量$n(CH_3COOH)=\frac{m(CH_3COOH)}{M(CH_3COOH)}=\frac{6.0g}{60g· mol^{-1}}=0.1mol$,与足量钠完全反应,得到氢气的物质的量为0.05mol,所以标准状况下$H_2$的体积为1.12L,D正确。
2. 下列关于乙酸的说法中,正确的有(
①乙酸分子里有四个氢原子,所以它不是一元酸
②除去乙酸乙酯中残留的乙酸,有效方法是用过量饱和碳酸钠溶液洗涤后分液
③1mol 乙酸与足量乙醇在浓硫酸作用下加热,可生成 88g 乙酸乙酯
④乙酸是一种重要的有机酸,常温下乙酸是有刺激性气味的液体
⑤乙酸能够与金属钠反应产生氢气
⑥乙酸的酸性比碳酸弱
⑦食醋中含有乙酸,乙酸可由乙醇氧化得到
⑧乙酸易溶于水和乙醇,其水溶液能导电
A.3 个
B.6 个
C.4 个
D.5 个
D
)①乙酸分子里有四个氢原子,所以它不是一元酸
②除去乙酸乙酯中残留的乙酸,有效方法是用过量饱和碳酸钠溶液洗涤后分液
③1mol 乙酸与足量乙醇在浓硫酸作用下加热,可生成 88g 乙酸乙酯
④乙酸是一种重要的有机酸,常温下乙酸是有刺激性气味的液体
⑤乙酸能够与金属钠反应产生氢气
⑥乙酸的酸性比碳酸弱
⑦食醋中含有乙酸,乙酸可由乙醇氧化得到
⑧乙酸易溶于水和乙醇,其水溶液能导电
A.3 个
B.6 个
C.4 个
D.5 个
答案:
2.D [解析]乙酸的结构简式为$CH_3COOH$,乙酸分子中有四个氢原子,但乙酸只能电离出一个氢离子,因此乙酸属于一元酸,①错误;乙酸乙酯是不溶于水的油状液体,密度小于水,除去乙酸乙酯中混有的乙酸,常用饱和碳酸钠溶液,碳酸钠能与乙酸反应,同时降低乙酸乙酯在溶液中的溶解度,然后采用分液的方法进行分离,②正确;乙酸与乙醇发生酯化反应,该反应为可逆反应,不能进行到底,因此1mol乙酸与足量的乙醇反应,生成的乙酸乙酯质量小于88g,③错误;乙酸是一种有机酸,常温下乙酸是具有强烈刺激性气味的无色液体,④正确;乙酸能与金属钠反应生成乙酸钠和氢气,⑤正确;乙酸的酸性强于碳酸,⑥错误;食醋中含有乙酸,乙酸可以由乙醇经过氧化得到,⑦正确;乙酸易溶于水和乙醇,乙酸属于电解质,其水溶液能导电,⑧正确。综上所述,②④⑤⑦⑧正确,选D。
3. [河北衡水 2025 高一月考]乙酸分子的结构式如图所示,下列关于断键位置叙述正确的是(
①乙酸在水溶液中电离时,断裂 a 键
②乙酸与乙醇发生酯化反应时,断裂 b 键

③在红磷存在时,Br₂与 CH₃COOH 反应的化学方程式为$ CH₃COOH + Br₂\xrightarrow{红磷}CH₂Br—COOH + HBr,$乙酸在该反应中断裂 c 键
④一定条件下,2mol 乙酸分子生成 1mol 乙酸酐的方程式可表示为$ 2CH₃COOH\xrightarrow{一定条件}$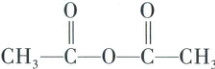
$ + H₂O,$乙酸在该反应中分别断裂 a、b 键
A.①②③
B.①③④
C.②③④
D.①②③④
D
)①乙酸在水溶液中电离时,断裂 a 键
②乙酸与乙醇发生酯化反应时,断裂 b 键

③在红磷存在时,Br₂与 CH₃COOH 反应的化学方程式为$ CH₃COOH + Br₂\xrightarrow{红磷}CH₂Br—COOH + HBr,$乙酸在该反应中断裂 c 键
④一定条件下,2mol 乙酸分子生成 1mol 乙酸酐的方程式可表示为$ 2CH₃COOH\xrightarrow{一定条件}$
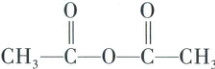
$ + H₂O,$乙酸在该反应中分别断裂 a、b 键
A.①②③
B.①③④
C.②③④
D.①②③④
答案:
3.D [解析]乙酸在水溶液中电离时,产生$CH_3COO^-$和$H^+$,断裂a键,①正确;乙酸与乙醇发生酯化反应时,遵循“酸脱羟基醇脱氢”的原则,乙酸断裂b键,②正确;对比$CH_3COOH$和$CH_2Br—COOH$可知,乙酸在题给反应中断裂c键,③正确;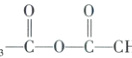
对比$CH_3COOH$和$CH_3—C(=O)—O—C(=O)—CH_3$可知,在题给反应中一分子乙酸断裂a键,一分子乙酸断裂b键,④正确。选D。
3.D [解析]乙酸在水溶液中电离时,产生$CH_3COO^-$和$H^+$,断裂a键,①正确;乙酸与乙醇发生酯化反应时,遵循“酸脱羟基醇脱氢”的原则,乙酸断裂b键,②正确;对比$CH_3COOH$和$CH_2Br—COOH$可知,乙酸在题给反应中断裂c键,③正确;

对比$CH_3COOH$和$CH_3—C(=O)—O—C(=O)—CH_3$可知,在题给反应中一分子乙酸断裂a键,一分子乙酸断裂b键,④正确。选D。
4. 下列关于酯化反应叙述不正确的是(
A.浓硫酸在酯化反应中只起催化剂的作用
B.酯化反应是有限度的
C.酯化反应的机理是酸脱去羟基,醇脱去羟基上的氢原子
D.酯化反应属于取代反应
A
)A.浓硫酸在酯化反应中只起催化剂的作用
B.酯化反应是有限度的
C.酯化反应的机理是酸脱去羟基,醇脱去羟基上的氢原子
D.酯化反应属于取代反应
答案:
4.A [解析]浓硫酸在酯化反应中作催化剂和吸水剂,A错误;酯化反应属于可逆反应,是有限度的,B正确;酯化反应的机理是酸脱去羟基,醇脱去羟基上的氢原子,C正确;酯化反应属于取代反应,D正确。
5. [广西钦州四中 2025 高一月考]下列制取乙酸乙酯的实验原理与装置能达到实验目的的是(
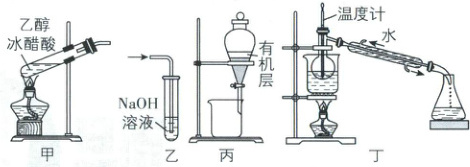
A.装置甲:制备乙酸乙酯
B.装置乙:收集乙酸乙酯并除去其中的乙醇和乙酸
C.装置丙:分离有机层和水层
D.装置丁:蒸馏得到乙酸乙酯
C
)
A.装置甲:制备乙酸乙酯
B.装置乙:收集乙酸乙酯并除去其中的乙醇和乙酸
C.装置丙:分离有机层和水层
D.装置丁:蒸馏得到乙酸乙酯
答案:
5.C [解析]乙醇、冰醋酸在浓硫酸催化作用下加热才会反应生成乙酸乙酯,且实验时应加入少量碎瓷片防止暴沸,A错误;乙酸乙酯在氢氧化钠溶液中会发生水解,应用饱和碳酸钠溶液,且未防止倒吸,应将导管口置于液面上方,B错误;乙酸乙酯密度比水小,难溶于水,有机层在上层,可以用分液的方法分离有机层和水层,C正确;冷凝水应下进上出,使冷凝更充分,且温度计水银球应与蒸馏烧瓶支管口下沿处齐平,D错误。
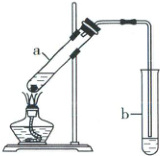
6. “酒是陈的香”是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室中我们也可以用图示装置制取乙酸乙酯。请回答下列问题:
(1)该反应的化学方程式是
(2)浓硫酸的作用是
(3)试管 a 中需要加入浓硫酸、乙酸各 2mL,乙醇 3mL,正确的加入顺序为
A. 浓硫酸、乙醇、乙酸
B. 浓硫酸、乙酸、乙醇
C. 乙醇、浓硫酸、乙酸
(4)为了防止试管 a 中的液体在实验时发生暴沸,在加热试管前应采取的措施是
(5)试管 b 中盛有饱和的碳酸钠溶液,其作用是
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是
(1)该反应的化学方程式是
$CH_3COOH+CH_3CH_2OH\underset{\triangle}{\overset{浓硫酸}{\rightleftharpoons}}CH_3COOCH_2CH_3+H_2O$
。(2)浓硫酸的作用是
作催化剂
,作吸水剂
。(3)试管 a 中需要加入浓硫酸、乙酸各 2mL,乙醇 3mL,正确的加入顺序为
C
(填序号)。A. 浓硫酸、乙醇、乙酸
B. 浓硫酸、乙酸、乙醇
C. 乙醇、浓硫酸、乙酸
(4)为了防止试管 a 中的液体在实验时发生暴沸,在加热试管前应采取的措施是
加入沸石或碎瓷片
。(5)试管 b 中盛有饱和的碳酸钠溶液,其作用是
①溶解挥发出来的乙醇;②吸收挥发出来的乙酸;③减少乙酸乙酯的溶解,便于分离和收集乙酸乙酯
。(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是
分液
。
答案:
6.
(1)$CH_3COOH+CH_3CH_2OH\underset{\triangle}{\overset{浓硫酸}{\rightleftharpoons}}CH_3COOCH_2CH_3+H_2O$
(2)作催化剂 作吸水剂
(3)C
(4)加入沸石或碎瓷片
(5)①溶解挥发出来的乙醇;②吸收挥发出来的乙酸;③减少乙酸乙酯的溶解,便于分离和收集乙酸乙酯
(6)分液
[解析]
(1)乙酸和乙醇在浓硫酸和加热条件下发生酯化反应生成乙酸乙酯和水,该反应的化学方程式是$CH_3COOH+CH_3CH_2OH\underset{\triangle}{\overset{浓硫酸}{\rightleftharpoons}}CH_3COOCH_2CH_3+H_2O$。
(2)乙酸、乙醇发生酯化反应需要浓硫酸作催化剂,酯化反应可逆,而浓硫酸具有吸水性,浓硫酸吸水有利于反应正向进行,即浓硫酸同时作催化剂和吸水剂。
(3)浓硫酸密度大,稀释时放热,而乙醇、乙酸均易挥发,加入试剂的顺序是先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却至室温后再加入乙酸,选C。
(4)为了防止试管a中的液体在实验时发生暴沸,在加热试管前应加入沸石或碎瓷片。
(5)试管b中盛有饱和的碳酸钠溶液,其作用是①溶解挥发出来的乙醇;②吸收挥发出来的乙酸;③减少乙酸乙酯的溶解,便于分离和收集乙酸乙酯。
(6)乙酸乙酯难溶于碳酸钠溶液,而乙醇、乙酸可溶于水或可以和碳酸钠反应,将试管中混合物静置后,会出现分层现象,故用分液的方法可分离出乙酸乙酯。
关键点拨:液体加热的实验一般需要加入沸石或碎瓷片,以防止暴沸。气体吸收装置一般需要注意防止倒吸。
(1)$CH_3COOH+CH_3CH_2OH\underset{\triangle}{\overset{浓硫酸}{\rightleftharpoons}}CH_3COOCH_2CH_3+H_2O$
(2)作催化剂 作吸水剂
(3)C
(4)加入沸石或碎瓷片
(5)①溶解挥发出来的乙醇;②吸收挥发出来的乙酸;③减少乙酸乙酯的溶解,便于分离和收集乙酸乙酯
(6)分液
[解析]
(1)乙酸和乙醇在浓硫酸和加热条件下发生酯化反应生成乙酸乙酯和水,该反应的化学方程式是$CH_3COOH+CH_3CH_2OH\underset{\triangle}{\overset{浓硫酸}{\rightleftharpoons}}CH_3COOCH_2CH_3+H_2O$。
(2)乙酸、乙醇发生酯化反应需要浓硫酸作催化剂,酯化反应可逆,而浓硫酸具有吸水性,浓硫酸吸水有利于反应正向进行,即浓硫酸同时作催化剂和吸水剂。
(3)浓硫酸密度大,稀释时放热,而乙醇、乙酸均易挥发,加入试剂的顺序是先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却至室温后再加入乙酸,选C。
(4)为了防止试管a中的液体在实验时发生暴沸,在加热试管前应加入沸石或碎瓷片。
(5)试管b中盛有饱和的碳酸钠溶液,其作用是①溶解挥发出来的乙醇;②吸收挥发出来的乙酸;③减少乙酸乙酯的溶解,便于分离和收集乙酸乙酯。
(6)乙酸乙酯难溶于碳酸钠溶液,而乙醇、乙酸可溶于水或可以和碳酸钠反应,将试管中混合物静置后,会出现分层现象,故用分液的方法可分离出乙酸乙酯。
关键点拨:液体加热的实验一般需要加入沸石或碎瓷片,以防止暴沸。气体吸收装置一般需要注意防止倒吸。
查看更多完整答案,请扫码查看


