2026年高中必刷题高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高中必刷题高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第5页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1. [甘肃酒泉四校2025高一期中联考]工业上制硫酸涉及如图三个装置。下列有关说法错误的是(
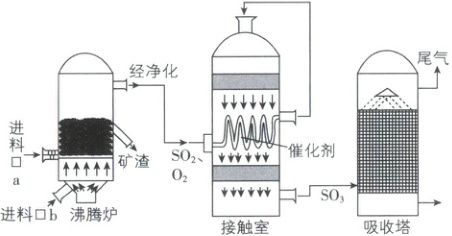
A.硫在过量的空气中燃烧生成SO₃
B.接触室中的反应主要为2SO₂ + O₂ $\xlongequal[\triangle]{催化剂}$ 2SO₃
C.吸收塔中不用水吸收SO₃的原因是SO₃溶于水时放出大量的热,从而形成酸雾,降低吸收效率
D.在浓硫酸使蔗糖变黑面包的实验中,浓硫酸表现脱水性和氧化性
A
)
A.硫在过量的空气中燃烧生成SO₃
B.接触室中的反应主要为2SO₂ + O₂ $\xlongequal[\triangle]{催化剂}$ 2SO₃
C.吸收塔中不用水吸收SO₃的原因是SO₃溶于水时放出大量的热,从而形成酸雾,降低吸收效率
D.在浓硫酸使蔗糖变黑面包的实验中,浓硫酸表现脱水性和氧化性
答案:
1.A 【解析】硫在过量的空气中燃烧生成SO₂,无法直接生成SO₃,
易错点:硫在纯氧条件下燃烧的产物也是SO₂
A错误;接触室内发生的反应为二氧化硫与氧气发生催化氧化反应生成三氧化硫,该反应为可逆反应,反应的化学方程式为$2SO₂ + O₂ \xrightarrow[△]{催化剂} 2SO₃,$B正确;三氧化硫与水反应放出大量的热,若用蒸馏水吸收三氧化硫会形成酸雾,降低吸收效率,C正确;浓硫酸使蔗糖变黑面包实验中,浓硫酸使蔗糖中的H、O原子以2:1的比例脱去,表现脱水性,同时有刺激性气味气体产生,为碳与浓硫酸发生氧化还原反应生成的二氧化硫气体,体现浓硫酸的氧化性,D正确。
易错点:硫在纯氧条件下燃烧的产物也是SO₂
A错误;接触室内发生的反应为二氧化硫与氧气发生催化氧化反应生成三氧化硫,该反应为可逆反应,反应的化学方程式为$2SO₂ + O₂ \xrightarrow[△]{催化剂} 2SO₃,$B正确;三氧化硫与水反应放出大量的热,若用蒸馏水吸收三氧化硫会形成酸雾,降低吸收效率,C正确;浓硫酸使蔗糖变黑面包实验中,浓硫酸使蔗糖中的H、O原子以2:1的比例脱去,表现脱水性,同时有刺激性气味气体产生,为碳与浓硫酸发生氧化还原反应生成的二氧化硫气体,体现浓硫酸的氧化性,D正确。
2. [广东广州2025高一期中]硫酸是重要的化工原料,工业制硫酸的原理示意图如下。
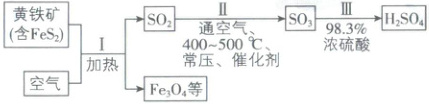
(1)FeS₂中Fe为+2价,S的化合价为
(2)将Ⅰ中反应的化学方程式补充完整:
$□$FeS₂ + $□$______ $\xlongequal{\triangle}$ $□$Fe₃O₄ + $□$SO₂
若反应中消耗了1 mol FeS₂,则生成SO₂的物质的量为
(3)Ⅱ中反应的化学方程式为______。
(4)为避免制备硫酸时尾气中的SO₂污染环境,可使用尿素[CO(NH₂)₂]/H₂O₂溶液吸收尾气。
①将尿素/H₂O₂溶液吸收SO₂的化学方程式补充完整:
SO₂ + CO(NH₂)₂ + H₂O₂ +
②使用尿素/H₂O₂溶液吸收SO₂,一般选择在50~70℃下进行。过高的温度会导致相同时间内的SO₂去除率下降,原因是______。

(1)FeS₂中Fe为+2价,S的化合价为
-1
。(2)将Ⅰ中反应的化学方程式补充完整:
$□$FeS₂ + $□$______ $\xlongequal{\triangle}$ $□$Fe₃O₄ + $□$SO₂
若反应中消耗了1 mol FeS₂,则生成SO₂的物质的量为
2 mol
。(3)Ⅱ中反应的化学方程式为______。
(4)为避免制备硫酸时尾气中的SO₂污染环境,可使用尿素[CO(NH₂)₂]/H₂O₂溶液吸收尾气。
①将尿素/H₂O₂溶液吸收SO₂的化学方程式补充完整:
SO₂ + CO(NH₂)₂ + H₂O₂ +
H₂O
$\xlongequal{}$ (NH₄)₂SO₄ + CO₂
②使用尿素/H₂O₂溶液吸收SO₂,一般选择在50~70℃下进行。过高的温度会导致相同时间内的SO₂去除率下降,原因是______。
答案:
2.
(1)-1
$(2)3FeS₂ + 8O₂ \xlongequal{△} Fe₃O₄ + 6SO₂ 2 mol$
$(3)2SO₂ + O₂ \xrightleftharpoons[400 - 500 ℃]{催化剂} 2SO₃$
(4)①SO₂ + CO(NH₂)₂ + H₂O + H₂O ══ (NH₄)₂SO₄ + CO₂
②温度过高,SO₂在溶液中的溶解度降低且H₂O₂分解速率大,浓度显著降低
(1)-1
$(2)3FeS₂ + 8O₂ \xlongequal{△} Fe₃O₄ + 6SO₂ 2 mol$
$(3)2SO₂ + O₂ \xrightleftharpoons[400 - 500 ℃]{催化剂} 2SO₃$
(4)①SO₂ + CO(NH₂)₂ + H₂O + H₂O ══ (NH₄)₂SO₄ + CO₂
②温度过高,SO₂在溶液中的溶解度降低且H₂O₂分解速率大,浓度显著降低
3. [河南新乡2024高一月考]在如图所示的实验装置中,实验开始一段时间后,对实验现象及结论的叙述均不正确的是(
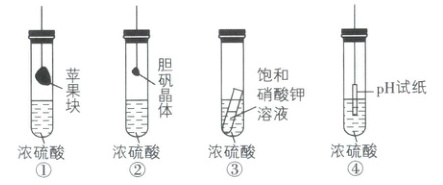

D
)

答案:
3.D 【解析】①中苹果块会干瘪,体现了浓硫酸的吸水性,A不符合题意;②中胆矾晶体失去结晶水后变白,体现了浓硫酸的吸水性,B不符合题意;③中小试管内有固体析出,体现了浓硫酸的吸水性,C不符合题意;④中pH试纸脱水炭化而变黑,体现了浓硫酸的脱水性,D符合题意。
关键点拨 本题考查浓硫酸的吸水性和脱水性。浓硫酸的吸水性很强,能从环境中吸收水分。KNO₃的饱和溶液中水分减少后会有固体析出。
关键点拨 本题考查浓硫酸的吸水性和脱水性。浓硫酸的吸水性很强,能从环境中吸收水分。KNO₃的饱和溶液中水分减少后会有固体析出。
4. 下列对浓硫酸的叙述正确的是(
A.常温下,浓硫酸与铁、铝不反应,所以铁制、铝制容器能盛放浓硫酸
B.浓硫酸具有强氧化性,SO₂、H₂、CO具有还原性,故浓硫酸不能干燥SO₂、H₂、CO
C.浓硫酸和铜片加热反应中铜是还原剂
D.浓硫酸与亚硫酸钠反应制取SO₂时,浓硫酸表现出强氧化性
C
)A.常温下,浓硫酸与铁、铝不反应,所以铁制、铝制容器能盛放浓硫酸
B.浓硫酸具有强氧化性,SO₂、H₂、CO具有还原性,故浓硫酸不能干燥SO₂、H₂、CO
C.浓硫酸和铜片加热反应中铜是还原剂
D.浓硫酸与亚硫酸钠反应制取SO₂时,浓硫酸表现出强氧化性
答案:
4.C 【解析】常温下,Fe、Al遇浓硫酸发生钝化,钝化过程中发生了化学反应,A错误;浓硫酸与SO₂、H₂、CO不反应,可以干燥SO₂、H₂、CO,B错误;铜与浓硫酸在加热条件下发生反应,部分H₂SO₄被还原,生成SO₂,作氧化剂,铜作还原剂,C正确;实验室中用浓硫酸与亚硫酸钠反应制取二氧化硫,其原理是用强酸制弱酸,因而在此反应中浓硫酸表现的是酸性,D错误。
查看更多完整答案,请扫码查看


