2026年高中必刷题高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高中必刷题高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第59页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1. [江苏连云港2024高一期末]碳原子成键的多样性是有机化合物种类繁多的原因之一,乙醇和二甲醚的结构式如图所示。下列关于两种物质的说法正确的是(
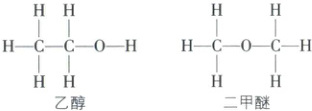
A.分子式不同
B.性质有差异的原因是分子结构不同
C.各1 mol分子中碳氧键(C—O)数目相同
D.各1 mol分子中共用电子对数目不同
B
)
A.分子式不同
B.性质有差异的原因是分子结构不同
C.各1 mol分子中碳氧键(C—O)数目相同
D.各1 mol分子中共用电子对数目不同
答案:
1.B [解析]由结构可知,二者分子式均为C₂H₆O,分子式相同,A错误;二者的结构不同,导致性质存在差异,B正确;1个乙醇分子中有一个碳氧键,1个二甲醚分子中有2个碳氧键,则各1mol分子中碳氧键(C—O)数目分别为Nₐ、2Nₐ,C错误;1mol乙醇、二甲醚分子中均有8mol共用电子对,数目相同,D错误。
2. [宁夏吴忠中学2025高一月考]将链状烷烃进行如图所示转化是近年来发现的石油绿色裂解方法,反应温度更低,且催化剂具有良好的选择性。下列说法不正确的是(
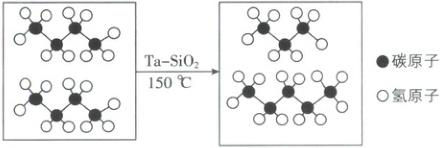
A.反应物与产物互为同系物
B.物质的量相同的3种烷烃,完全燃烧时戊烷消耗的氧气最多
C.3种烷烃在常压下沸点最高的是丙烷
D.质量相同的3种烷烃,完全燃烧时丙烷消耗的氧气最多
C
)
A.反应物与产物互为同系物
B.物质的量相同的3种烷烃,完全燃烧时戊烷消耗的氧气最多
C.3种烷烃在常压下沸点最高的是丙烷
D.质量相同的3种烷烃,完全燃烧时丙烷消耗的氧气最多
答案:
2.C [解析]反应物与产物分子式不同,但均属于饱和链烃,互为同系物,A正确;物质的量相同的烷烃,碳原子数越多,完全燃烧时消耗的氧气越多,因此完全燃烧时戊烷消耗的氧气最多,B正确;碳原子数越多,相对分子质量越大,分子间作用力越强,沸点越高,所以沸点由高到低的顺序是戊烷>丁烷>丙烷,C错误;烷烃中,H的质量分数越大,等质量的烷烃完全燃烧时消耗的氧气越多,故质量相同的3种烷烃,丙烷消耗的氧气最多,D正确。
方法技巧等质量的烷烃完全燃烧时的耗氧量规律
烷烃通式:CₙH₂ₙ₊₂(n为正整数)
由元素守恒可得,烷烃完全燃烧时,存在关系式:
C~O₂ H~$\frac{1}{4}$O₂
12g 1mol 1g $\frac{1}{4}$mol
则1gC元素消耗$\frac{1}{12}$molO₂,1gH元素消耗$\frac{1}{4}$molO₂,故等质量的烷烃完全燃烧时,烷烃中H元素质量分数越大,耗氧量越大。
烷烃中H元素质量分数w(H)=$\frac{2n+2}{14n+2}$=$\frac{n+1}{7n+1}$=$\frac{1}{7+\frac{6}{7n+1}}$,n越小,w(H)越大,等质量的烷烃完全燃烧时耗氧量越大。
方法技巧等质量的烷烃完全燃烧时的耗氧量规律
烷烃通式:CₙH₂ₙ₊₂(n为正整数)
由元素守恒可得,烷烃完全燃烧时,存在关系式:
C~O₂ H~$\frac{1}{4}$O₂
12g 1mol 1g $\frac{1}{4}$mol
则1gC元素消耗$\frac{1}{12}$molO₂,1gH元素消耗$\frac{1}{4}$molO₂,故等质量的烷烃完全燃烧时,烷烃中H元素质量分数越大,耗氧量越大。
烷烃中H元素质量分数w(H)=$\frac{2n+2}{14n+2}$=$\frac{n+1}{7n+1}$=$\frac{1}{7+\frac{6}{7n+1}}$,n越小,w(H)越大,等质量的烷烃完全燃烧时耗氧量越大。
3. [天津和平区2025高一期中]1 mol某链状烷烃在氧气中充分燃烧,需要消耗氧气246.4 L(标准状况下)。它在光照的条件下与氯气反应能生成四种不同的一氯代物,该烃的结构简式可能是(
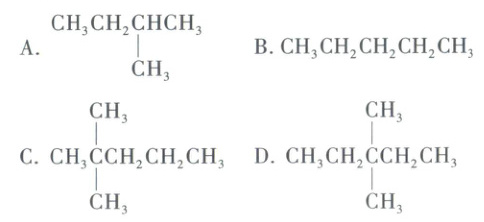
C
)
答案:
3.C
思路导引 1mol某链状烷烃在氧气中充分燃烧,需要消耗标准状况下氧气$\frac{246.4L}{22.4L·mol⁻¹}=11mol$,根据烷烃燃烧通式CₙH₂ₙ₊₂+$\frac{3n+1}{2}$O₂$\stackrel{点燃}{⇌}$nCO₂+(n+1)H₂O可知,$\frac{3n+1}{2}=11$,解得n=7。
思路导引 1mol某链状烷烃在氧气中充分燃烧,需要消耗标准状况下氧气$\frac{246.4L}{22.4L·mol⁻¹}=11mol$,根据烷烃燃烧通式CₙH₂ₙ₊₂+$\frac{3n+1}{2}$O₂$\stackrel{点燃}{⇌}$nCO₂+(n+1)H₂O可知,$\frac{3n+1}{2}=11$,解得n=7。
4. [浙江杭州2024高一期中]下列说法错误的是(
A.正戊烷和2-甲基丁烷互为同系物
B.某有机物在空气中充分燃烧后只生成CO₂和H₂O,该有机物可能是烃或烃的衍生物
C.医学上研究发现 具有抗癌作用,而
具有抗癌作用,而 没有抗癌作用,说明二者互为同分异构体,都是以Pt原子为中心的平面结构
没有抗癌作用,说明二者互为同分异构体,都是以Pt原子为中心的平面结构
D.C₅H₁₁Cl的同分异构体有8种
A
)A.正戊烷和2-甲基丁烷互为同系物
B.某有机物在空气中充分燃烧后只生成CO₂和H₂O,该有机物可能是烃或烃的衍生物
C.医学上研究发现
 具有抗癌作用,而
具有抗癌作用,而 没有抗癌作用,说明二者互为同分异构体,都是以Pt原子为中心的平面结构
没有抗癌作用,说明二者互为同分异构体,都是以Pt原子为中心的平面结构D.C₅H₁₁Cl的同分异构体有8种
答案:
4.A [解析]正戊烷和2−甲基丁烷的分子式相同,结构不同,互为同分异构体,A错误;某有机物在空气中充分燃烧后只生成CO₂和H₂O,该有机物中可能只含有碳和氢元素,也可能含有氧元素,则该有机物可能是烃或烃的衍生物,B正确;由题意知,两种物质的组成相同、分子式相同,性质不同,则 是不同的物质,所以二者均不是NH₃四面体结构,二者均是以Pt原子为中心的平面结构,互为同分异构体,C正确;C₅H₁₁Cl由戊基和氯原子构成,戊基的结构有8种,则C₅H₁₁Cl的同分异构体有8种,D正确。
是不同的物质,所以二者均不是NH₃四面体结构,二者均是以Pt原子为中心的平面结构,互为同分异构体,C正确;C₅H₁₁Cl由戊基和氯原子构成,戊基的结构有8种,则C₅H₁₁Cl的同分异构体有8种,D正确。
4.A [解析]正戊烷和2−甲基丁烷的分子式相同,结构不同,互为同分异构体,A错误;某有机物在空气中充分燃烧后只生成CO₂和H₂O,该有机物中可能只含有碳和氢元素,也可能含有氧元素,则该有机物可能是烃或烃的衍生物,B正确;由题意知,两种物质的组成相同、分子式相同,性质不同,则
 是不同的物质,所以二者均不是NH₃四面体结构,二者均是以Pt原子为中心的平面结构,互为同分异构体,C正确;C₅H₁₁Cl由戊基和氯原子构成,戊基的结构有8种,则C₅H₁₁Cl的同分异构体有8种,D正确。
是不同的物质,所以二者均不是NH₃四面体结构,二者均是以Pt原子为中心的平面结构,互为同分异构体,C正确;C₅H₁₁Cl由戊基和氯原子构成,戊基的结构有8种,则C₅H₁₁Cl的同分异构体有8种,D正确。 5. [广西柳州2025高一期末]常温下,乙烷分子中的两个甲基可以绕C—C键自由旋转,理论上乙烷分子可以有多种构象,其中两种构象的能量关系如图所示,下列说法错误的是(
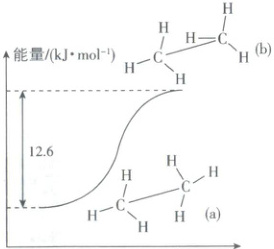
A.a分子比b分子稳定
B.乙烷分子中所有原子不在同一平面上
C.乙烷在光照条件下能与氯气发生反应生成多种有机物
D.1个a分子完全转化为b分子需要吸收12.6 kJ热量
D
)
A.a分子比b分子稳定
B.乙烷分子中所有原子不在同一平面上
C.乙烷在光照条件下能与氯气发生反应生成多种有机物
D.1个a分子完全转化为b分子需要吸收12.6 kJ热量
答案:
5.D [解析]a分子能量比b分子更低,更稳定,A正确;甲烷为正四面体结构,乙烷可视为CH₄上的一个H被甲基取代所得,分子中所有原子不在同一平面上,B正确;乙烷在光照条件下能与氯气发生取代反应生成多种有机物,如CH₃CH₂Cl、CH₃CHCl₂、CH₃CCl₃等,C正确;1mol a分子完全转化为1mol b分子吸收12.6kJ热量,D错误。
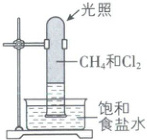
6. CH₄在光照条件下与Cl₂反应可得到各种氯代甲烷。取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气,并置于光亮处(如图)。回答下列问题:
(1)下列说法正确的是(填序号)。
A. 反应过程中试管内黄绿色逐渐变浅,试管壁上有油状液滴产生
B. 将该装置放在黑暗处,CH₄与Cl₂也能反应
C. 该实验发生了取代反应
D. CH₄和Cl₂完全反应后试管内液面上升,液体充满试管
(2)CH₄氯代为自由基(带有单电子的原子或原子团,如Cl·、·CH₃)反应,包括以下几步: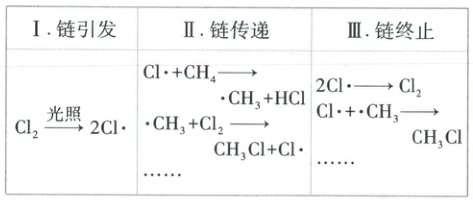
①写出由CH₃Cl生成CH₂Cl₂过程中链传递的方程式:CH₃Cl + Cl·→·CH₂Cl + HCl、________________________。
②已知:25℃、101 kPa时,CH₄中C—H和HCl中H—Cl的键能分别是439 kJ·mol⁻¹和431 kJ·mol⁻¹。则反应Cl· + CH₄→·CH₃ + HCl(填“放出”或“吸收”)热量。
(1)下列说法正确的是(填序号)。
A. 反应过程中试管内黄绿色逐渐变浅,试管壁上有油状液滴产生
B. 将该装置放在黑暗处,CH₄与Cl₂也能反应
C. 该实验发生了取代反应
D. CH₄和Cl₂完全反应后试管内液面上升,液体充满试管
(2)CH₄氯代为自由基(带有单电子的原子或原子团,如Cl·、·CH₃)反应,包括以下几步:

①写出由CH₃Cl生成CH₂Cl₂过程中链传递的方程式:CH₃Cl + Cl·→·CH₂Cl + HCl、________________________。
②已知:25℃、101 kPa时,CH₄中C—H和HCl中H—Cl的键能分别是439 kJ·mol⁻¹和431 kJ·mol⁻¹。则反应Cl· + CH₄→·CH₃ + HCl(填“放出”或“吸收”)热量。

答案:
6.
(1)AC
(2)①·CH₃Cl+Cl₂→CH₂Cl₂+Cl· ②吸收
[解析]
(1)Cl₂和甲烷在光照条件下发生取代反应,反应过程中试管内黄绿色逐渐变浅,试管壁上有油状液滴产生,A、C 正确;将该装置放在黑暗处,CH₄与Cl₂不发生反应,B错误;
高中必刷题 化学
CH₄和Cl₂完全反应后试管内液面上升,常温下CH₃Cl为气体,CH₂Cl₂、CHCl₃、CCl₄均为油状液体,液体不能充满试管,
D错误。
(2)②反应Cl·+CH₄→·CH₃+HCl的反应热为(4×439−3×439−431)kJ·mol⁻¹=8kJ·mol⁻¹,反应吸收热量。
(1)AC
(2)①·CH₃Cl+Cl₂→CH₂Cl₂+Cl· ②吸收
[解析]
(1)Cl₂和甲烷在光照条件下发生取代反应,反应过程中试管内黄绿色逐渐变浅,试管壁上有油状液滴产生,A、C 正确;将该装置放在黑暗处,CH₄与Cl₂不发生反应,B错误;
高中必刷题 化学
CH₄和Cl₂完全反应后试管内液面上升,常温下CH₃Cl为气体,CH₂Cl₂、CHCl₃、CCl₄均为油状液体,液体不能充满试管,
D错误。
(2)②反应Cl·+CH₄→·CH₃+HCl的反应热为(4×439−3×439−431)kJ·mol⁻¹=8kJ·mol⁻¹,反应吸收热量。
查看更多完整答案,请扫码查看


