2026年江苏13大市中考名卷优选38套化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年江苏13大市中考名卷优选38套化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第98页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
15 (12分)锰及其化合物在生产生活中具有广泛应用。
(1) 锰元素在元素周期表中的信息及原子结构示意图如图1所示,下列有关说法不正确的是
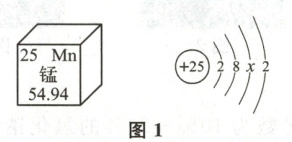
A. 图中$x=8$
B. 锰元素为非金属元素
C. 锰元素的原子序数是25
D. 锰元素的相对原子质量是54.94g
(2) 将打磨过的铝片插入$CuCl_{2}$溶液,观察到铝的表面有红色固体,意外发现铝片表面有少量气泡产生,据此可推测$CuCl_{2}$溶液中阳离子是
(3) $Mn_{3}O_{4}$常用于电子工业,$KMnO_{4}$可用于制备$O_{2}$,乙烯溶液还是良好的消毒剂,利用废电池的炭包(C、$MnO_{2}$)制备$Mn_{3}O_{4}$和$KMnO_{4}$流程如下。

①将炭包在足量氧气中焙烧,目的是
②反应1中化合价改变的元素是
③$MnSO_{4}$能与$O_{2}、NH_{3}$反应生成$(NH_{4})_{2}SO_{4}$和$Mn_{3}O_{4}$(难溶于水的黑色固体),实验装置如图2,制备时温度和pH对$Mn_{3}O_{4}$影响如图3,为获得产率高、纯度高的$Mn_{3}O_{4}$。请补充完整下列实验方案:取一定量的$MnSO_{4}$溶液放入三颈烧瓶中,在不断搅拌下,通入空气,
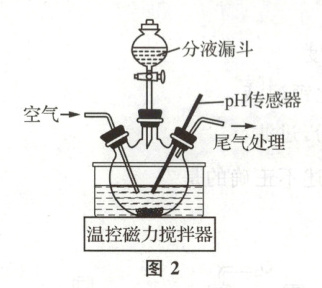

④反应2原理:$2MnO_{2}+4KOH+O_{2}\xlongequal{\triangle}2K_{2}MnO_{4}+2X$,X的化学式是
⑤将锰酸钾转化为高锰酸钾的方案通常有两种。
方案一:$2K_{2}MnO_{4}+2H_{2}O\xlongequal{通电}2KMnO_{4}+H_{2}\uparrow+2KOH$
方案二:$3K_{2}MnO_{4}+2H_{2}O+4CO_{2}=2KMnO_{4}+MnO_{2}\downarrow+4KHCO_{3}$
对比以上两种方案,你认为哪种方案更优?理由是
(1) 锰元素在元素周期表中的信息及原子结构示意图如图1所示,下列有关说法不正确的是
ABD
(填字母)。
A. 图中$x=8$
B. 锰元素为非金属元素
C. 锰元素的原子序数是25
D. 锰元素的相对原子质量是54.94g
(2) 将打磨过的铝片插入$CuCl_{2}$溶液,观察到铝的表面有红色固体,意外发现铝片表面有少量气泡产生,据此可推测$CuCl_{2}$溶液中阳离子是
Cu²⁺、H⁺
(填离子符号)。(3) $Mn_{3}O_{4}$常用于电子工业,$KMnO_{4}$可用于制备$O_{2}$,乙烯溶液还是良好的消毒剂,利用废电池的炭包(C、$MnO_{2}$)制备$Mn_{3}O_{4}$和$KMnO_{4}$流程如下。

①将炭包在足量氧气中焙烧,目的是
除去炭包中的碳
。②反应1中化合价改变的元素是
Mn、O
(填元素符号)。③$MnSO_{4}$能与$O_{2}、NH_{3}$反应生成$(NH_{4})_{2}SO_{4}$和$Mn_{3}O_{4}$(难溶于水的黑色固体),实验装置如图2,制备时温度和pH对$Mn_{3}O_{4}$影响如图3,为获得产率高、纯度高的$Mn_{3}O_{4}$。请补充完整下列实验方案:取一定量的$MnSO_{4}$溶液放入三颈烧瓶中,在不断搅拌下,通入空气,
控制溶液温度在50℃左右,打开分液漏斗旋塞逐滴滴加氨水至溶液pH接近8.5,充分反应一段时间后,过滤,用蒸馏水洗涤沉淀2~3次
,真空干燥(实验方案中必须使用的试剂:氨水、蒸馏水)。

④反应2原理:$2MnO_{2}+4KOH+O_{2}\xlongequal{\triangle}2K_{2}MnO_{4}+2X$,X的化学式是
H₂O
。⑤将锰酸钾转化为高锰酸钾的方案通常有两种。
方案一:$2K_{2}MnO_{4}+2H_{2}O\xlongequal{通电}2KMnO_{4}+H_{2}\uparrow+2KOH$
方案二:$3K_{2}MnO_{4}+2H_{2}O+4CO_{2}=2KMnO_{4}+MnO_{2}\downarrow+4KHCO_{3}$
对比以上两种方案,你认为哪种方案更优?理由是
方案一更优,Mn原子利用率高(或方案二更优,不需要通电,节约能源)(答案合理即可)
。
答案:
15.(除特殊标注外,每空1分,共12分)
(1)ABD(2分)
(2)Cu²⁺、H⁺(2分)
(3)①除去炭包中的碳 ②Mn、O(2分)
③控制溶液温度在50℃左右,打开分液漏斗旋塞逐滴滴加氨水至溶液pH接近8.5,充分反应一段时间后,过滤,用蒸馏水洗涤沉淀2~3次(3分)
④H₂O ⑤方案一更优,Mn原子利用率高(或方案二更优,不需要通电,节约能源)(答案合理即可)
解析:
(2)CuCl₂溶液与CuSO₄溶液类似,其水溶液也呈酸性,放入铝片产生的少量气体是H₂,则溶液中存在的阳离子是Cu²⁺、H⁺。
(3)①将炭包在足量的O₂中焙烧,目的是除去炭包中的碳。②焙烧后得到的是MnO₂,再用MnO₂作原料进行后续的系列转化,反应1为H₂O₂+H₂SO₄+MnO₂=MnSO₄+2H₂O+O₂↑,Mn元素由+4价变为+2价,O元素由-1价变为0价,其他元素的化合价未变。③结合图像分析,该反应在50℃并控制pH=8.5时产率最高,围绕这一核心信息再结合题目要求即可顺利解答。⑤方案选择时,可从过程控制、生产成本、原料利用率等角度进行分析。
Plus关键点拨
设计实验方案的要点
以本题为例,设计实验方案时,先结合图像分析出产率最大的反应条件(如温度、pH),再结合物质制备的步骤(如除杂、制备、过滤、洗涤、干燥)和装置图,将所给必用药品和操作情境用通顺的语言表达出来即可。
(1)ABD(2分)
(2)Cu²⁺、H⁺(2分)
(3)①除去炭包中的碳 ②Mn、O(2分)
③控制溶液温度在50℃左右,打开分液漏斗旋塞逐滴滴加氨水至溶液pH接近8.5,充分反应一段时间后,过滤,用蒸馏水洗涤沉淀2~3次(3分)
④H₂O ⑤方案一更优,Mn原子利用率高(或方案二更优,不需要通电,节约能源)(答案合理即可)
解析:
(2)CuCl₂溶液与CuSO₄溶液类似,其水溶液也呈酸性,放入铝片产生的少量气体是H₂,则溶液中存在的阳离子是Cu²⁺、H⁺。
(3)①将炭包在足量的O₂中焙烧,目的是除去炭包中的碳。②焙烧后得到的是MnO₂,再用MnO₂作原料进行后续的系列转化,反应1为H₂O₂+H₂SO₄+MnO₂=MnSO₄+2H₂O+O₂↑,Mn元素由+4价变为+2价,O元素由-1价变为0价,其他元素的化合价未变。③结合图像分析,该反应在50℃并控制pH=8.5时产率最高,围绕这一核心信息再结合题目要求即可顺利解答。⑤方案选择时,可从过程控制、生产成本、原料利用率等角度进行分析。
Plus关键点拨
设计实验方案的要点
以本题为例,设计实验方案时,先结合图像分析出产率最大的反应条件(如温度、pH),再结合物质制备的步骤(如除杂、制备、过滤、洗涤、干燥)和装置图,将所给必用药品和操作情境用通顺的语言表达出来即可。
查看更多完整答案,请扫码查看


