2026年江苏13大市中考名卷优选38套化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年江苏13大市中考名卷优选38套化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第115页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
11 (8分)合成氨是20世纪伟大的成就之一。研究氨气的组成、性质及用途具有重要意义。
(1) 液氨可用作制冷剂。构成氨分子的微粒是氮原子和。液态的氨转化为氨气的过程中,氨分子间的距离(填“变大”或“变小”)。
(2) 反应$8NH_3+3Cl_2=6NH_4Cl+N_2$可用于检查输送氯气的管道是否泄漏。
①$N$的质子数为7,核外第一层有2个电子,则第二层有个电子。由$Cl$转化为$Cl^-$的过程中,$Cl$(填“得到电子”或“失去电子”)。
②$NH_4^+$中$H$的化合价为+1,则$N$的化合价为。
(3) $NH_3$在能源与环境领域应用广泛。
①$NH_3$燃烧生成$N_2$和$H_2O$,未来可用作化石燃料的替代能源,从产物的角度分析,作为燃料$NH_3$相比于$CH_4$的优点是。
②$NH_3$可用于烟气脱硝,如$4NH_3+6R \begin{matrix}\underline{\underline{催化剂}}\\ \triangle\end{matrix} 5N_2+6H_2O$,$R$的化学式为 ______ 。
(1) 液氨可用作制冷剂。构成氨分子的微粒是氮原子和。液态的氨转化为氨气的过程中,氨分子间的距离(填“变大”或“变小”)。
(2) 反应$8NH_3+3Cl_2=6NH_4Cl+N_2$可用于检查输送氯气的管道是否泄漏。
①$N$的质子数为7,核外第一层有2个电子,则第二层有个电子。由$Cl$转化为$Cl^-$的过程中,$Cl$(填“得到电子”或“失去电子”)。
②$NH_4^+$中$H$的化合价为+1,则$N$的化合价为。
(3) $NH_3$在能源与环境领域应用广泛。
①$NH_3$燃烧生成$N_2$和$H_2O$,未来可用作化石燃料的替代能源,从产物的角度分析,作为燃料$NH_3$相比于$CH_4$的优点是。
②$NH_3$可用于烟气脱硝,如$4NH_3+6R \begin{matrix}\underline{\underline{催化剂}}\\ \triangle\end{matrix} 5N_2+6H_2O$,$R$的化学式为 ______ 。
答案:
11.(除特殊标注外,每空1分,共8分)
(1)氢原子 变大
(2)①5 得到电子 ②-3(2分)
(3)①燃烧产物无污染(或环保) ②NO
解析:
(2)②在离子团中各元素正负化合价的代数和为离子团所带电荷,已知NH₄⁺带1个单位正电荷,其中H的化合价为+1,设N的化合价为x,则有x+(+1)×4=+1,解得x=-3,因此,NH₄⁺中N的化合价为-3。
Plus易错提醒
(2)中NH₄⁺不是化合物,其化合价的代数和不为0,根据离子所带电荷数可以推导其化合价代数和为+1,从而计算出N的化合价为-3。
(1)氢原子 变大
(2)①5 得到电子 ②-3(2分)
(3)①燃烧产物无污染(或环保) ②NO
解析:
(2)②在离子团中各元素正负化合价的代数和为离子团所带电荷,已知NH₄⁺带1个单位正电荷,其中H的化合价为+1,设N的化合价为x,则有x+(+1)×4=+1,解得x=-3,因此,NH₄⁺中N的化合价为-3。
Plus易错提醒
(2)中NH₄⁺不是化合物,其化合价的代数和不为0,根据离子所带电荷数可以推导其化合价代数和为+1,从而计算出N的化合价为-3。
12 (6分)实验室以一种工业废渣(主要成分为$MgCO_3$,含少量$FeO$、$Fe_2O_3$、$Al_2O_3$)为原料制备$MgCO_3$。
实验过程如下:
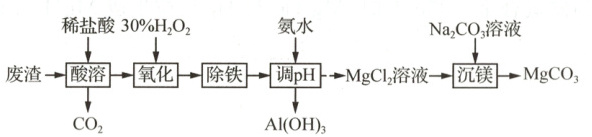
已知:①在溶液中,$pH=5.0$时$AlCl_3$完全转化为$Al(OH)_3$沉淀,$pH=8.5$时$MgCl_2$开始生成$Mg(OH)_2$沉淀。②$MgCl_2$在过量$Na_2CO_3$溶液中会生成$Mg(OH)_2$沉淀。
(1) “酸溶”时,$MgCO_3$与稀盐酸反应的化学方程式为
(2) “氧化”时发生的反应为$2FeCl_2+2HCl+H_2O_2=2FeCl_3+2H_2O$。
①反应前后化合价发生变化的元素有$O$、
②“酸溶”时需加入稍过量的稀盐酸,原因可能是
(3) “调$pH$”时,需控制溶液$pH$为
(4) “沉镁”时,为提高$MgCO_3$的纯度,试剂加入顺序为
a. 向$Na_2CO_3$溶液中逐滴加入$MgCl_2$溶液
b. 向$MgCl_2$溶液中逐滴加入$Na_2CO_3$溶液
实验过程如下:

已知:①在溶液中,$pH=5.0$时$AlCl_3$完全转化为$Al(OH)_3$沉淀,$pH=8.5$时$MgCl_2$开始生成$Mg(OH)_2$沉淀。②$MgCl_2$在过量$Na_2CO_3$溶液中会生成$Mg(OH)_2$沉淀。
(1) “酸溶”时,$MgCO_3$与稀盐酸反应的化学方程式为
MgCO₃+2HCl=MgCl₂+CO₂↑+H₂O
。(2) “氧化”时发生的反应为$2FeCl_2+2HCl+H_2O_2=2FeCl_3+2H_2O$。
①反应前后化合价发生变化的元素有$O$、
Fe
。②“酸溶”时需加入稍过量的稀盐酸,原因可能是
使废渣溶解充分,提高原料的浸出率(合理即可)
(写一条)。(3) “调$pH$”时,需控制溶液$pH$为
5.0≤pH<8.5
。(4) “沉镁”时,为提高$MgCO_3$的纯度,试剂加入顺序为
b
(填“a”或“b”)。a. 向$Na_2CO_3$溶液中逐滴加入$MgCl_2$溶液
b. 向$MgCl_2$溶液中逐滴加入$Na_2CO_3$溶液
答案:
12.(除特殊标注外,每空1分,共6分)
(1)MgCO₃+2HCl=MgCl₂+CO₂↑+H₂O(2分)
(2)①Fe ②使废渣溶解充分,提高原料的浸出率(合理即可)
(3)5.0≤pH<8.5
(4)b
解析:
(3)根据流程可知,“调pH”的目的是让AlCl₃完全转化为Al(OH)₃沉淀而MgCl₂不能转化为沉淀,根据题文信息,需控制溶液pH为5.0≤pH<8.5。
(4)MgCl₂在过量Na₂CO₃溶液中会生成Mg(OH)₂沉淀,“沉镁”时,为提高MgCO₃的纯度,试剂加入顺序为向MgCl₂溶液中逐滴加入Na₂CO₃溶液。
(1)MgCO₃+2HCl=MgCl₂+CO₂↑+H₂O(2分)
(2)①Fe ②使废渣溶解充分,提高原料的浸出率(合理即可)
(3)5.0≤pH<8.5
(4)b
解析:
(3)根据流程可知,“调pH”的目的是让AlCl₃完全转化为Al(OH)₃沉淀而MgCl₂不能转化为沉淀,根据题文信息,需控制溶液pH为5.0≤pH<8.5。
(4)MgCl₂在过量Na₂CO₃溶液中会生成Mg(OH)₂沉淀,“沉镁”时,为提高MgCO₃的纯度,试剂加入顺序为向MgCl₂溶液中逐滴加入Na₂CO₃溶液。
查看更多完整答案,请扫码查看


