2026年江苏13大市中考名卷优选38套化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年江苏13大市中考名卷优选38套化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第55页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
18 电厂的脱硫废水含${CaCl_{2}}$、${MgCl_{2}}$、${MgSO_{4}}$,通过如下实验净化。下列说法正确的是 ()
A.加入过量${Ba(OH)_{2}}$溶液,产生白色沉淀,静置,上层清液含2种溶质
B.再加入过量${Na_{2}CO_{3}}$溶液,搅拌、静置、过滤,所得滤渣中含4种难溶物质
C.向滤液中先滴加酚酞溶液、再加入稀盐酸,溶液先变红、再变无色后一定呈中性
D.净化过程中,若调换${Ba(OH)_{2}}$和${Na_{2}CO_{3}}$的添加顺序,则${Ca^{2+}}$、${Ba^{2+}}$也都能除尽
A.加入过量${Ba(OH)_{2}}$溶液,产生白色沉淀,静置,上层清液含2种溶质
B.再加入过量${Na_{2}CO_{3}}$溶液,搅拌、静置、过滤,所得滤渣中含4种难溶物质
C.向滤液中先滴加酚酞溶液、再加入稀盐酸,溶液先变红、再变无色后一定呈中性
D.净化过程中,若调换${Ba(OH)_{2}}$和${Na_{2}CO_{3}}$的添加顺序,则${Ca^{2+}}$、${Ba^{2+}}$也都能除尽
答案:
B
19 铜应用广泛,对其性质作如下探究。

实验①:取铜片和黄铜片相互刻画。
实验②:取铜片和锌片连接电流表并插入${CuSO_{4}}$溶液。
实验③:取铜粉于试管中,加入稀硫酸,通入${O_{2}}$并加热。
实验④:向实验③的溶液中逐滴加入$NaOH$溶液,产生沉淀的质量与滴加$NaOH$溶液质量关系如图所示。
下列说法不正确的是 ()
A.实验①中铜片上有划痕,说明铜片的硬度小于黄铜片
B.实验②中电流表指针发生偏转,说明化学能转化为电能
C.实验③中溶液变蓝,该反应为${2Cu + O_{2} + 2H_{2}SO_{4}\xlongequal{\triangle}2CuSO_{4} + 2H_{2}O}$
D.实验④图中M点对应的溶液中溶质为${CuSO_{4}}$、${Na_{2}SO_{4}}$

实验①:取铜片和黄铜片相互刻画。
实验②:取铜片和锌片连接电流表并插入${CuSO_{4}}$溶液。
实验③:取铜粉于试管中,加入稀硫酸,通入${O_{2}}$并加热。
实验④:向实验③的溶液中逐滴加入$NaOH$溶液,产生沉淀的质量与滴加$NaOH$溶液质量关系如图所示。
下列说法不正确的是 ()
A.实验①中铜片上有划痕,说明铜片的硬度小于黄铜片
B.实验②中电流表指针发生偏转,说明化学能转化为电能
C.实验③中溶液变蓝,该反应为${2Cu + O_{2} + 2H_{2}SO_{4}\xlongequal{\triangle}2CuSO_{4} + 2H_{2}O}$
D.实验④图中M点对应的溶液中溶质为${CuSO_{4}}$、${Na_{2}SO_{4}}$
答案:
D
20 已知:${Fe + Fe_{2}(SO_{4})_{3} = 3FeSO_{4}}$,${Cu + Fe_{2}(SO_{4})_{3} = 2FeSO_{4} + CuSO_{4}}$。取铜、铁的混合物18.0 g,加入400.0 g溶质质量分数为25.0%的${Fe_{2}(SO_{4})_{3}}$溶液,充分反应后剩余固体2.8 g。下列说法不正确的是 ()
A.剩余固体全部为铜
B.原固体混合物中铁的质量大于铜
C.所得溶液中铁元素和铜元素的质量比为7:2
D.向所得溶液中加入过量铁粉,充分反应后溶液中${FeSO_{4}}$质量为114.0 g
A.剩余固体全部为铜
B.原固体混合物中铁的质量大于铜
C.所得溶液中铁元素和铜元素的质量比为7:2
D.向所得溶液中加入过量铁粉,充分反应后溶液中${FeSO_{4}}$质量为114.0 g
答案:
B
21 (4分)用化学符号表示:
(1)金刚石
(2)最简单的有机物
(3)3个氯离子
(4)缺少
(1)金刚石
C
。(2)最简单的有机物
CH₄
。(3)3个氯离子
3Cl⁻
。(4)缺少
Zn
元素会使儿童发育停滞。
答案:
21.(每空1分,共4分)
(1)C
(2)$\mathrm{CH_4}$
(3)$3\mathrm{Cl^-}$
(4)Zn
(1)C
(2)$\mathrm{CH_4}$
(3)$3\mathrm{Cl^-}$
(4)Zn
22 (6分)选择下列适当的物质填空(填字母)。
A. 食盐
B. 烧碱
C. 熟石灰
D. 硝酸铵
E. 氧气
F. 干冰
G. 蛋白质
H. 纤维素
(1)可用于医疗急救的是
(2)厨房中作调味品的是
(3)可用于人工增雨的是
(4)可配制波尔多液的是
(5)溶于水温度明显升高的是
(6)鱼肉、牛奶中富含有
A. 食盐
B. 烧碱
C. 熟石灰
D. 硝酸铵
E. 氧气
F. 干冰
G. 蛋白质
H. 纤维素
(1)可用于医疗急救的是
E
。(2)厨房中作调味品的是
A
。(3)可用于人工增雨的是
F
。(4)可配制波尔多液的是
C
。(5)溶于水温度明显升高的是
B
。(6)鱼肉、牛奶中富含有
G
。
答案:
22.(每空1分,共6分)
(1)E
(2)A
(3)F
(4)C
(5)B
(6)G
(1)E
(2)A
(3)F
(4)C
(5)B
(6)G
23 (7分)助力“碳中和”,${CO_{2}}$捕集、高效制氢与综合利用是重要课题。
Ⅰ. ${CO_{2}}$的捕集。制备$CaO$捕集$CO$及再生的过程如下。

(1)转化①产生一种有毒气体,其化学式为
(2)与直接热解${CaCO_{3}}$生成$CaO$相比,“再生”反应${H_{2} + CaCO_{3}\xlongequal{600° C}CaO + CO + H_{2}O}$的优点是
Ⅱ. ${H_{2}}$的制取。
(3)光催化水制氢,原理如图1所示。整个过程中产生${H_{2}}$和${O_{2}}$的体积比为

(4)硼氢化钠水解制氢,原理为${NaBH_{4} + 2H_{2}O\xlongequal{ 催化剂}NaBO_{2} + 4H_{4}\uparrow}$。
①不同钛(Ti)的氧化物催化${NaBH_{4}}$水解产生${H_{2}}$的速率如图2所示。催化效率最好的是
②${NaBH_{4}}$水解制氢方便、制得的${H_{2}}$纯度高,但${NaBH_{4}}$价格昂贵阻碍其工业化发展。写出一条可能化解阻碍的发展路线: 。
Ⅲ. 综合利用。下列流程可实现${CO_{2}}$、${H_{2}}$的贮存、释放和利用。
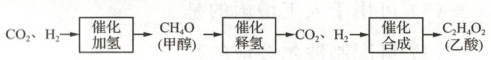
(5)“催化加氢”发生反应的化学方程式为
(6)利用“催化释氢”的产物催化合成乙酸时需添加
Ⅰ. ${CO_{2}}$的捕集。制备$CaO$捕集$CO$及再生的过程如下。

(1)转化①产生一种有毒气体,其化学式为
CO
。(2)与直接热解${CaCO_{3}}$生成$CaO$相比,“再生”反应${H_{2} + CaCO_{3}\xlongequal{600° C}CaO + CO + H_{2}O}$的优点是
反应条件相对温和,能耗低
。Ⅱ. ${H_{2}}$的制取。
(3)光催化水制氢,原理如图1所示。整个过程中产生${H_{2}}$和${O_{2}}$的体积比为
2:1
。
(4)硼氢化钠水解制氢,原理为${NaBH_{4} + 2H_{2}O\xlongequal{ 催化剂}NaBO_{2} + 4H_{4}\uparrow}$。
①不同钛(Ti)的氧化物催化${NaBH_{4}}$水解产生${H_{2}}$的速率如图2所示。催化效率最好的是
Ti₂O₃
。②${NaBH_{4}}$水解制氢方便、制得的${H_{2}}$纯度高,但${NaBH_{4}}$价格昂贵阻碍其工业化发展。写出一条可能化解阻碍的发展路线: 。
Ⅲ. 综合利用。下列流程可实现${CO_{2}}$、${H_{2}}$的贮存、释放和利用。

(5)“催化加氢”发生反应的化学方程式为
CO₂+3H₂→CH₄O+H₂O
。(6)利用“催化释氢”的产物催化合成乙酸时需添加
CO₂
(填“${CO_{2}}$”或“${H_{2}}$”)促进另一气体完全反应。
答案:
23.(每空1分,共7分)
I.
(1)CO
(2)反应条件相对温和,能耗低
II.
(3)2:1
(4)①$\mathrm{Ti_2O_3}$ ②实现$\mathrm{NaBH_4}$的循环利用(或寻找$\mathrm{NaBH_4}$的替代品等)
III.
(5)$\mathrm{CO_2+3H_2\xlongequal{催化剂}CH_4O+H_2O}$
(6)$\mathrm{CO_2}$
解析:I.
(1)转化①产生一种有毒气体,根据元素组成,可推知其为CO。
(2)直接热解$\mathrm{CaCO_3}$需要反应条件为800∼1000℃,“再生”生成CaO的反应温度为600℃,能耗低。III.
(5)由流程图,结合反应前后原子守恒可推知,$\mathrm{CO_2}$与$\mathrm{H_2}$反应除生成甲醇外,还应有水生成。
(6)“催化释氢”的反应为$\mathrm{CH_4O+H_2O\xlongequal{催化剂}CO_2+3H_2}$,“催化合成”乙酸的反应为$2\mathrm{CO_2+4H_2\xlongequal{催化剂}C_2H_4O_2+2H_2O}$,比较$\mathrm{CO_2}$和$\mathrm{H_2}$的分子数比,添加$\mathrm{CO_2}$可促进$\mathrm{H_2}$完全反应。
Plus关键点拨
利用化学方程式中的比例关系解题
由图可知,光催化水制氢总的反应物为$\mathrm{H_2O}$,生成物为$\mathrm{H_2}$和$\mathrm{O_2}$,总反应为$2\mathrm{H_2O\xlongequal{光,催化剂}2H_2\uparrow+O_2\uparrow}$,则整个过程中产生$\mathrm{H_2}$和$\mathrm{O_2}$的体积比为2:1。由“催化释氢”和“催化合成”的反应知,与催化合成所需的反应物相比,催化释氢产物中$\mathrm{CO_2}$所占比例偏小,为确保$\mathrm{H_2}$被反应完全,则需要添加的气体是$\mathrm{CO_2}$。
I.
(1)CO
(2)反应条件相对温和,能耗低
II.
(3)2:1
(4)①$\mathrm{Ti_2O_3}$ ②实现$\mathrm{NaBH_4}$的循环利用(或寻找$\mathrm{NaBH_4}$的替代品等)
III.
(5)$\mathrm{CO_2+3H_2\xlongequal{催化剂}CH_4O+H_2O}$
(6)$\mathrm{CO_2}$
解析:I.
(1)转化①产生一种有毒气体,根据元素组成,可推知其为CO。
(2)直接热解$\mathrm{CaCO_3}$需要反应条件为800∼1000℃,“再生”生成CaO的反应温度为600℃,能耗低。III.
(5)由流程图,结合反应前后原子守恒可推知,$\mathrm{CO_2}$与$\mathrm{H_2}$反应除生成甲醇外,还应有水生成。
(6)“催化释氢”的反应为$\mathrm{CH_4O+H_2O\xlongequal{催化剂}CO_2+3H_2}$,“催化合成”乙酸的反应为$2\mathrm{CO_2+4H_2\xlongequal{催化剂}C_2H_4O_2+2H_2O}$,比较$\mathrm{CO_2}$和$\mathrm{H_2}$的分子数比,添加$\mathrm{CO_2}$可促进$\mathrm{H_2}$完全反应。
Plus关键点拨
利用化学方程式中的比例关系解题
由图可知,光催化水制氢总的反应物为$\mathrm{H_2O}$,生成物为$\mathrm{H_2}$和$\mathrm{O_2}$,总反应为$2\mathrm{H_2O\xlongequal{光,催化剂}2H_2\uparrow+O_2\uparrow}$,则整个过程中产生$\mathrm{H_2}$和$\mathrm{O_2}$的体积比为2:1。由“催化释氢”和“催化合成”的反应知,与催化合成所需的反应物相比,催化释氢产物中$\mathrm{CO_2}$所占比例偏小,为确保$\mathrm{H_2}$被反应完全,则需要添加的气体是$\mathrm{CO_2}$。
查看更多完整答案,请扫码查看


