2026年学易优高考二轮总复习化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年学易优高考二轮总复习化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第28页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1.(2025·河北一模)用于$HMF$(  )转化为
)转化为 的液流燃料电池(LFFC)的结构和原理示意图如下图所示。该系统采用了酸性—碱性电解液的不对称设计,使用$1\ mol·L^{-1}KOH$作为M极电解液,使用$2\ mol·L^{-1}H_2SO_4$作为N极电解液。下列说法正确的是( )
的液流燃料电池(LFFC)的结构和原理示意图如下图所示。该系统采用了酸性—碱性电解液的不对称设计,使用$1\ mol·L^{-1}KOH$作为M极电解液,使用$2\ mol·L^{-1}H_2SO_4$作为N极电解液。下列说法正确的是( )

A.电子由N极通过外电路转移向M极
B.M极的电极反应式为$HMF + 6OH^- + 6e^- \longrightarrow 4H_2O + FDCA$
C.理论上,随反应进行需要及时添加$HNO_3$
D.理论上,当消耗$1.5\ mol\ O_2$时生成$1\ mol\ FDCA$
 )转化为
)转化为 的液流燃料电池(LFFC)的结构和原理示意图如下图所示。该系统采用了酸性—碱性电解液的不对称设计,使用$1\ mol·L^{-1}KOH$作为M极电解液,使用$2\ mol·L^{-1}H_2SO_4$作为N极电解液。下列说法正确的是( )
的液流燃料电池(LFFC)的结构和原理示意图如下图所示。该系统采用了酸性—碱性电解液的不对称设计,使用$1\ mol·L^{-1}KOH$作为M极电解液,使用$2\ mol·L^{-1}H_2SO_4$作为N极电解液。下列说法正确的是( )
A.电子由N极通过外电路转移向M极
B.M极的电极反应式为$HMF + 6OH^- + 6e^- \longrightarrow 4H_2O + FDCA$
C.理论上,随反应进行需要及时添加$HNO_3$
D.理论上,当消耗$1.5\ mol\ O_2$时生成$1\ mol\ FDCA$
答案:
1.D $N$极$V$化合价$+5\to+4$,得电子,则$N$极为正极,电极反应式为$VO_2^+ + e^- + 2H^+=VO^{2+} + H_2O$,故$M$极为负极,电极反应式为:$HMF + 6OH^- - 6e^-=4H_2O + FDCA$。生成的$VO^{2+}$在$NO$、$HNO_3$的催化下与氧气反应生成$VO_2^+$和$H_2O$。
据分析,$N$极为正极,$M$极为负极,电子由$M$极通过外电路转移到$N$极,故A错误;据分析,$M$极的电极反应式为$HMF + 6OH^- - 6e^-=4H_2O + FDCA$,故B错误;由图示可知,$HNO_3$通过通入氧气再生,循环利用,无需添加,故C错误;根据电子守恒,列出关系式:$1.5\ mol\ O_2\sim 6\ mol\ e^-\sim 1\ mol\ FDCA$,故D正确;故答案为D。
据分析,$N$极为正极,$M$极为负极,电子由$M$极通过外电路转移到$N$极,故A错误;据分析,$M$极的电极反应式为$HMF + 6OH^- - 6e^-=4H_2O + FDCA$,故B错误;由图示可知,$HNO_3$通过通入氧气再生,循环利用,无需添加,故C错误;根据电子守恒,列出关系式:$1.5\ mol\ O_2\sim 6\ mol\ e^-\sim 1\ mol\ FDCA$,故D正确;故答案为D。
2.(2025·黑龙江齐齐哈尔二模)与锂离子电池相比,镁离子电池因能量密度高、价格低廉而得到了广泛关注。一种$Mg–PTO$可充电电池示意图如下。该电池分别以$PTO$(结构如标注框内所示)材料和$Mg$为电极,以$Mg(CB_{11}H_{12})_2$溶液为电解质溶液。下列说法正确的是(
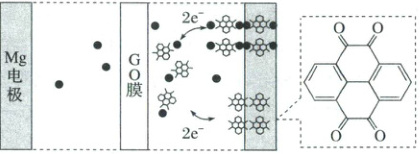
A.充电时,$Mg$电极为阳极
B.放电时,正极区存在反应:$MgPTO + 2e^- + Mg^{2+} \longrightarrow Mg_2PTO$
C.放电时,$PTO$能通过$GO$膜进入左室
D.充电时,外电路转移$0.1\ mol$电子,左边电极质量减少$1.2\ g$
B
)
A.充电时,$Mg$电极为阳极
B.放电时,正极区存在反应:$MgPTO + 2e^- + Mg^{2+} \longrightarrow Mg_2PTO$
C.放电时,$PTO$能通过$GO$膜进入左室
D.充电时,外电路转移$0.1\ mol$电子,左边电极质量减少$1.2\ g$
答案:
2.B 放电时$Mg$电极失电子转化为$Mg^{2+}$,$Mg$电极为负极,发生氧化反应$Mg-2e^-=Mg^{2+}$;$PTO$电极为正极,发生还原反应$PTO + 2e^- + Mg^{2+}=MgPTO$、$MgPTO + 2e^- + Mg^{2+}=Mg_2PTO$;充电时$Mg$电极为阴极,发生还原反应$Mg^{2+} + 2e^-=Mg$;$PTO$电极为阳极,发生氧化反应$Mg_2PTO-2e^-=PTO + Mg^{2+}$。放电时,$Mg$为负极,充电时$Mg$为阴极,故A错误;放电时,$PTO$电极为正极,发生还原反应$PTO + 2e^- + Mg^{2+}=MgPTO$、$MgPTO + 2e^- + Mg^{2+}=Mg_2PTO$,故B正确;图中$GO$膜只允许$Mg^{2+}$通过,能阻止$PTO$进入左极室,故C错误;充电时,外电路转移$0.1\ mol$电子,左侧反应为$Mg^{2+} + 2e^-=Mg$,左侧有$0.05\ mol\ Mg^{2+}$转化成$Mg$,使得左边电极质量增加$1.2\ g$,故D错误;选B。
3.(2025·广东深圳一模)我国科学家研发了一种具有“氨氧化、析氢”双功能的$Zn–NH_3$电池,其工作原理如图所示。下列说法不正确的是(

A.放电时,负极反应为$Zn + 4OH^- - 2e^- \longrightarrow [Zn(OH)_4]^{2-}$
B.充电时,阴极室电解质溶液pH增大
C.复合石墨电极表面,放电时析出$H_2$,充电时析出$N_2$
D.充电时,每生成$3\ mol\ Zn$,阳极室溶液质量减少$28\ g$
D
)
A.放电时,负极反应为$Zn + 4OH^- - 2e^- \longrightarrow [Zn(OH)_4]^{2-}$
B.充电时,阴极室电解质溶液pH增大
C.复合石墨电极表面,放电时析出$H_2$,充电时析出$N_2$
D.充电时,每生成$3\ mol\ Zn$,阳极室溶液质量减少$28\ g$
答案:
3.D 根据图示可知,放电时是原电池,放电时,负极为锌,锌在负极失去电子生成锌离子与氢氧根离子结合生成$[Zn(OH)_4]^{2-}$,负极的电极反应式为$Zn + 4OH^- - 2e^- = [Zn(OH)_4]^{2-}$,A正确;充电时,阴极的反应为$[Zn(OH)_4]^{2-} + 2e^-=Zn + 4OH^-$,当转移$2\ mol$电子时,生成$4\ mol\ OH^-$,有$2\ mol\ OH^-$透过阴离子交换膜移向右侧,故阴极室电解质溶液$pH$增大,B正确;由分析的电极反应可知,复合石墨电极表面,放电时析出$H_2$,充电时析出$N_2$,C正确;充电时,外电路转移$6\ mol$电子,阳极生成$1\ mol$氮气,同时会有$6\ mol\ OH^-$透过阴离子交换膜移向阳极室,故阳极室质量增加$6\ mol × 17\ g · mol^{-1} - 28\ g=74\ g$,D错误;故选D。
查看更多完整答案,请扫码查看


