2026年学易优高考二轮总复习化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年学易优高考二轮总复习化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第19页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
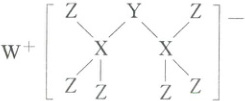
1. (2025·鄂东南省级示范高中联盟联考)科学家合成出了一种新化合物(如图所示),其中 W、X、Y、Z 为同一短周期元素,Z 核外最外层电子数是 X 核外电子数的一半。下列叙述正确的是(
A.一个 WZ 的晶胞中平均含有 4 个 W⁺
B.元素非金属性的强弱顺序为 X>Y>Z
C.Y 的最高价氧化物的水化物是强酸
D.该新化合物中 Y 不满足 8 电子稳定结构
A
)
A.一个 WZ 的晶胞中平均含有 4 个 W⁺
B.元素非金属性的强弱顺序为 X>Y>Z
C.Y 的最高价氧化物的水化物是强酸
D.该新化合物中 Y 不满足 8 电子稳定结构
答案:
1.A W、X、Y、Z为同一短周期元素,由化合物的组成,可确定Z的最外层电子数为7,Z核外最外层电子数是X核外电子数的一半,则X为Si,Z为Cl,W为Na,若Y为S,则不形成阴离子,所以Y为P,从而得出W、X、Y、Z分别为Na、Si、P、Cl。WZ为NaCl,NaCl晶胞中,Na⁺的个数为4,A正确;X、Y、Z分别为Si、P、Cl,位于同周期,元素非金属性强弱顺序为Cl>P>Si,B不正确;Y为P元素,其最高价氧化物的水化物是中强酸,C不正确;该新化合物中,Y为P元素,其与2个Si原子各形成1个共用电子对,还获得Na失去的1个电子,所以满足8电子稳定结构D不正确。
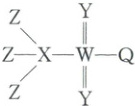
2. (2025·福建厦门二模)一种电池电解质的前驱体结构如图。X、Y、Z、W、Q 为分属三个主族的短周期元素,Z 的电负性最大,X 基态原子的 s 轨道上电子数是 p 轨道的 2 倍。下列说法错误的是(
A.最简单氢化物沸点:W>Y>X
B.第一电离能:Z>Y>X
C.键长:W-Q>W-X>X-Z
D.最高价氧化物对应水化物的酸性:Q>W>X
A
)
A.最简单氢化物沸点:W>Y>X
B.第一电离能:Z>Y>X
C.键长:W-Q>W-X>X-Z
D.最高价氧化物对应水化物的酸性:Q>W>X
答案:
2.A X、Y、Z、W、Q为分属三个主族的短周期元素,由前驱体的结构式可知,Z、Q形成1个共价键,Z的电负性最大,故Z为F,Q为Cl,X基态原子的s轨道上电子数是p轨道的2倍,X核外电子排布式为1s²2s²2p²,故X为C,Y形成2个共价键,W形成6个共价键,故Y为O,W为S,据此解答。根据上述分析,Y为O,W为S,X为C,H₂O分子间存在氢键,故沸点最高,相对分子质量越大,分子间范德华力越大,沸点越高,故沸点:H₂O>H₂S>CH₄,故最简单氢化物沸点:Y>W>X,A错误;Z为F,Y为O,X为C,同一周期内,随着原子序数的递增,元素第一电离能呈增大趋势,故第一电离能:F>O>C,B正确;W为S,X为C,Z为F,Q为Cl,原子半径:S>Cl>C>F,成键原子的半径越大,则键长越长,故键长:S−Cl>S−C>C−F,C正确;W为S,X为C,Q为Cl,元素非金属性越强,最高价氧化物对应水化物的酸性越强,故酸性:HClO₄>H₂SO₄>H₂CO₃,D正确;故答案为A。
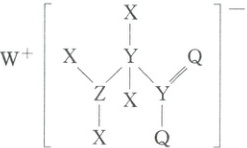
3. (2025·四川南充第一中学二模)化合物 A 是一种常见的食品添加剂,被广泛应用于酱油等调味品中,A 的结构如图所示。其中 X、Y、Z、Q、W 为原子序数依次增大的短周期主族元素,Q 的原子最外层电子数是电子层数的 3 倍。下列说法正确的是(
A.YQ₂ 与 ZQ₂ 的空间构型均为直线形
B.W 单质的熔点高于 Y 单质
C.Y、Z、Q 原子的杂化方式均为 sp³
D.最高价氧化物对应的水化物的酸性 Z>Y
D
)
A.YQ₂ 与 ZQ₂ 的空间构型均为直线形
B.W 单质的熔点高于 Y 单质
C.Y、Z、Q 原子的杂化方式均为 sp³
D.最高价氧化物对应的水化物的酸性 Z>Y
答案:
3.D 其中X、Y、Z、Q、W为原子序数依次增大的短周期主族元素,Q的原子最外层电子数是电子层数的3倍,Q为O元素,由结构图可知:X、Y、Z所成共价键的数目分别为1、4、3,则它们分别为H、C、N,而W能形成稳定的一价阳离子,则其为Na。CO₂的空间构型为直线形,NO₂中心原子价层电子对数为2+$\frac{1}{2}$(5 - 2×2)=3,空间构型为V形,故A错误;C单质的熔点高于Na,故B错误;由结构式可知,C既有sp²杂化、也有sp³杂化,故C错误;非金属性:N>C,非金属性越强,元素最高价氧化物对应的水化物的酸性越强,则酸性:HNO₃>H₂CO₃,选D。
1. (2025·黑吉辽蒙卷) $ Na_xWO_3 $ 晶体因 $ x $ 变化形成空位而导致颜色各异,当 $ 0.44 \leq x \leq 0.95 $ 时,其立方晶胞结构如图。设 $ N_A $ 为阿伏加德罗常数的值,下列说法错误的是(

A.与 $ W $ 最近且等距的 $ O $ 有 $ 6 $ 个
B.$ x $ 增大时,$ W $ 的平均价态升高
C.密度为 $ \frac{243.5 × 10^{30}}{a^3 · N_A} g · cm^{-3} $ 时,$ x = 0.5 $
D.空位数不同,吸收的可见光波长不同
B
)
A.与 $ W $ 最近且等距的 $ O $ 有 $ 6 $ 个
B.$ x $ 增大时,$ W $ 的平均价态升高
C.密度为 $ \frac{243.5 × 10^{30}}{a^3 · N_A} g · cm^{-3} $ 时,$ x = 0.5 $
D.空位数不同,吸收的可见光波长不同
答案:
1.B 由题图可知,W位于O形成的八面体空隙中,故与W最近且等距的O有6个,A正确;$\mathrm{Na_xWO_3}$中$\mathrm{Na}$为$+1$价,O为$-2$价,由化合物中各元素化合价代数和为零可知,$x$增大,W的平均价态降低,B错误;由均摊法可知,W位于晶胞顶点,个数为$8 × \frac{1}{8}=1$,O位于晶胞棱心,个数为$12 × \frac{1}{4}=3$,当$x=0.5$时,晶胞中$\mathrm{Na}$的个数为$0.5$,则晶体密度为$\frac{184+16 × 3+23 × 0.5}{a^3 · N_{\mathrm{A}} × 10^{-30}} \ \mathrm{g · cm^{-3}} =\frac{243.5 × 10^{30}}{a^3 · N_{\mathrm{A}}} \ \mathrm{g · cm^{-3}}$,C正确;由题目信息知,$\mathrm{Na_xWO_3}$晶体因$x$变化形成空位而导致颜色各异,空位能够捕获自由电子或空穴而对可见光产生选择性吸收,光的颜色与波长有关,故空位数不同,吸收的可见光波长不同,D正确。
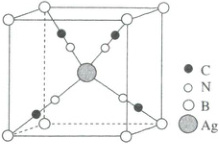
2. (2025·陕晋青宁卷) 一种负热膨胀材料的立方晶胞结构如图,晶体密度为 $ d g · cm^{-3} $。阿伏加德罗常数的值为 $ N_A $。下列说法错误的是(
A.沿晶胞体对角线方向的投影图为
B.$ Ag $ 和 $ B $ 均为 $ sp^3 $ 杂化
C.晶体中与 $ Ag $ 最近且距离相等的 $ Ag $ 有 $ 6 $ 个
D.$ Ag $ 和 $ B $ 的最短距离为 $ \frac{\sqrt{3}}{2} × \sqrt[3]{\frac{223}{N_A d}} × 10^{10} pm $
A
)
A.沿晶胞体对角线方向的投影图为

B.$ Ag $ 和 $ B $ 均为 $ sp^3 $ 杂化
C.晶体中与 $ Ag $ 最近且距离相等的 $ Ag $ 有 $ 6 $ 个
D.$ Ag $ 和 $ B $ 的最短距离为 $ \frac{\sqrt{3}}{2} × \sqrt[3]{\frac{223}{N_A d}} × 10^{10} pm $
答案:
2.A 沿晶胞体对角线方向投影得到的投影图为
,A错误;由题图可知,与Ag直接相连的原子有4个,晶胞中B位于顶点,个数为$8 × \frac{1}{8}=1$,与B直接相连的原子有4个,故Ag与B均为$\mathrm{sp^3}$杂化,B正确;晶体中与Ag最近且距离相等的Ag分别位于该晶胞上、下、前、后、左、右相邻6个晶胞的体心,C正确;Ag和B的最短距离为晶胞体对角线长的$\frac{1}{2}$,由题目信息知,该晶胞的密度为$d \ \mathrm{g · cm^{-3}}$,设晶胞参数为$a \ \mathrm{pm}$,由均摊法知,B位于晶胞的顶点,个数为$8 × \frac{1}{8}=1$,C、N、Ag均位于晶胞体内,个数分别为4、4、1,则该晶胞的密度=$\frac{ \frac{M(Ag_4C_4N_4B)}{} × 1}{ \left( a × 10^{-10} \mathrm{cm} \right)^3 × N_{\mathrm{A}} } = \frac{ \frac{223}{} × 10^{30}}{a^3 · N_{\mathrm{A}}} × 1 = d \ \mathrm{g · cm^{-3}}$,解得$a= \sqrt[3]{ \frac{223}{N_{\mathrm{A}}d}} × 10^{10}$,故Ag和B的最短距离为$\frac{\sqrt{3}}{2} × \sqrt[3]{ \frac{223}{N_{\mathrm{A}}d}} × 10^{10} \ \mathrm{pm}$,D正确。
2.A 沿晶胞体对角线方向投影得到的投影图为

,A错误;由题图可知,与Ag直接相连的原子有4个,晶胞中B位于顶点,个数为$8 × \frac{1}{8}=1$,与B直接相连的原子有4个,故Ag与B均为$\mathrm{sp^3}$杂化,B正确;晶体中与Ag最近且距离相等的Ag分别位于该晶胞上、下、前、后、左、右相邻6个晶胞的体心,C正确;Ag和B的最短距离为晶胞体对角线长的$\frac{1}{2}$,由题目信息知,该晶胞的密度为$d \ \mathrm{g · cm^{-3}}$,设晶胞参数为$a \ \mathrm{pm}$,由均摊法知,B位于晶胞的顶点,个数为$8 × \frac{1}{8}=1$,C、N、Ag均位于晶胞体内,个数分别为4、4、1,则该晶胞的密度=$\frac{ \frac{M(Ag_4C_4N_4B)}{} × 1}{ \left( a × 10^{-10} \mathrm{cm} \right)^3 × N_{\mathrm{A}} } = \frac{ \frac{223}{} × 10^{30}}{a^3 · N_{\mathrm{A}}} × 1 = d \ \mathrm{g · cm^{-3}}$,解得$a= \sqrt[3]{ \frac{223}{N_{\mathrm{A}}d}} × 10^{10}$,故Ag和B的最短距离为$\frac{\sqrt{3}}{2} × \sqrt[3]{ \frac{223}{N_{\mathrm{A}}d}} × 10^{10} \ \mathrm{pm}$,D正确。
查看更多完整答案,请扫码查看


