2026年学易优高考二轮总复习化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年学易优高考二轮总复习化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第24页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
1. (2025·河南郑州二模)Ca²⁺一般不形成配位化合物,但可与乙二胺四乙酸(EDTA)离子通过配位键形成稳定的螯合离子,其结构如下图所示。Nₐ为阿伏加德罗常数的值。
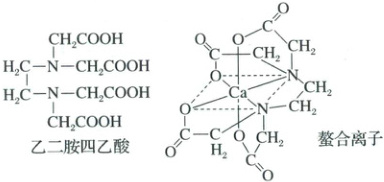
下列说法错误的是(
A.螯合离子中含 5 个五元环
B.0.5 mol 螯合离子中含 π 键数为 4Nₐ
C.乙二胺四乙酸分子中碳原子的杂化类型有 sp²、sp³两种
D.螯合离子中与 Ca²⁺形成配位键的原子在空间上构成八面体形

下列说法错误的是(
B
)A.螯合离子中含 5 个五元环
B.0.5 mol 螯合离子中含 π 键数为 4Nₐ
C.乙二胺四乙酸分子中碳原子的杂化类型有 sp²、sp³两种
D.螯合离子中与 Ca²⁺形成配位键的原子在空间上构成八面体形
答案:
1.B 根据图示,每个螯合离子中含有$5$个五元环,A正确;一个$Ca^{2+}$与一个乙二胺四乙酸(EDTA)离子形成螯合离子,每个乙二胺四乙酸离子中有$4$个$C=O$即$4$个$\pi$键,故$0.5 mol$螯合离子中含$\pi$键数为$2N_{A}$,B错误;乙二胺四乙酸分子中$—COO—$的碳原子成三条$\sigma$键,没有孤电子对,采用$sp^{2}$杂化,$—CH_{2}—$的碳原子成四条$\sigma$键,没有孤电子对,采用$sp^{3}$杂化,C正确;根据图知,螯合离子中与$Ca^{2+}$形成配位键的原子为$N$原子和连接单键的$O$原子,共$6$个配位原子,与$Ca^{2+}$在空间上构成八面体形,D正确;故选B。
2. (2025·四川雅安二模)磷化铟晶体(相对分子质量为 Mr)的载流子迁移率大,可用于制造高速电子器件,如高速晶体管和高电子迁移率晶体管。磷化铟的立方晶胞(晶胞参数为 m pm)如下图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,图中 a 原子的分数坐标为$(0,\frac{1}{2},\frac{1}{2})$,下列说法不正确的是(
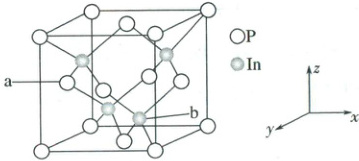
A.其化学式为 InP
B.每个 P 周围紧邻且距离相等的 P 有 4 个
C.b 原子的分数坐标为$(\frac{3}{4},\frac{3}{4},\frac{1}{4})$
D.设 Nₐ为阿伏加德罗常数的值,则其晶体的密度为$\frac{4Mr×10^{30}}{N_Am^3}$ g·cm⁻³
B
)
A.其化学式为 InP
B.每个 P 周围紧邻且距离相等的 P 有 4 个
C.b 原子的分数坐标为$(\frac{3}{4},\frac{3}{4},\frac{1}{4})$
D.设 Nₐ为阿伏加德罗常数的值,则其晶体的密度为$\frac{4Mr×10^{30}}{N_Am^3}$ g·cm⁻³
答案:
2.B 晶胞中,$In$原子数目为$4$,$P$的原子数目$8×\frac{1}{8}+6×\frac{1}{2}=4$,二者原子数目之比为$1:1$,则晶体的化学式$InP$,故A正确;以顶角$P$原子分析,其周围紧邻且距离相等的$P$处于晶胞面心,每个顶角围为$8$个晶胞共用、每个面心为$2$个晶胞共用,则每个$P$周围紧邻且距离相等的$P$有$\frac{3×8}{2}=12$个,故B错误;由几何知识可知,$b$原子到左侧面、后平面、下底面的距离分别为晶胞参数的$\frac{3}{4}$、$\frac{3}{4}$、$\frac{1}{4}$,则$b$原子的分数坐标为$(\frac{3}{4},\frac{3}{4},\frac{1}{4})$,故C正确;$1 mol$晶胞含有$4 mol InP$,$1 mol$晶胞的质量为$4 mol× Mr g·mol^{-1}=4Mr g$,$1 mol$晶胞体积为$(m×10^{-10} cm)^{3}× N_{A}$,则晶体密度=$\frac{4Mr g}{(m×10^{-10} cm)^{3}× N_{A}}=\frac{4Mr×10^{30}}{N_{A}· m^{3}} g·cm^{-3}$,故D正确;答案选B。
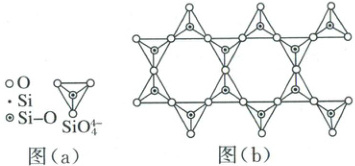
3. 天然硅酸盐组成复杂阴离子的基本结构单元是 SiO₄⁴⁻四面体,如图(a),通过共用顶角氧离子可形成链状、网状等结构,图(b)为一种无限长双链的多硅酸根,其中 Si 与 O 的原子个数之比为________,化学式为________。
]
]

答案:
3.答案:$4:11$ $[Si_{4}O_{11}]_{n}^{6n-}$
解析:$n$个$SiO_{4}^{4-}$通过共用顶角氧离子可形成双链结构,找出重复的结构单元,如图:
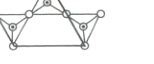
由于是双链,其中$Si$的原子数为$4$,顶角氧占$\frac{1}{2}$,$O$原子数为$4×\frac{1}{2}+6×\frac{1}{2}+4+2=11$,其中$Si$与$O$的原子数之比为$4:11$,化学式为$[Si_{4}O_{11}]_{n}^{6n-}$。
3.答案:$4:11$ $[Si_{4}O_{11}]_{n}^{6n-}$
解析:$n$个$SiO_{4}^{4-}$通过共用顶角氧离子可形成双链结构,找出重复的结构单元,如图:

由于是双链,其中$Si$的原子数为$4$,顶角氧占$\frac{1}{2}$,$O$原子数为$4×\frac{1}{2}+6×\frac{1}{2}+4+2=11$,其中$Si$与$O$的原子数之比为$4:11$,化学式为$[Si_{4}O_{11}]_{n}^{6n-}$。
4. (2025·辽宁省沈阳市高中联合体高三模拟节选)超高热导率半导体材料砷化硼(BAs)的立方晶胞结构如下图所示,则 1 号砷原子的原子分数坐标为
 ]
]
$(\frac{1}{4},\frac{1}{4},\frac{1}{4})$
。若晶胞中 As 原子到 B 原子最近距离为 a pm,则该晶体的密度 ρ = $\frac{4×86}{(\frac{4}{\sqrt{3}}a)^{3}N_{A}}×10^{30}$
g·cm⁻³(列出计算式,阿伏加德罗常数的值为 Nₐ)。 ]
]
答案:
4.答案:$(\frac{1}{4},\frac{1}{4},\frac{1}{4})$ $\frac{4×86}{(\frac{4}{\sqrt{3}}a)^{3}N_{A}}×10^{30}$
解析:由图,$1$号砷原子在$x$、$y$、$z$轴上投影坐标分别为$\frac{1}{4}$、$\frac{1}{4}$、$\frac{1}{4}$,则原子分数坐标为$(\frac{1}{4},\frac{1}{4},\frac{1}{4})$;晶胞中$As$原子到$B$原子最近距离为$a pm$,此距离为体对角线的四分之一,则晶胞参数为$\frac{4}{\sqrt{3}}a pm$,据“均摊法”,晶胞中含$8×\frac{1}{8}+6×\frac{1}{2}=4$个$B$、$4$个$As$,则晶体密度为$\frac{4×86}{(\frac{4}{\sqrt{3}}a)^{3}N_{A}}×10^{30} g·cm^{-3}$。
解析:由图,$1$号砷原子在$x$、$y$、$z$轴上投影坐标分别为$\frac{1}{4}$、$\frac{1}{4}$、$\frac{1}{4}$,则原子分数坐标为$(\frac{1}{4},\frac{1}{4},\frac{1}{4})$;晶胞中$As$原子到$B$原子最近距离为$a pm$,此距离为体对角线的四分之一,则晶胞参数为$\frac{4}{\sqrt{3}}a pm$,据“均摊法”,晶胞中含$8×\frac{1}{8}+6×\frac{1}{2}=4$个$B$、$4$个$As$,则晶体密度为$\frac{4×86}{(\frac{4}{\sqrt{3}}a)^{3}N_{A}}×10^{30} g·cm^{-3}$。
查看更多完整答案,请扫码查看


