第84页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
12.某温度下,在恒容密闭容器中进行反应:$\text{X(g)} + \text{Y(g)}\rightleftharpoons \text{Z(g)} + \text{W(s)}$。下列叙述正确的是 ( )
A.充入$\text{X}$,反应速率减小
B.当容器中$\text{Y}$的正反应速率与逆反应速率相等时,反应达到平衡
C.升高温度,反应速率减小
D.达到平衡后,反应停止
A.充入$\text{X}$,反应速率减小
B.当容器中$\text{Y}$的正反应速率与逆反应速率相等时,反应达到平衡
C.升高温度,反应速率减小
D.达到平衡后,反应停止
答案:
B [充入X,反应物的浓度增大,反应速率增大,故A错误;当容器中Y的正反应速率与逆反应速率相等时,各物质的浓度保持不变,反应达到平衡,故B正确;升高温度,反应速率增大,故C错误;化学平衡是动态平衡,达到平衡后,反应没有停止,故D错误。]
13.向容积为$1.0\ L$的密闭容器中通入一定量的$\text{N}_{2}\text{O}_{4}$和$\text{NO}_{2}$的混合气体,发生反应:$\text{N}_{2}\text{O}_{4}(g)\rightleftharpoons 2\text{NO}_{2}(g)$,体系中各物质浓度随时间变化如图所示。下列有关说法正确的是 ( )
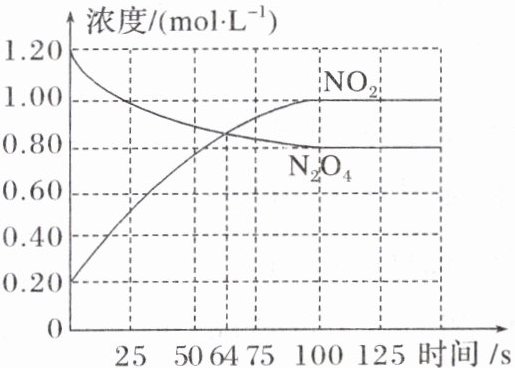
已知:$\text{NO}_{2}$为红棕色气体,$\text{N}_{2}\text{O}_{4}$为无色气体
A.$64\ s$时,反应达到化学平衡状态
B.达到化学平衡前,混合气体的颜色逐渐变浅
C.当容器中气体的密度保持不变时,该反应达到化学平衡状态
D.前$100\ s$内,用$\text{NO}_{2}$浓度的变化表示的化学反应速率是$0.008\ mol\cdot L^{-1}\cdot s^{-1}$

已知:$\text{NO}_{2}$为红棕色气体,$\text{N}_{2}\text{O}_{4}$为无色气体
A.$64\ s$时,反应达到化学平衡状态
B.达到化学平衡前,混合气体的颜色逐渐变浅
C.当容器中气体的密度保持不变时,该反应达到化学平衡状态
D.前$100\ s$内,用$\text{NO}_{2}$浓度的变化表示的化学反应速率是$0.008\ mol\cdot L^{-1}\cdot s^{-1}$
答案:
D [A项,反应达到化学平衡状态时,各物质的浓度不变,但不一定相等,由题图中信息可知,64 s时反应未达到化学平衡状态;B项,由题图中信息可知,反应正向进行,反应体系中c(NO₂)增大,所以混合气体的颜色逐渐变深;C项,反应前后气体的质量不变,容器容积不变,密度始终不变,当容器中气体的密度保持不变时,不能说明该反应达到化学平衡状态;D项,前100 s内,NO₂浓度的变化为(1.00 - 0.20) mol/L = 0.80 mol/L,化学反应速率v = 0.80 mol/L÷100 s = 0.008 mol·L⁻¹·s⁻¹。]
14.按要求作答。
(1)在容积为$5\ L$的密闭容器中,加入$0.2\ mol\ \text{CO}$和$0.2\ mol\ \text{H}_{2}\text{O(g)}$,在催化剂存在的条件下高温加热,发生反应$\text{CO(g)} + \text{H}_{2}\text{O(g)}\rightleftharpoons \text{CO}_{2}(g) + \text{H}_{2}(g)$,并放出热量。反应中$\text{CO}_{2}$的浓度随时间变化的曲线如图所示。
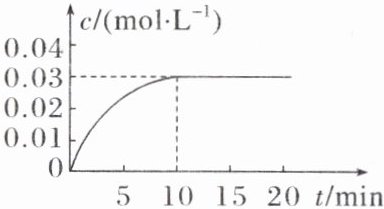
根据图中数据,从反应开始至达到平衡时,$\text{CO}$的化学反应速率为________;反应达到平衡时$c(\text{H}_{2}) = $________;判断该反应达到平衡状态的依据是________(填字母序号)。
A.单位时间内$\text{CO}$消耗的物质的量和$\text{CO}_{2}$消耗的物质的量相等
B.$\text{CO}$、$\text{H}_{2}\text{O}$、$\text{CO}_{2}$、$\text{H}_{2}$的浓度都相等
C.$\text{CO}$、$\text{H}_{2}\text{O}$、$\text{CO}_{2}$、$\text{H}_{2}$的浓度都不再发生变化
D.正、逆反应速率都为$0$
(2)在容积固定的绝热容器中发生反应$2\text{NO(g)} + 2\text{CO(g)}\rightleftharpoons 2\text{CO}_{2}(g) + \text{N}_{2}(g)$,能说明该反应已达到平衡状态的是________(填字母序号)。
A.容器内温度不再变化
B.$1\ mol\ \text{N}\equiv\text{N}$断裂的同时,有$2\ mol\ \text{CO}$消耗
C.$2v_{逆}(\text{NO}) = v_{正}(\text{N}_{2})$
D.容器内混合气体的密度保持不变
(3)一定温度下,往容积为$2\ L$的密闭容器中充入$1\ mol\ \text{N}_{2}$和$3\ mol\ \text{H}_{2}$,在一定条件下发生合成氨反应,$2\ min$时达到平衡。测得平衡时混合气体中$\text{NH}_{3}$的体积分数为$25\%$。则:$0~2\ min$内,$v(\text{NH}_{3}) = $________;$\text{H}_{2}$在平衡混合气中的体积分数$ = $________;平衡时容器的压强与起始时的压强之比为________;能说明该反应进行到最大限度的是________(填字母序号)。
a.$\text{N}_{2}$的转化率达到最大值
b.$\text{N}_{2}$、$\text{H}_{2}$和$\text{NH}_{3}$的体积分数之比为$1:3:2$
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
(1)在容积为$5\ L$的密闭容器中,加入$0.2\ mol\ \text{CO}$和$0.2\ mol\ \text{H}_{2}\text{O(g)}$,在催化剂存在的条件下高温加热,发生反应$\text{CO(g)} + \text{H}_{2}\text{O(g)}\rightleftharpoons \text{CO}_{2}(g) + \text{H}_{2}(g)$,并放出热量。反应中$\text{CO}_{2}$的浓度随时间变化的曲线如图所示。

根据图中数据,从反应开始至达到平衡时,$\text{CO}$的化学反应速率为________;反应达到平衡时$c(\text{H}_{2}) = $________;判断该反应达到平衡状态的依据是________(填字母序号)。
A.单位时间内$\text{CO}$消耗的物质的量和$\text{CO}_{2}$消耗的物质的量相等
B.$\text{CO}$、$\text{H}_{2}\text{O}$、$\text{CO}_{2}$、$\text{H}_{2}$的浓度都相等
C.$\text{CO}$、$\text{H}_{2}\text{O}$、$\text{CO}_{2}$、$\text{H}_{2}$的浓度都不再发生变化
D.正、逆反应速率都为$0$
(2)在容积固定的绝热容器中发生反应$2\text{NO(g)} + 2\text{CO(g)}\rightleftharpoons 2\text{CO}_{2}(g) + \text{N}_{2}(g)$,能说明该反应已达到平衡状态的是________(填字母序号)。
A.容器内温度不再变化
B.$1\ mol\ \text{N}\equiv\text{N}$断裂的同时,有$2\ mol\ \text{CO}$消耗
C.$2v_{逆}(\text{NO}) = v_{正}(\text{N}_{2})$
D.容器内混合气体的密度保持不变
(3)一定温度下,往容积为$2\ L$的密闭容器中充入$1\ mol\ \text{N}_{2}$和$3\ mol\ \text{H}_{2}$,在一定条件下发生合成氨反应,$2\ min$时达到平衡。测得平衡时混合气体中$\text{NH}_{3}$的体积分数为$25\%$。则:$0~2\ min$内,$v(\text{NH}_{3}) = $________;$\text{H}_{2}$在平衡混合气中的体积分数$ = $________;平衡时容器的压强与起始时的压强之比为________;能说明该反应进行到最大限度的是________(填字母序号)。
a.$\text{N}_{2}$的转化率达到最大值
b.$\text{N}_{2}$、$\text{H}_{2}$和$\text{NH}_{3}$的体积分数之比为$1:3:2$
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
答案:
解析 (1)根据题图中数据,从反应开始至10 min,反应达到平衡,CO₂的浓度增加了0.03 mol·L⁻¹,变化量之比等于化学计量数之比,则CO的浓度减少了0.03 mol·L⁻¹,化学反应速率为0.003 mol·L⁻¹·min⁻¹;反应达到平衡时c(H₂)=c(CO₂)=0.03 mol·L⁻¹。A. 单位时间内CO消耗的物质的量和CO₂消耗的物质的量相等,正逆反应速率相等,反应达到平衡;B. CO、H₂O、CO₂、H₂的浓度都相等,不能说明保持不变,则不能说明反应达到平衡;C. CO、H₂O、CO₂、H₂的浓度都不再发生变化,各物质含量不变,反应达到平衡;D. 可逆反应达到平衡时,正、逆反应速率相等,但不为0;符合题意的是AC。(2)在容积固定的绝热容器中发生反应2NO(g) + 2CO(g) ⇌ 2CO₂(g) + N₂(g),A. 绝热容器,容器内温度是变量,不再变化,则说明反应达到平衡;B. 1 mol N≡N断裂的同时,有2 mol CO消耗,说明正逆反应速率相等,达到平衡;C. 2v逆(NO)=v正(N₂),则v逆(NO):v正(N₂)=1:2,不等于化学计量数之比,不能说明反应达到平衡;D. 容器容积固定,气体的总质量保持不变,混合气体的密度始终保持不变,不能说明达到平衡;符合题意的是AB。(3)根据题意,设平衡时N₂转化了x mol,列三段式:
N₂ + 3H₂ ⇌ 2NH₃
起始/mol 1 3 0
转化/mol x 3x 2x
平衡/mol 1 - x 3 - 3x 2x
则有2x / (4 - 2x)×100% = 25%,解得x = 0.4;0~2 min内,n(NH₃)=0.8 mol,则v(NH₃)=0.8 mol / (2 L×2 min)=0.2 mol·L⁻¹·min⁻¹;根据阿伏加德罗定律,H₂在平衡混合气中的体积分数等于物质的量分数,为(3 - 3×0.4) / (4 - 2×0.4)×100% = 56.25%;平衡时容器的压强与起始时的压强之比为(4 - 2×0.4):4 = 4:5;a. N₂的转化率达到最大值,说明反应达到最大限度;b. N₂、H₂和NH₃的体积分数之比为1:3:2,不能说明各物质的含量保持不变,故不能说明反应达到最大限度;c. 反应容器的体积不变,气体总质量不变,体系内气体的密度始终不变,故体系内气体的密度保持不变不能说明反应进行到最大限度;d. 体系内物质的平均相对分子质量在数值上等于气体总质量与气体总物质的量的比值,气体总质量不变,气体总物质的量是变量,故平均相对分子质量保持不变,说明该反应进行到最大限度;符合题意的是ad。
答案 (1)0.003 mol·L⁻¹·min⁻¹ 0.03 mol·L⁻¹ AC (2)AB (3)0.2 mol·L⁻¹·min⁻¹ 56.25% 4:5 ad
查看更多完整答案,请扫码查看


