第75页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
1.可逆反应
(1)定义
在同一条件下 正向反应 和 逆向反应 均能进行的化学反应。
(2)特点
①正向反应和逆向反应 同时 进行。
②一定条件下,反应物不可能 完全 转化为生成物,即反应物的转化率不可能达到 100% 。
(3)表示
书写 可逆反应的化学方程式时不用“——”而用“⇌”。
(1)定义
在同一条件下 正向反应 和 逆向反应 均能进行的化学反应。
(2)特点
①正向反应和逆向反应 同时 进行。
②一定条件下,反应物不可能 完全 转化为生成物,即反应物的转化率不可能达到 100% 。
(3)表示
书写 可逆反应的化学方程式时不用“——”而用“⇌”。
答案:
1.(1)正反应方向 逆反应方向 (2)①同时 ②全部 100%
2.化学平衡状态的建立
(1)化学平衡状态的建立过程
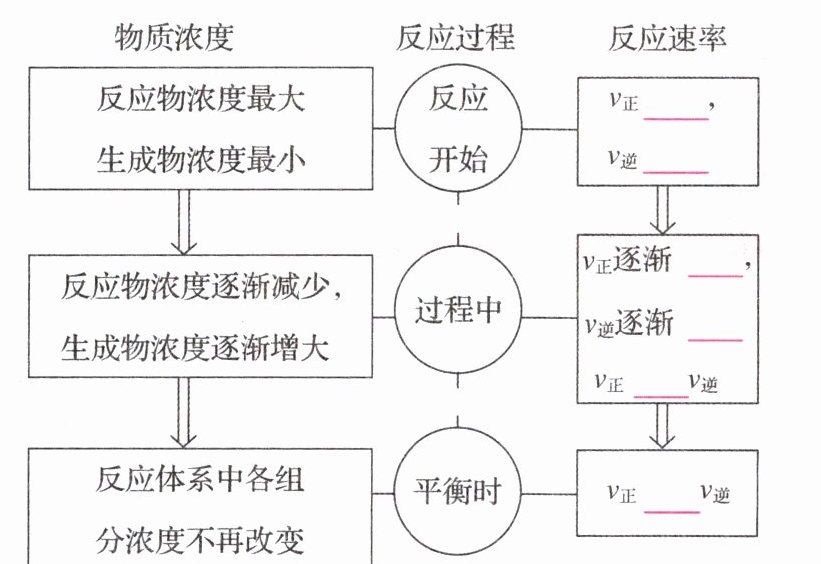
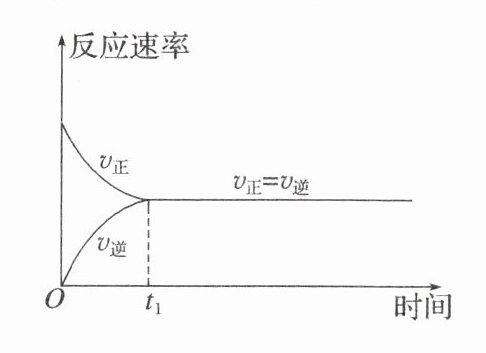
(2)用速率变化图像表示化学平衡状态的建立
(1)化学平衡状态的建立过程

(2)用速率变化图像表示化学平衡状态的建立

答案:
2.(1)最大 为零 减小 增大 > =
3.化学平衡状态
(1)化学平衡状态的概念
如果外界条件(温度、浓度、压强等)不发生改变,当 可逆 反应进行到一定程度时, 正反应速率 与 逆反应速率 相等,反应物的浓度和生成物的浓度 不再改变 ,达到一种表面静止的状态,称为化学平衡状态,简称化学平衡。
(2)化学平衡状态的特征

(1)化学平衡状态的概念
如果外界条件(温度、浓度、压强等)不发生改变,当 可逆 反应进行到一定程度时, 正反应速率 与 逆反应速率 相等,反应物的浓度和生成物的浓度 不再改变 ,达到一种表面静止的状态,称为化学平衡状态,简称化学平衡。
(2)化学平衡状态的特征

答案:
3.(1)可逆 正反应速率 逆反应速率 都不再改变
1.化学反应在一定条件下建立平衡状态时,化学反应将会停止。 (×)
2.在一定条件下,一个可逆反应达到的平衡状态,就是该反应所能达到的最大限度。 (√)
3.化学反应的限度与时间的长短无关。 (√)
4.化学反应的限度是不可改变的。 (×)
2.在一定条件下,一个可逆反应达到的平衡状态,就是该反应所能达到的最大限度。 (√)
3.化学反应的限度与时间的长短无关。 (√)
4.化学反应的限度是不可改变的。 (×)
答案:
×
@@√
@@√
@@×
@@√
@@√
@@×
1.工业上合成氨的反应为$N_{2}(g)+3H_{2}(g)\underset{催化剂}{\overset{高温、高压}{\rightleftharpoons}}2NH_{3}(g)$,在实际生产中为提高合成氨的反应速率,下列说法正确的是 (C)
A.温度越高,反应速率越快,因此采取的温度越高越好
B.压强越大,反应速率越快,因此采取的压强越大越好
C.催化剂能加快反应速率,因此可选用适当的催化剂
D.可向容器中加入一定量的水蒸气,使氨溶解以提高反应速率
A.温度越高,反应速率越快,因此采取的温度越高越好
B.压强越大,反应速率越快,因此采取的压强越大越好
C.催化剂能加快反应速率,因此可选用适当的催化剂
D.可向容器中加入一定量的水蒸气,使氨溶解以提高反应速率
答案:
C [A项,温度高反应速率快,但温度过高会消耗更多的燃料,因此实际生产中的温度不是越高越好,错误;B项,压强大反应速率快,但压强过高会增加设备的成本,因此实际生产中的压强不是越大越好,错误;C项,可选用适当的催化剂提高反应速率,正确;D项,加入水蒸气会降低反应体系的温度,且氨溶于水并不能提高反应速率,错误。]
查看更多完整答案,请扫码查看


