第129页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
1.下列关于金属冶炼的说法中错误的是( )
A.电解法获得镁时,不可在CO₂或N₂中降温冷却
B.热还原法常用的还原剂有CO、H₂、C、Al等
C.金属Na、Mg、Al均能通过电解熔融氯化物的方法获得
D.回收废旧金属可以重新制成金属或它们的化合物
A.电解法获得镁时,不可在CO₂或N₂中降温冷却
B.热还原法常用的还原剂有CO、H₂、C、Al等
C.金属Na、Mg、Al均能通过电解熔融氯化物的方法获得
D.回收废旧金属可以重新制成金属或它们的化合物
答案:
C [A项,镁与CO₂或N₂都能反应,因此电解法获得镁时,不可在CO₂或N₂中降温冷却;B项,热还原法常用有CO、H₂、C、Al等四种还原剂;C项,金属Na、Mg均能通过电解熔融氯化物的方法获得,金属Al通过电解熔融氧化铝的方法获得;D项,回收废旧金属可进行冶炼生成金属单质,也可用于制备其他化工产品,如回收铁、铝等。]
2.在金属活动性顺序中,钴的活动性介于镁和铜之间。工业上冶炼钴的方法是 ( )
A.加热CoO制备Co
B.在高温下用CO还原CoO制备Co
C.常温下电解固体CoO制备Co
D.钠与CoCl₂溶液反应制备Co
A.加热CoO制备Co
B.在高温下用CO还原CoO制备Co
C.常温下电解固体CoO制备Co
D.钠与CoCl₂溶液反应制备Co
答案:
B [钴的活动性介于镁和铜之间,故工业上冶炼钴应采用热还原法,通过加入还原剂,将钴还原出来,A、C项不符合题意;钠会与水反应,D项不符合题意。]
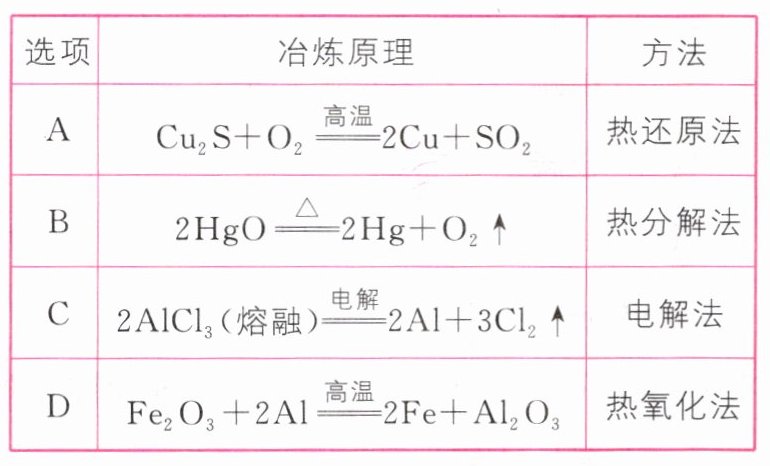
3.下表中金属的冶炼原理与方法都正确的是 ( )

答案:
B [A项,$Cu_{2}S + O_{2}\xlongequal{高温}2Cu + SO_{2}$中氧气不是还原剂,所以采用的不是热还原法;B项,Hg为不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来;C项,Al为活泼金属,通常用电解熔融的金属化合物的方法冶炼,但氯化铝是共价化合物,熔融态不导电;D项,铝的还原性大于铁,可利用铝热反应产生的高温来冶炼,属于热还原法。]
4.工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:
①$2C(焦炭)+O_{2}(空气)\xlongequal{高温}2CO$
②$Fe_{2}O_{3} + 3CO\xlongequal{高温}2Fe + 3CO_{2}$该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需,其主要原因是( )
A.CO过量
B.CO与铁矿石接触不充分
C.炼铁高炉的高度不够
D.CO与Fe₂O₃的反应有一定限度
①$2C(焦炭)+O_{2}(空气)\xlongequal{高温}2CO$
②$Fe_{2}O_{3} + 3CO\xlongequal{高温}2Fe + 3CO_{2}$该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需,其主要原因是( )
A.CO过量
B.CO与铁矿石接触不充分
C.炼铁高炉的高度不够
D.CO与Fe₂O₃的反应有一定限度
答案:
D [高炉炼铁的反应$Fe_{2}O_{3} + 3CO\xlongequal{高温}2Fe + 3CO_{2}$为可逆反应,所以对焦炭的实际使用量要远高于按化学方程式计算所需,这样可以提高CO的浓度,促进该反应正向移动。]
5.(1)Al与Fe₃O₄发生铝热反应的化学方程式为______________________________
______________________________,该反应中氧化剂是__________,还原剂是__________。
(2)工业上电解冶炼铝的化学方程式为______________________________。
若电路中通过1 mol电子,可以得到Al__________g。
______________________________,该反应中氧化剂是__________,还原剂是__________。
(2)工业上电解冶炼铝的化学方程式为______________________________。
若电路中通过1 mol电子,可以得到Al__________g。
答案:
(1)$8Al + 3Fe_{3}O_{4}\xlongequal{高温}4Al_{2}O_{3} + 9Fe$ $Fe_{3}O_{4}$ Al (2)$2Al_{2}O_{3}(熔融)\xlongequal[冰晶石]{电解}4Al + 3O_{2}\uparrow$ 9
查看更多完整答案,请扫码查看


