第41页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
8.将$3.84\ g\ Cu$和一定量的浓$HNO_{3}$反应,当$Cu$反应完全时,共收集到气体$2.24\ L\ NO_{2}$和$NO$(标准状况,不考虑$NO_{2}$转化为$N_{2}O_{4}$),则反应中消耗$HNO_{3}$的物质的量为 ( )
A.0.1 mol
B.0.24 mol
C.0.16 mol
D.0.22 mol
A.0.1 mol
B.0.24 mol
C.0.16 mol
D.0.22 mol
答案:
D [铜与硝酸反应转化为Cu(NO₃)₂、NO和NO₂,根据铜原子守恒n[Cu(NO₃)₂]=n(Cu)=3.84 g÷64 g·mol⁻¹ = 0.06 mol,NO和NO₂的物质的量共为n = V÷Vₘ = 2.24 L÷22.4 L·mol⁻¹ = 0.1 mol,根据氮原子守恒:n(HNO₃)=2n[Cu(NO₃)₂]+n(NO)+n(NO₂)=2×0.06 mol + 0.1 mol = 0.22 mol。]
9.将$14\ g$铜银合金与足量的硝酸反应,放出的气体与标准状况下体积为$1.12\ L$的$O_{2}$混合后再通入水中,恰好全部吸收,则合金中铜的质量为 ( )
A.4.8 g
B.3.2 g
C.6.4 g
D.10.8 g
A.4.8 g
B.3.2 g
C.6.4 g
D.10.8 g
答案:
B
10.100 mL某混合酸中,$c(HNO_{3})$为$0.3\ mol/L$,$c(H_{2}SO_{4})$为$0.25\ mol/L$。向其中加入$3.2\ g$铜粉,待充分反应后,忽略溶液体积变化,下列说法正确的是 ( )
A.反应后溶液中$c(Cu^{2+})$为$0.45\ mol/L$
B.标准状况下,生成$NO$的体积为$224\ mL$
C.反应中转移$0.09\ mol$电子
D.反应后铜有剩余,加足量稀硫酸,铜减少,但仍然有剩余
A.反应后溶液中$c(Cu^{2+})$为$0.45\ mol/L$
B.标准状况下,生成$NO$的体积为$224\ mL$
C.反应中转移$0.09\ mol$电子
D.反应后铜有剩余,加足量稀硫酸,铜减少,但仍然有剩余
答案:
D [3.2 g铜粉的物质的量为n(Cu)=3.2 g÷64 g/mol = 0.05 mol,混合溶液中n(H⁺)=100 mL×10⁻³ L/mL×0.3 mol/L + 100 mL×10⁻³ L/mL×0.25 mol/L×2 = 0.08 mol,n(NO₃⁻)=0.03 mol,根据3Cu + 8H⁺ + 2NO₃⁻ = 3Cu²⁺ + 2NO↑ + 4H₂O,H⁺不足,Cu和NO₃⁻过量,按照H⁺进行计算,据此分析。A项,根据上述分析,H⁺不足,Cu和NO₃⁻过量,按照H⁺进行计算,充分反应后,溶液中n(Cu²⁺)=0.03 mol,即c(Cu²⁺)=0.03 mol÷0.1 L = 0.3 mol/L;B项,根据上述分析,标准状况下,产生NO的体积为0.08 mol÷8×2×22.4 L/mol = 0.448 L,即产生标准状况下NO的体积为448 mL;C项,根据B选项分析,生成NO的物质的量为0.02 mol,即转移电子物质的量为0.02 mol×(5 - 2)=0.06 mol;D项,根据上述分析,反应后剩余铜粉的物质的量为0.02 mol,剩余n(NO₃⁻)=0.01 mol,加入足量稀硫酸时,0.01 mol NO₃⁻全部反应时消耗Cu的物质的量为0.01 mol×3÷2 = 0.015<0.02 mol,因此加入足量稀硫酸时,铜减少,但仍然有剩余。]
11.向$13.6\ g$由$Cu$和$Cu_{2}O$组成的混合物中加入一定浓度的稀硝酸$250\ mL$,当固体物质完全溶解后生成$Cu(NO_{3})_{2}$和$NO$气体。在所得溶液中加入$0.5\ mol·L^{-1}$的$NaOH$溶液$1.0\ L$,生成沉淀的质量为$19.6\ g$,此时溶液呈中性且金属离子已完全沉淀。下列有关说法正确的是 ( )
A.原固体混合物中$Cu$和$Cu_{2}O$的物质的量之比为1∶1
B.原稀硝酸中$HNO_{3}$的物质的量浓度为$1.3\ mol·L^{-1}$
C.产生$NO$的体积为$2.24\ L$
D.$Cu$、$Cu_{2}O$与硝酸反应后剩余的$HNO_{3}$为$0.1\ mol$
A.原固体混合物中$Cu$和$Cu_{2}O$的物质的量之比为1∶1
B.原稀硝酸中$HNO_{3}$的物质的量浓度为$1.3\ mol·L^{-1}$
C.产生$NO$的体积为$2.24\ L$
D.$Cu$、$Cu_{2}O$与硝酸反应后剩余的$HNO_{3}$为$0.1\ mol$
答案:
D
12.下列各组物质混合后(必要时可提供加热条件),最终只能得到一种气体产物的是( )
A.足量的铜与浓硝酸
B.足量的木炭与浓硫酸
C.足量的铜与浓硫酸
D.足量的锌与浓硫酸
A.足量的铜与浓硝酸
B.足量的木炭与浓硫酸
C.足量的铜与浓硫酸
D.足量的锌与浓硫酸
答案:
C [A项,先得到NO₂后得到NO;B项,得到CO₂、SO₂;C项,只能得到SO₂;D项,先得到SO₂后得到H₂。]
13.用$N_{A}$表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.50 mL 18.4 mol·L^{-1}的浓硫酸与足量的铜在加热条件下反应,生成$SO_{2}$分子的数目为$0.46N_{A}$
B.3.2 g Cu与足量浓硝酸反应生成的气体为$0.2\ mol$
C.在标准状况下,含$4\ mol\ HCl$的浓盐酸与足量的$MnO_{2}$反应可生成$22.4\ L$氯气
D.1 mol Cu在加热条件下与足量浓硫酸反应产生$1\ mol\ SO_{2}$
A.50 mL 18.4 mol·L^{-1}的浓硫酸与足量的铜在加热条件下反应,生成$SO_{2}$分子的数目为$0.46N_{A}$
B.3.2 g Cu与足量浓硝酸反应生成的气体为$0.2\ mol$
C.在标准状况下,含$4\ mol\ HCl$的浓盐酸与足量的$MnO_{2}$反应可生成$22.4\ L$氯气
D.1 mol Cu在加热条件下与足量浓硫酸反应产生$1\ mol\ SO_{2}$
答案:
D
14.将相同质量的铜分别与过量浓硝酸、稀硝酸反应,下列叙述正确的是 ( )
A.消耗硝酸的物质的量:前者少,后者多
B.反应中转移的电子总数:两者相同
C.反应速率:两者相同
D.反应生成气体的颜色:前者浅,后者深
A.消耗硝酸的物质的量:前者少,后者多
B.反应中转移的电子总数:两者相同
C.反应速率:两者相同
D.反应生成气体的颜色:前者浅,后者深
答案:
B
15.下列有关浓硫酸、浓盐酸、浓硝酸的认识正确的是 ( )
A.浓硫酸、浓硝酸与金属反应时,主要是$S$或$N$得电子
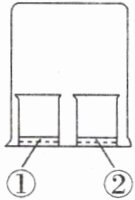
B.如图,①中为三种酸的一种,②中为浓氨水,则大烧杯中均观察到白烟
C.浓盐酸、浓硫酸都可用来干燥氧气
D.常温下,浓硫酸或浓硝酸中投入$Fe$片,均会产生大量的气体

A.浓硫酸、浓硝酸与金属反应时,主要是$S$或$N$得电子
B.如图,①中为三种酸的一种,②中为浓氨水,则大烧杯中均观察到白烟
C.浓盐酸、浓硫酸都可用来干燥氧气
D.常温下,浓硫酸或浓硝酸中投入$Fe$片,均会产生大量的气体
答案:
A [浓硫酸、浓硝酸均有强氧化性,与金属反应时,主要是S或N得电子,A正确;浓硫酸是难挥发性酸,B错;浓盐酸没有吸水性,C错;常温下,Fe在浓硫酸、浓硝酸中钝化,D错。]
查看更多完整答案,请扫码查看


