第6页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
8.如图所示是一套检验气体性质的实验装置。向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化而澄清的石灰水变浑浊;若打开活塞,则品红溶液褪色。据此判断气体X和洗气瓶内溶液Y分别可能为( )
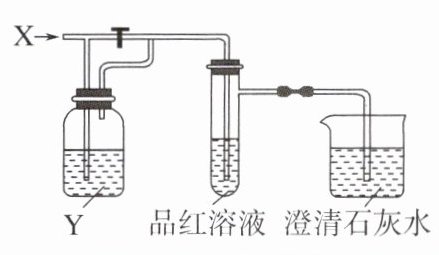
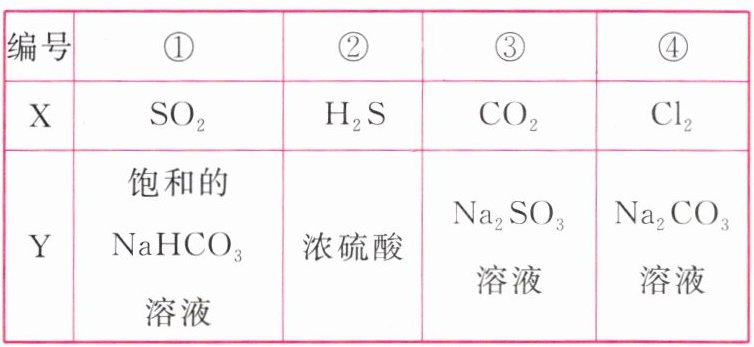
A.①④
B.①②
C.②③
D.③④


A.①④
B.①②
C.②③
D.③④
答案:
A
9.实验室用Na₂SO₃和70%的硫酸溶液反应制取SO₂,某研究性学习小组设计如图实验,制取并探究SO₂的性质。
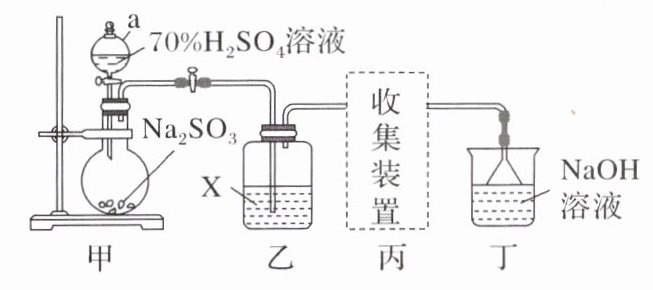
(1)丁装置的作用是___。
(2)实验中若生成标准状况1.12 L SO₂,则至少需要___g Na₂SO₃。
(3)①若X是品红溶液,气体通过乙装置,观察到的现象是___。
②若X是酸性KMnO₄溶液,气体通过乙装置,观察到溶液褪色,说明SO₂具有___。
A.酸性 B.还原性 C.漂白性
③若X是FeCl₃和BaCl₂的混合溶液,气体通过乙装置,观察到溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生,白色沉淀化学式为___。
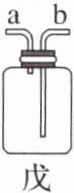
④若X是浓硫酸,用于干燥SO₂气体,在丙处选用如图戊所示的收集装置,A、B两位同学的连接方式为
A同学:SO₂气体从a导管通入集气瓶中。
B同学:SO₂气体从b导管通入集气瓶中。
正确的收集装置是___(填“A”或“B”)同学的连接方式。
⑤若X是硫化氢水溶液(氢硫酸),气体通过乙装置,观察到的现象是___,发生的化学方程式为___。

(1)丁装置的作用是___。
(2)实验中若生成标准状况1.12 L SO₂,则至少需要___g Na₂SO₃。
(3)①若X是品红溶液,气体通过乙装置,观察到的现象是___。
②若X是酸性KMnO₄溶液,气体通过乙装置,观察到溶液褪色,说明SO₂具有___。
A.酸性 B.还原性 C.漂白性
③若X是FeCl₃和BaCl₂的混合溶液,气体通过乙装置,观察到溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生,白色沉淀化学式为___。

④若X是浓硫酸,用于干燥SO₂气体,在丙处选用如图戊所示的收集装置,A、B两位同学的连接方式为
A同学:SO₂气体从a导管通入集气瓶中。
B同学:SO₂气体从b导管通入集气瓶中。
正确的收集装置是___(填“A”或“B”)同学的连接方式。
⑤若X是硫化氢水溶液(氢硫酸),气体通过乙装置,观察到的现象是___,发生的化学方程式为___。
答案:
(1) 吸收二氧化硫,防止污染空气
(2) 6.3
(3) ①品红溶液褪色 ②B ③BaSO₄
(4) B
(5) 有淡黄色沉淀生成 2H₂S + SO₂ = 3S↓ + 2H₂O
(1) 吸收二氧化硫,防止污染空气
(2) 6.3
(3) ①品红溶液褪色 ②B ③BaSO₄
(4) B
(5) 有淡黄色沉淀生成 2H₂S + SO₂ = 3S↓ + 2H₂O
10.某化学实验小组的同学为探究和比较SO₂和氯水的漂白性,设计了如下的实验装置。
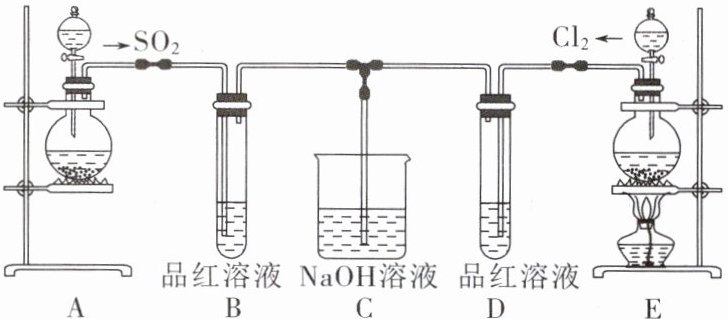
(1)实验室用装置A制备SO₂。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:___;
(2)实验室用装置E制备Cl₂,其反应的化学方程式为MnO₂ + 4HCl(浓)$\frac{\triangle}{}$MnCl₂ + Cl₂↑ + 2H₂O。若有6 mol的HCl参加反应,则转移的电子总数为___;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是B:___,D:___;
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:___,D:___。

(1)实验室用装置A制备SO₂。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:___;
(2)实验室用装置E制备Cl₂,其反应的化学方程式为MnO₂ + 4HCl(浓)$\frac{\triangle}{}$MnCl₂ + Cl₂↑ + 2H₂O。若有6 mol的HCl参加反应,则转移的电子总数为___;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是B:___,D:___;
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:___,D:___。
答案:
解析
(1) A中分液漏斗的玻璃塞没有取下,漏斗内气体与空气不连通,故打开活塞后液体不能流下。
(2) 根据制取Cl₂的反应原理可知,每生成1 mol Cl₂,消耗4 mol HCl,转移2 mol电子,故有6 mol HCl参加反应,则转移3 mol电子。
(3) SO₂具有漂白性,可使品红溶液褪色,但其漂白性是可逆的。加热后会恢复原来的颜色;Cl₂通入品红溶液时与H₂O反应生成HCl和HClO,HClO具有强氧化性,会把品红氧化而褪色,且该过程不可逆,故加热不会恢复原来的颜色。 答案
(1) 分液漏斗的玻璃塞没有取下来
(2) 3Nₐ
(3) ①褪色 褪色 ②褪色的品红溶液又恢复成红色 无明显现象
(1) A中分液漏斗的玻璃塞没有取下,漏斗内气体与空气不连通,故打开活塞后液体不能流下。
(2) 根据制取Cl₂的反应原理可知,每生成1 mol Cl₂,消耗4 mol HCl,转移2 mol电子,故有6 mol HCl参加反应,则转移3 mol电子。
(3) SO₂具有漂白性,可使品红溶液褪色,但其漂白性是可逆的。加热后会恢复原来的颜色;Cl₂通入品红溶液时与H₂O反应生成HCl和HClO,HClO具有强氧化性,会把品红氧化而褪色,且该过程不可逆,故加热不会恢复原来的颜色。 答案
(1) 分液漏斗的玻璃塞没有取下来
(2) 3Nₐ
(3) ①褪色 褪色 ②褪色的品红溶液又恢复成红色 无明显现象
查看更多完整答案,请扫码查看


