第124页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
5.下列方法中可以证明乙醇分子中有一个氢原子与其他氢原子不同的是 ( )
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以和水任意比互溶
C.1 mol乙醇跟足量的Na作用得0.5 mol $H_2$
D.乙醇可被酸性$KMnO_4$溶液氧化为乙酸$(CH_3COOH)$
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以和水任意比互溶
C.1 mol乙醇跟足量的Na作用得0.5 mol $H_2$
D.乙醇可被酸性$KMnO_4$溶液氧化为乙酸$(CH_3COOH)$
答案:
C
6.维生素C的结构简式如图所示,有关它的叙述不正确的是 ( )<ImageHere6></Img>
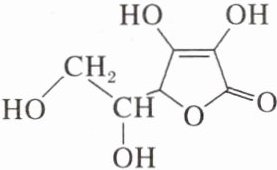
A.能使溴水褪色
B.在任何条件下都能稳定存在
C.易被氧化,是一种较强的还原剂,又叫抗坏血酸
D.能促进伤口愈合,但人体不能合成,通常从食物中获得

A.能使溴水褪色
B.在任何条件下都能稳定存在
C.易被氧化,是一种较强的还原剂,又叫抗坏血酸
D.能促进伤口愈合,但人体不能合成,通常从食物中获得
答案:
B
7.乙醇催化氧化制取乙醛(沸点为20.8℃,能与水混溶)的装置(夹持装置已略)如图所示。下列说法错误的是 ( )<ImageHere7></Img>
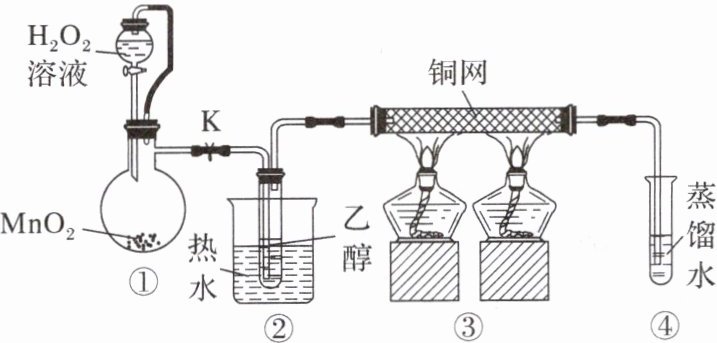
A.①中用胶管连接的作用是平衡气压,便于液体顺利流下
B.实验过程中铜丝会出现红黑交替变化
C.实验开始时需先加热②,再通$O_2$,然后加热③
D.实验结束时需先将④中的导管移出,再停止加热

A.①中用胶管连接的作用是平衡气压,便于液体顺利流下
B.实验过程中铜丝会出现红黑交替变化
C.实验开始时需先加热②,再通$O_2$,然后加热③
D.实验结束时需先将④中的导管移出,再停止加热
答案:
C [A项,当分液漏斗上部压强大于烧瓶内压强时,分液漏斗内液体才能顺利流下,所以用胶管连接起到平衡气压,使液体顺利流下的作用;B项,反应中存在铜被氧化生成氧化铜,氧化铜与乙醇反应生成铜,铜丝出现红黑交替变化的现象;C项,实验时应先加热③,以起到预热的作用,使乙醇充分反应;D项,实验结束时需先将④中的导管移出,再停止加热,防止发生倒吸。]
8.乙醇、乙酸分子中的各种化学键如图所示,下列反应中断键的位置错误的是 ( )<ImageHere8></Img>
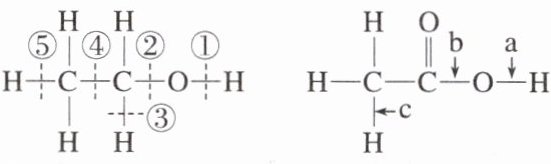
A.乙醇与金属钠反应,断裂①键
B.乙酸与乙醇发生酯化反应,断裂②键、a键
C.乙醇在铜催化共热下与$O_2$反应,断裂①③键
D.乙酸变成乙酸酐的反应$2CH_3COOH\rightarrow (CH_3CO)_2O + H_2O$,断裂a、b键
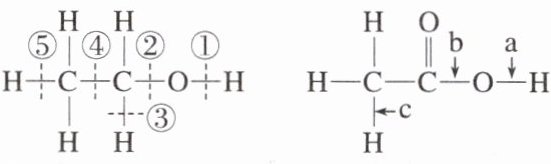
A.乙醇与金属钠反应,断裂①键
B.乙酸与乙醇发生酯化反应,断裂②键、a键
C.乙醇在铜催化共热下与$O_2$反应,断裂①③键
D.乙酸变成乙酸酐的反应$2CH_3COOH\rightarrow (CH_3CO)_2O + H_2O$,断裂a、b键
答案:
B
9.为测定乙醇的结构式,有人设计了用无水乙醇与钠反应的实验装置和测定氢气体积的装置进行实验,可供选用的实验装置如图所示。
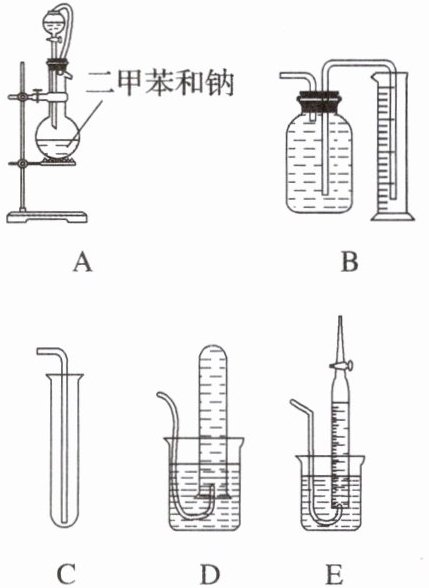
请回答以下问题:
(1)测量氢气体积的最佳装置是 (填字母)。
(2)装置A的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是 (填字母)。
A.防止无水乙醇挥发
B.保证实验装置不漏气
C.使无水乙醇容易滴下
D.减少测量实验误差
(3)实验前预先使小块钠在二甲苯中熔化成若干个小钠球,冷却后再倒入烧瓶中,其目的是 。
(4)已知无水乙醇的密度为0.789 g·$cm^{-3}$,移取2.0 mL乙醇,反应完全后(钠过量),收集到390 mL(已折算为标准状况)气体。则一个乙醇分子中能被钠原子置换的氢原子数为 ,由此可确定乙醇的结构式为 ,而不是 。

请回答以下问题:
(1)测量氢气体积的最佳装置是 (填字母)。
(2)装置A的分液漏斗与蒸馏烧瓶之间连接的导管所起的作用是 (填字母)。
A.防止无水乙醇挥发
B.保证实验装置不漏气
C.使无水乙醇容易滴下
D.减少测量实验误差
(3)实验前预先使小块钠在二甲苯中熔化成若干个小钠球,冷却后再倒入烧瓶中,其目的是 。
(4)已知无水乙醇的密度为0.789 g·$cm^{-3}$,移取2.0 mL乙醇,反应完全后(钠过量),收集到390 mL(已折算为标准状况)气体。则一个乙醇分子中能被钠原子置换的氢原子数为 ,由此可确定乙醇的结构式为 ,而不是 。
答案:
解析 (1)氢气不溶于水,可用排水法测量氢气的体积。C装置无法测量氢气的体积,D装置中试管无刻度,E装置测量最准确,但容积受限。(3)要准确测定乙醇和钠反应生成的氢气的量与乙醇的量之间的关系,钠必须过量。又因为钠的化学性质很活泼,容易与空气中的氧气、水蒸气发生反应,故实验时应预先使小块钠在二甲苯中熔化成若干个小钠球,从而防止钠与空气反应干扰实验,且可增大乙醇与钠的接触面积,加快反应速率。(4)由题意知,$n(乙醇)=\frac{0.789\ g\cdot cm^{-3}\times2.0\ mL}{46\ g\cdot mol}=0.0343\ mol$,$n(H)=\frac{0.390\ mL}{22.4\ L\cdot mol^{-1}}\times2 = 0.0348\ mol$,则$n(乙醇):n(H)=1:1$,则一个乙醇分子中能被钠原子置换的氢原子数为1,由此得出乙醇的结构式应为$H-\underset{\underset{H}{\vert }}{C}-\underset{\underset{H}{\vert }}{C}-O-H$,而不是$H-\underset{\underset{H}{\vert }}{C}-O-\underset{\underset{H}{\vert }}{C}-H$。
答案 (1)B (2)CD (3)防止钠与空气反应干扰实验,同时增大无水乙醇与钠的接触面积,加快反应速率 (4)1 $H-\underset{\underset{H}{\vert }}{C}-\underset{\underset{H}{\vert }}{C}-O-H$ $H-\underset{\underset{H}{\vert }}{C}-O-\underset{\underset{H}{\vert }}{C}-H$
查看更多完整答案,请扫码查看


