第16页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
1.下列实验中能证明某气体为SO₂的是( )
①使澄清石灰水变浑浊
②使湿润的蓝色石蕊试纸变红
③使品红溶液褪色
④通入足量NaOH溶液中,再滴加BaCl₂溶液,有白色沉淀生成,该沉淀溶于稀盐酸
⑤通入溴水中,能使溴水褪色,再滴加Ba(NO₃)₂溶液有白色沉淀产生
A.都能证明
B.都不能证明
C.③④⑤均能证明
D.只有⑤能证明
①使澄清石灰水变浑浊
②使湿润的蓝色石蕊试纸变红
③使品红溶液褪色
④通入足量NaOH溶液中,再滴加BaCl₂溶液,有白色沉淀生成,该沉淀溶于稀盐酸
⑤通入溴水中,能使溴水褪色,再滴加Ba(NO₃)₂溶液有白色沉淀产生
A.都能证明
B.都不能证明
C.③④⑤均能证明
D.只有⑤能证明
答案:
D
2.吸烟有害健康,因为香烟烟雾中含有CO、CO₂、SO₂、H₂O等气体,用①无水硫酸铜、②澄清石灰水、③红热氧化铜、④碱石灰、⑤品红溶液、⑥足量酸性高锰酸钾溶液等可将其一一检出,检出的正确顺序是 ( )
A.混合气→①→⑤→②→①→④→③
B.混合气→③→④→②→⑥→⑤→①
C.混合气→①→⑤→⑥→②→④→③
D.混合气→②→⑤→①→④→③→⑥
A.混合气→①→⑤→②→①→④→③
B.混合气→③→④→②→⑥→⑤→①
C.混合气→①→⑤→⑥→②→④→③
D.混合气→②→⑤→①→④→③→⑥
答案:
C
3.下列四种有色溶液与SO₂作用,均能褪色,其实质相同的是 ( )
①品红溶液 ②酸性KMnO₄溶液
③溴水 ④滴有酚酞的NaOH溶液
A.①④
B.②③
C.②③④
D.①②③
①品红溶液 ②酸性KMnO₄溶液
③溴水 ④滴有酚酞的NaOH溶液
A.①④
B.②③
C.②③④
D.①②③
答案:
B
4.下列说法正确的是 ( )
A.浓硫酸和浓盐酸长期露置在空气中浓度降低,其原因相同
B.SO₂、漂白粉、活性炭、过氧化钠都能使红墨水褪色,其原理相同
C.漂白粉和氢氧化钠长期露置在空气中变质,反应原理相同
D.能使品红溶液褪色的气体不一定是SO₂
A.浓硫酸和浓盐酸长期露置在空气中浓度降低,其原因相同
B.SO₂、漂白粉、活性炭、过氧化钠都能使红墨水褪色,其原理相同
C.漂白粉和氢氧化钠长期露置在空气中变质,反应原理相同
D.能使品红溶液褪色的气体不一定是SO₂
答案:
D [浓硫酸具有吸水性,溶剂增多,浓盐酸具有挥发性,溶质减少,即二者浓度减小的原因不同,A项错误;漂白粉、过氧化钠具有强氧化性,活性炭具有吸附性,SO₂与有色物质化合体现其漂白性,漂白原理不完全相同,B项错误;漂白粉与二氧化碳和水反应生成HClO,HClO易分解,氢氧化钠和二氧化碳反应生成碳酸钠,即反应原理不相同,C项错误;具有漂白性的物质可使品红溶液褪色,如氯气、二氧化硫等,所以能使品红溶液褪色的气体不一定是SO₂,D项正确。]
5.某化学兴趣小组在实验室探究SO₂的相关性质。
Ⅰ.制备并收集SO₂气体
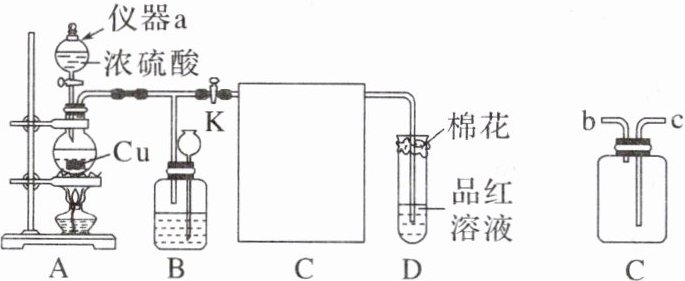
(1)仪器a的名称为 ,装置A中发生反应的化学方程式为 。
(2)把如图装置C接回如图装置中,按照从左往右的顺序应该先连接 (填“b”或“c”),当D中出现 现象时,证明气体已集满,停止加热。装置D中试管口的棉花应提前在氢氧化钠溶液中浸湿,其作用是 。
Ⅱ.探究SO₂的性质
将SO₂分别通入下列五种溶液中
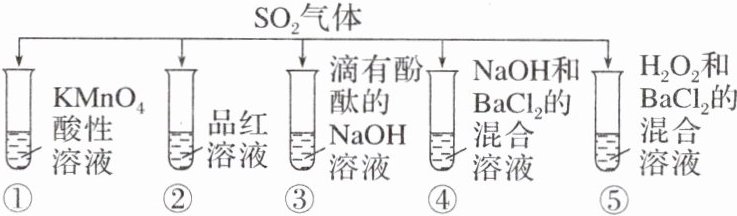
回答下列问题:
(3)试管①中的实验现象:KMnO₄酸性溶液 ,证明SO₂具有 性。
(4)试管④中的实验现象:溶液 ,写出该反应的离子方程式: 。
Ⅰ.制备并收集SO₂气体

(1)仪器a的名称为 ,装置A中发生反应的化学方程式为 。
(2)把如图装置C接回如图装置中,按照从左往右的顺序应该先连接 (填“b”或“c”),当D中出现 现象时,证明气体已集满,停止加热。装置D中试管口的棉花应提前在氢氧化钠溶液中浸湿,其作用是 。
Ⅱ.探究SO₂的性质
将SO₂分别通入下列五种溶液中

回答下列问题:
(3)试管①中的实验现象:KMnO₄酸性溶液 ,证明SO₂具有 性。
(4)试管④中的实验现象:溶液 ,写出该反应的离子方程式: 。
答案:
解析
(1) 仪器a的名称为分液漏斗,装置A中铜和浓硫酸反应生成硫酸铜和水、二氧化硫,化学方程式为Cu + 2H₂SO₄(浓)$\xlongequal{\triangle}$CuSO₄ + 2H₂O + SO₂↑;
(2) 二氧化硫密度大于空气,应该使用向上排空气法收集,装置C中应该长进短出,故按从左往右的顺序装置C应该先接c,当D中出现品红溶液红色褪去的现象时,证明气体已集满,停止加热。二氧化硫有毒且能和氢氧化钠反应,装置D中试管口的棉花应提前在氢氧化钠溶液中浸湿,其作用是吸收尾气,减少污染;
(3) 高锰酸钾具有强氧化性,二氧化硫和酸性高锰酸钾反应生成硫酸根离子和锰离子,使得KMnO₄酸性溶液褪色,证明SO₂具有还原性。
(4) 二氧化硫和氢氧化钠生成亚硫酸钠,亚硫酸钠和氯化钡生成亚硫酸钡白色沉淀,故试管④中的实验现象:溶液变浑浊生成白色沉淀,该反应的离子方程式:SO₂ + 2OH⁻ + Ba²⁺$\xlongequal{}$BaSO₃↓ + H₂O。 答案
(1) 分液漏斗 Cu + 2H₂SO₄(浓)$\xlongequal{\triangle}$CuSO₄ + 2H₂O + SO₂↑
(2) c 品红溶液红色褪去 吸收尾气
(3) 褪色 还原
(4) 变浑浊生成白色沉淀 SO₂ + 2OH⁻ + Ba²⁺$\xlongequal{}$BaSO₃↓ + H₂O
(1) 仪器a的名称为分液漏斗,装置A中铜和浓硫酸反应生成硫酸铜和水、二氧化硫,化学方程式为Cu + 2H₂SO₄(浓)$\xlongequal{\triangle}$CuSO₄ + 2H₂O + SO₂↑;
(2) 二氧化硫密度大于空气,应该使用向上排空气法收集,装置C中应该长进短出,故按从左往右的顺序装置C应该先接c,当D中出现品红溶液红色褪去的现象时,证明气体已集满,停止加热。二氧化硫有毒且能和氢氧化钠反应,装置D中试管口的棉花应提前在氢氧化钠溶液中浸湿,其作用是吸收尾气,减少污染;
(3) 高锰酸钾具有强氧化性,二氧化硫和酸性高锰酸钾反应生成硫酸根离子和锰离子,使得KMnO₄酸性溶液褪色,证明SO₂具有还原性。
(4) 二氧化硫和氢氧化钠生成亚硫酸钠,亚硫酸钠和氯化钡生成亚硫酸钡白色沉淀,故试管④中的实验现象:溶液变浑浊生成白色沉淀,该反应的离子方程式:SO₂ + 2OH⁻ + Ba²⁺$\xlongequal{}$BaSO₃↓ + H₂O。 答案
(1) 分液漏斗 Cu + 2H₂SO₄(浓)$\xlongequal{\triangle}$CuSO₄ + 2H₂O + SO₂↑
(2) c 品红溶液红色褪去 吸收尾气
(3) 褪色 还原
(4) 变浑浊生成白色沉淀 SO₂ + 2OH⁻ + Ba²⁺$\xlongequal{}$BaSO₃↓ + H₂O
查看更多完整答案,请扫码查看


