第64页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
1. 火箭所需要的巨大能量由特制的燃料来提供,有关燃料燃烧过程中的变化,下列说法不正确的是 ( )
A. 所有的燃烧过程均是放热的
B. 需要点燃才能发生的燃烧过程是吸热的
C. 所有燃料在燃烧过程中均会发生化学键的断裂
D. 燃烧后产物的总能量一定小于反应物的总能量
A. 所有的燃烧过程均是放热的
B. 需要点燃才能发生的燃烧过程是吸热的
C. 所有燃料在燃烧过程中均会发生化学键的断裂
D. 燃烧后产物的总能量一定小于反应物的总能量
答案:
B [A项,燃烧反应反应物的总能量高于生成物的总能量,都是放热反应;B项,根据A选项的分析,所有的燃烧过程均是放热的;C项,燃烧是化学变化,化学变化从微观上看是旧键断裂新键形成的过程,因此燃料在燃烧过程中均会发生化学键的断裂;D项,燃烧为放热反应,产物的总能量一定小于反应物的总能量。]
2. 氢气在氯气中燃烧产生苍白色火焰。在反应过程中,破坏 1 mol 氢气中的化学键消耗的能量为$Q_{1}$kJ,破坏 1 mol 氯气中的化学键消耗的能量为$Q_{2}$kJ,形成 1 mol 氯化氢中的化学键释放的能量为$Q_{3}$kJ。下列关系式中正确的是 ( )
A. $Q_{1}+Q_{2}<2Q_{3}$
B. $Q_{1}+Q_{2}>Q_{3}$
C. $Q_{1}+Q_{2}<Q_{3}$
D. $Q_{1}+Q_{2}>2Q_{3}$
A. $Q_{1}+Q_{2}<2Q_{3}$
B. $Q_{1}+Q_{2}>Q_{3}$
C. $Q_{1}+Q_{2}<Q_{3}$
D. $Q_{1}+Q_{2}>2Q_{3}$
答案:
A [由于Cl₂和H₂反应生成HCl要放出热量,所以Q₁ + Q₂<2Q₃。]
3. 已知断开 1 mol H—H 吸收的能量为 436 kJ,形成 1 mol H—N 放出的能量为 391 kJ,根据化学方程式$N_{2}+3H_{2}\underset{催化剂}{\overset{高温、高压}{=\!=\!=}}2NH_{3}$,反应完 1 mol $N_{2}$放出的能量为 92.4 kJ,则断开 1 mol N≡N 需吸收的能量是 ( )
A. 431 kJ
B. 945.6 kJ
C. 649 kJ
D. 869 kJ
A. 431 kJ
B. 945.6 kJ
C. 649 kJ
D. 869 kJ
答案:
B [设断开1 mol N≡N需吸收的能量为x,根据反应放出的能量 = 形成新键放出的能量 - 断开旧键吸收的能量,代入数据:92.4 kJ = 6×391 kJ - 3×436 kJ - x,x = 945.6 kJ。]
4. 根据下面的信息,判断下列叙述正确的是 ( )
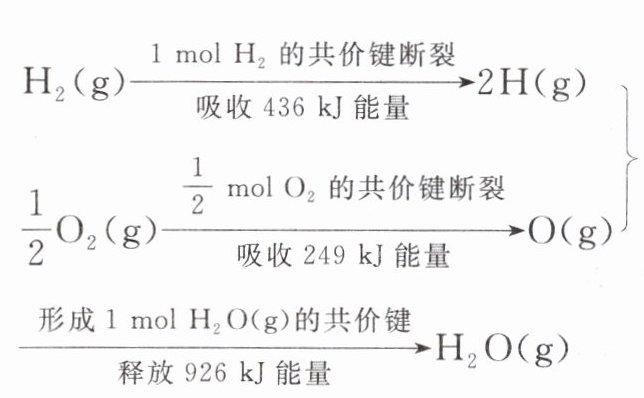
A. 氢气跟氧气反应生成水的同时释放能量
B. 1 mol $H_{2}(g)$和$\frac{1}{2}$mol $O_{2}(g)$的能量低于 1 mol $H_{2}O(g)$的能量
C. 1 mol $H_{2}(g)$和$\frac{1}{2}$mol $O_{2}(g)$反应生成 1 mol $H_{2}O$一定释放能量 241 kJ
D. 2 mol $H_{2}(g)$跟 1 mol $O_{2}(g)$反应生成 2 mol $H_{2}O(g)$吸收能量 482 kJ

A. 氢气跟氧气反应生成水的同时释放能量
B. 1 mol $H_{2}(g)$和$\frac{1}{2}$mol $O_{2}(g)$的能量低于 1 mol $H_{2}O(g)$的能量
C. 1 mol $H_{2}(g)$和$\frac{1}{2}$mol $O_{2}(g)$反应生成 1 mol $H_{2}O$一定释放能量 241 kJ
D. 2 mol $H_{2}(g)$跟 1 mol $O_{2}(g)$反应生成 2 mol $H_{2}O(g)$吸收能量 482 kJ
答案:
A
5. 化学反应$H_{2}(g)+Cl_{2}(g)\xlongequal{\;\;}2HCl(g)$(“g”表示气体)的能量变化如图所示,则下列说法中正确的是 ( )
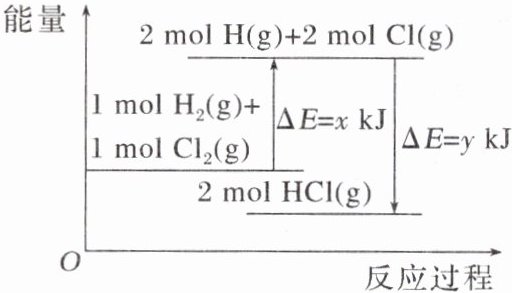
A. 该反应是吸热反应
B. 断裂 1 mol H—H 和 1 mol Cl—Cl 时放出$x$kJ 的能量
C. 断裂 2 mol H—Cl 时需要吸收$y$kJ 的能量
D. 生成 2 mol HCl(g)放出的能量为$(x - y)$kJ

A. 该反应是吸热反应
B. 断裂 1 mol H—H 和 1 mol Cl—Cl 时放出$x$kJ 的能量
C. 断裂 2 mol H—Cl 时需要吸收$y$kJ 的能量
D. 生成 2 mol HCl(g)放出的能量为$(x - y)$kJ
答案:
C [由题图可知反应物的总能量大于生成物的总能量,所以该反应为放热反应,A错误;断键要吸收能量,所以断裂1 mol H—H和1 mol Cl—Cl吸收x kJ能量,B错误;由题图可知,断裂2 mol H—Cl需要吸收y kJ的能量,C正确;由题图可知,反应生成2 mol HCl,放出的能量为(y - x)kJ,D错误。]
查看更多完整答案,请扫码查看


