第4页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
课堂·即时达标
1.硫单质能与许多金属单质和非金属单质发生反应。下列说法正确的是( )
A.硫蒸气与红热的铁丝反应后,残留的硫可用二硫化碳洗涤
B.硫蒸气与红热的铜丝反应生成黑色的CuS固体
C.硫单质在化合反应中只体现氧化性
D.硫元素广泛存在于自然界中,火山口附近的环境中硫元素只以游离态形式存在
1.硫单质能与许多金属单质和非金属单质发生反应。下列说法正确的是( )
A.硫蒸气与红热的铁丝反应后,残留的硫可用二硫化碳洗涤
B.硫蒸气与红热的铜丝反应生成黑色的CuS固体
C.硫单质在化合反应中只体现氧化性
D.硫元素广泛存在于自然界中,火山口附近的环境中硫元素只以游离态形式存在
答案:
A [A项,硫蒸气与红热的铁丝反应产生FeS,残留的硫易溶于CS₂,因此可用二硫化碳洗涤未反应的硫单质;B项,S单质氧化性比较弱,硫蒸气与红热的铜丝反应生成黑色的Cu₂S固体;C项,硫单质与氧气反应时,硫单质体现还原性;与H₂反应产生H₂S时表现氧化性;D项,火山口附近的环境中也存在化合态的硫。]
2.下列有关SO₂说法正确的是( )
A.工业上用H₂O吸收SO₂气体制备硫酸
B.SO₂是无色、无味、密度比空气大的有毒气体
C.可以用排水法收集SO₂气体
D.SO₂能使紫色的酸性KMnO₄溶液褪色
A.工业上用H₂O吸收SO₂气体制备硫酸
B.SO₂是无色、无味、密度比空气大的有毒气体
C.可以用排水法收集SO₂气体
D.SO₂能使紫色的酸性KMnO₄溶液褪色
答案:
D [A项,工业上用浓硫酸吸收SO₃来制备硫酸;B项,二氧化硫是无色、但具有刺激性气味的有毒气体;C项,SO₂易溶于水,不能用排水法收集;D项,SO₂具有还原性,能与酸性KMnO₄溶液发生氧化还原反应而使紫色的酸性KMnO₄溶液褪色。]
3.下列溶液中,不能鉴别CO₂、SO₂气体的是( )
①石灰水 ②H₂S水溶液 ③酸性KMnO₄溶液 ④溴水 ⑤氯水 ⑥品红溶液
A.①⑤
B.②③④⑤⑥
C.只有①
D.③④
①石灰水 ②H₂S水溶液 ③酸性KMnO₄溶液 ④溴水 ⑤氯水 ⑥品红溶液
A.①⑤
B.②③④⑤⑥
C.只有①
D.③④
答案:
C [SO₂和CO₂都是酸性氧化物,都能使澄清的石灰水变浑浊,但SO₂气体具有漂白性、还原性和氧化性,所以只有①不能鉴别二者。]
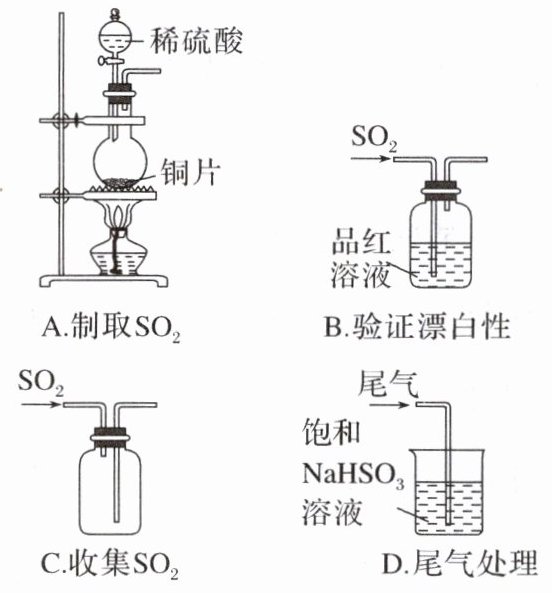
4.下列制取SO₂、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是( )

答案:
B [A项,铜片和浓硫酸在加热条件下可反应制备二氧化硫,铜片和稀硫酸不反应;B项,二氧化硫可使品红溶液褪色,可验证二氧化硫具有漂白性,能达到实验目的;C项,二氧化硫的密度比空气的大,所以应该采用向上排空气法收集,即“长管进短管出”;D项,饱和亚硫酸氢钠溶液可降低二氧化硫在水中的溶解度,不能进行尾气处理,烧杯中应该用氢氧化钠溶液。]
5.向盛有下列溶液的试管中分别通入SO₂气体:①紫色石蕊溶液;②NaOH溶液(滴有酚酞溶液);③品红溶液;④溴水。请回答下列问题:
(1)试管①中的现象是___,发生反应的化学方程式为___。
(2)试管②中的现象是___,发生反应的化学方程式为___,若继续通入过量的SO₂,则发生反应的化学方程式为___。
(3)试管③中的现象是___,若将吸收SO₂的品红溶液加热,现象是___。
(4)试管④中的现象是___。
(5)上述实验中,SO₂表现出酸性氧化物性质的是___(填序号,下同),SO₂表现出漂白性的是___,SO₂表现出还原性的是___。
(1)试管①中的现象是___,发生反应的化学方程式为___。
(2)试管②中的现象是___,发生反应的化学方程式为___,若继续通入过量的SO₂,则发生反应的化学方程式为___。
(3)试管③中的现象是___,若将吸收SO₂的品红溶液加热,现象是___。
(4)试管④中的现象是___。
(5)上述实验中,SO₂表现出酸性氧化物性质的是___(填序号,下同),SO₂表现出漂白性的是___,SO₂表现出还原性的是___。
答案:
(1) 紫色石蕊溶液变红 SO₂ + H₂O$\rightleftharpoons$H₂SO₃
(2) 溶液红色变浅,甚至褪色 SO₂ + 2NaOH = Na₂SO₃ + H₂O 、Na₂SO₃ + SO₂ + H₂O = 2NaHSO₃
(3) 品红溶液褪色 溶液恢复红色
(4) 溴水褪色
(5) ①② ③ ④
(1) 紫色石蕊溶液变红 SO₂ + H₂O$\rightleftharpoons$H₂SO₃
(2) 溶液红色变浅,甚至褪色 SO₂ + 2NaOH = Na₂SO₃ + H₂O 、Na₂SO₃ + SO₂ + H₂O = 2NaHSO₃
(3) 品红溶液褪色 溶液恢复红色
(4) 溴水褪色
(5) ①② ③ ④
查看更多完整答案,请扫码查看


