第104页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
1.下列物质都能与金属钠反应放出$H_{2}$,产生$H_{2}$的速率排序正确的是(C)
①$C_{2}H_{5}OH$ ②NaOH溶液 ③醋酸溶液
A.①>②>③
B.②>①>③
C.③>②>①
D.③>①>②
①$C_{2}H_{5}OH$ ②NaOH溶液 ③醋酸溶液
A.①>②>③
B.②>①>③
C.③>②>①
D.③>①>②
答案:
金属钠与NaOH溶液反应的实质是与溶液中的水反应;已知钠与水反应的速率比与乙醇反应得快;醋酸溶液中c(H⁺)大于H₂O中c(H⁺),所以醋酸溶液与钠反应速率更快,C项正确。
2.下列探究乙醇的有关实验,得出的结论正确的是(C)
|选项|实验步骤及现象|实验结论|
|----|----|----|
|A|在酒精试样中加入少量$CuSO_{4}\cdot 5H_{2}O$,搅拌,试管底部有蓝色晶体|酒精试样中一定含有水|
|B|在乙醇燃烧火焰上方罩一干燥的烧杯,内壁有水珠出现,另罩一内壁涂有澄清石灰水的烧杯,内壁出现白色沉淀|乙醇由C、H、O三种元素组成|
|C|将灼烧后表面变黑的螺旋状铜丝伸入约50℃的乙醇中,铜丝能保持红热一段时间|乙醇催化氧化反应是放热反应|
|D|在0.01 mol金属钠中加入过量的乙醇充分反应,收集到标准状况下气体112 mL|乙醇分子中有1个氢原子与氧原子相连,其余与碳原子相连|
|选项|实验步骤及现象|实验结论|
|----|----|----|
|A|在酒精试样中加入少量$CuSO_{4}\cdot 5H_{2}O$,搅拌,试管底部有蓝色晶体|酒精试样中一定含有水|
|B|在乙醇燃烧火焰上方罩一干燥的烧杯,内壁有水珠出现,另罩一内壁涂有澄清石灰水的烧杯,内壁出现白色沉淀|乙醇由C、H、O三种元素组成|
|C|将灼烧后表面变黑的螺旋状铜丝伸入约50℃的乙醇中,铜丝能保持红热一段时间|乙醇催化氧化反应是放热反应|
|D|在0.01 mol金属钠中加入过量的乙醇充分反应,收集到标准状况下气体112 mL|乙醇分子中有1个氢原子与氧原子相连,其余与碳原子相连|
答案:
CuSO₄·5H₂O不能再结合水,加入后无现象,故无法证明酒精中是否含水,A错误;由现象知,乙醇燃烧生成CO₂和H₂O,可以说明乙醇中含有C、H元素,但不能确定是否含有氧元素,B错误;由现象“铜丝能保持红热一段时间”,可以说明反应为放热反应,C正确;0.01 mol Na和过量乙醇生成标准状况下112 mL氢气,但因为乙醇过量,无法确定就是一个H与O相连,D错误。
3.下列说法正确的是(B)
A.羟基与氢氧根有相同的化学式
B.1 mol —OH中含有9 mol电子
C.常温下,1 mol乙醇可与足量的Na反应生成11.2 L $H_{2}$
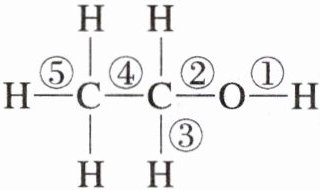
D.已知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键为②③
$H-\underset{\underset{H}{\vert }}{\overset{\overset{H}{\vert }}{C}}-\underset{\underset{H}{\vert }}{\overset{\overset{H}{\vert }}{C}}-O-H$
A.羟基与氢氧根有相同的化学式
B.1 mol —OH中含有9 mol电子
C.常温下,1 mol乙醇可与足量的Na反应生成11.2 L $H_{2}$
D.已知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键为②③
$H-\underset{\underset{H}{\vert }}{\overset{\overset{H}{\vert }}{C}}-\underset{\underset{H}{\vert }}{\overset{\overset{H}{\vert }}{C}}-O-H$

答案:
A项,羟基的化学式是—OH,电子式是·O∶H,氢氧根的化学式是OH⁻,电子式是[∶O∶H]⁻;B项,1 mol —OH中含有9 mol电子;C项,1 mol乙醇与足量的Na反应生成0.5 mol H₂,常温下气体摩尔体积不是22.4 L/mol,体积不是11.2 L;D项,乙醇催化氧化生成乙醛,断裂化学键为①③。
4.为了探究乙醇和钠反应的原理,做如下实验:
甲:向试管中加入3 mL乙醇,放入一小块钠,观察现象,并收集、检验产生的气体。
乙:向试管中加入3 mL乙醚($CH_{3}CH_{2}OCH_{2}CH_{3}$),放入一小块钠,无气体产生。
回答以下问题:
(1)简述检验实验甲中产生的气体的方法及作出判断的依据:将收集到的气体靠近酒精灯火焰,若听到“噗”的一声或发出轻微的爆鸣声,则证明该气体是氢气。
(2)从结构上分析,选取乙醚作参照物的原因是乙醚分子中含有乙基,与乙醇分子中的乙基相同,且乙醚分子中无羟基,以此对比乙醇分子中羟基的作用。
(3)实验甲说明乙醇分子中的羟基能与钠反应;实验乙说明乙醚分子中无羟基,不能与钠反应;根据实验结果,乙醇和金属钠反应的化学方程式应为$2CH_{3}CH_{2}OH + 2Na → 2CH_{3}CH_{2}ONa + H_{2}\uparrow$。
甲:向试管中加入3 mL乙醇,放入一小块钠,观察现象,并收集、检验产生的气体。
乙:向试管中加入3 mL乙醚($CH_{3}CH_{2}OCH_{2}CH_{3}$),放入一小块钠,无气体产生。
回答以下问题:
(1)简述检验实验甲中产生的气体的方法及作出判断的依据:将收集到的气体靠近酒精灯火焰,若听到“噗”的一声或发出轻微的爆鸣声,则证明该气体是氢气。
(2)从结构上分析,选取乙醚作参照物的原因是乙醚分子中含有乙基,与乙醇分子中的乙基相同,且乙醚分子中无羟基,以此对比乙醇分子中羟基的作用。
(3)实验甲说明乙醇分子中的羟基能与钠反应;实验乙说明乙醚分子中无羟基,不能与钠反应;根据实验结果,乙醇和金属钠反应的化学方程式应为$2CH_{3}CH_{2}OH + 2Na → 2CH_{3}CH_{2}ONa + H_{2}\uparrow$。
答案:
(1)试管中加入乙醇,放入一小块钠,二者会发生反应得到乙醇钠和氢气,氢气的检验方法:将收集到的气体点燃,在火焰上方罩一干燥的冷烧杯,若能燃烧或发出爆鸣声并且杯壁有水滴,则证明该气体是氢气。
(2)乙醇分子中含有乙基和羟基,乙醚分子中含有乙基和醚键,故选取乙醚作参照物,说明与钠发生反应的为羟基。
(3)乙醇分子中含有乙基和羟基,乙醚分子中含有乙基,向试管中加入3 mL乙醚(CH₃CH₂OCH₂CH₃),放入一小块钠,不发生反应,故与钠反应的物质中需含有羟基氢,羟基中的氢原子能和金属钠反应得到氢气。
查看更多完整答案,请扫码查看


