第15页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
二氧化碳的制取和性质研究
1. 教材实验原理图

2. 实验原理
原理一:CaCO₃ + 2HCl = CaCl₂ + H₂O + CO₂↑。
原理二:CO₂ + Ca(OH)₂ = CaCO₃↓ + H₂O,H₂O + CO₂ = H₂CO₃。
3. 实验结论
结论一:二氧化碳密度大于空气密度;二氧化碳不能燃烧也不支持燃烧。
结论二:二氧化碳能使澄清石灰水变浑浊。
结论三:二氧化碳的水溶液会使______试液变红。
4. 实验关键点
(1)实验仪器使用和操作过程的注意事项:长颈漏斗使用的时候需要______。
(2)若选用大理石或石灰石为原料,则不能用稀硫酸。因为生成的硫酸钙是微溶性物质,它包裹在______,从而使反应中止。
(3)收集二氧化碳的时候,集气瓶瓶口朝上,用向上排空气法,导管应伸入到集气瓶底部。若未伸入到集气瓶底部则会使收集到的气体______。
5. 实验拓展
拓展:二氧化碳与氢氧化钠反应没有沉淀、气体、颜色变化等明显现象,只有气压减小这一不易观察的现象。故探究二氧化碳性质时,必须借助其他现象来反映二氧化碳与氢氧化钠发生了反应。
起式:
教材实验:通过瓶内气压变化证明二氧化碳与水发生反应,如图所示。
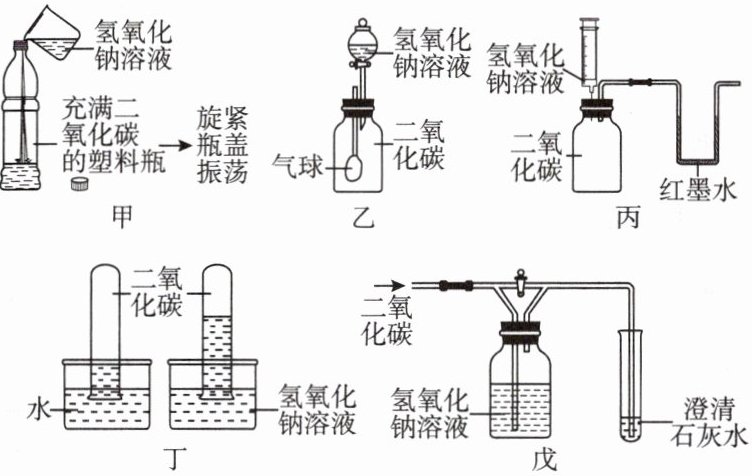
变式:
(1)使用塑料瓶,观察到塑料瓶变扁,说明瓶内二氧化碳与氢氧化钠发生了反应,如图甲所示。
(2)密闭容器中使用气球,观察气球的变化,如图乙所示。
(3)使用 U 形管,观察反应体系的气压变化,如图丙所示。

(4)使用等量的清水做对比,观察对比进入试管内液体的量确定二氧化碳与氢氧化钠发生反应,如图丁所示。
(5)使用澄清石灰水对通过氢氧化钠的二氧化碳进行检测,如图戊所示。
1. 教材实验原理图

2. 实验原理
原理一:CaCO₃ + 2HCl = CaCl₂ + H₂O + CO₂↑。
原理二:CO₂ + Ca(OH)₂ = CaCO₃↓ + H₂O,H₂O + CO₂ = H₂CO₃。
3. 实验结论
结论一:二氧化碳密度大于空气密度;二氧化碳不能燃烧也不支持燃烧。
结论二:二氧化碳能使澄清石灰水变浑浊。
结论三:二氧化碳的水溶液会使______试液变红。
4. 实验关键点
(1)实验仪器使用和操作过程的注意事项:长颈漏斗使用的时候需要______。
(2)若选用大理石或石灰石为原料,则不能用稀硫酸。因为生成的硫酸钙是微溶性物质,它包裹在______,从而使反应中止。
(3)收集二氧化碳的时候,集气瓶瓶口朝上,用向上排空气法,导管应伸入到集气瓶底部。若未伸入到集气瓶底部则会使收集到的气体______。
5. 实验拓展
拓展:二氧化碳与氢氧化钠反应没有沉淀、气体、颜色变化等明显现象,只有气压减小这一不易观察的现象。故探究二氧化碳性质时,必须借助其他现象来反映二氧化碳与氢氧化钠发生了反应。
起式:
教材实验:通过瓶内气压变化证明二氧化碳与水发生反应,如图所示。

变式:
(1)使用塑料瓶,观察到塑料瓶变扁,说明瓶内二氧化碳与氢氧化钠发生了反应,如图甲所示。
(2)密闭容器中使用气球,观察气球的变化,如图乙所示。
(3)使用 U 形管,观察反应体系的气压变化,如图丙所示。

(4)使用等量的清水做对比,观察对比进入试管内液体的量确定二氧化碳与氢氧化钠发生反应,如图丁所示。
(5)使用澄清石灰水对通过氢氧化钠的二氧化碳进行检测,如图戊所示。
答案:
3.紫色石蕊
4.
(1)液封
(2)大理石或石灰石表面
(3)不纯
4.
(1)液封
(2)大理石或石灰石表面
(3)不纯
典例 8 [2025·舟山定海区一模]某同学用如图所示的简易装置在实验室制取二氧化碳并验证其性质。

(1)实验室制取二氧化碳,液体 X 应为______。
(2)图示虚线框内,应选用图中的______(选填“A”或“B”)收集装置。
(3)图中铜制燃烧匙可在试管内上下移动,此装置与将大理石直接放入液体 X 中相比,其主要优点是______。
(4)将产生的气体通入石蕊试液中可以观察到的现象是______。

(1)实验室制取二氧化碳,液体 X 应为______。
(2)图示虚线框内,应选用图中的______(选填“A”或“B”)收集装置。
(3)图中铜制燃烧匙可在试管内上下移动,此装置与将大理石直接放入液体 X 中相比,其主要优点是______。
(4)将产生的气体通入石蕊试液中可以观察到的现象是______。
答案:
(1)稀盐酸(或稀HCl)
(2)B
(3)可以控制反应的开始和停止
(4)石蕊试液变红色
(1)稀盐酸(或稀HCl)
(2)B
(3)可以控制反应的开始和停止
(4)石蕊试液变红色
查看更多完整答案,请扫码查看


