第35页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
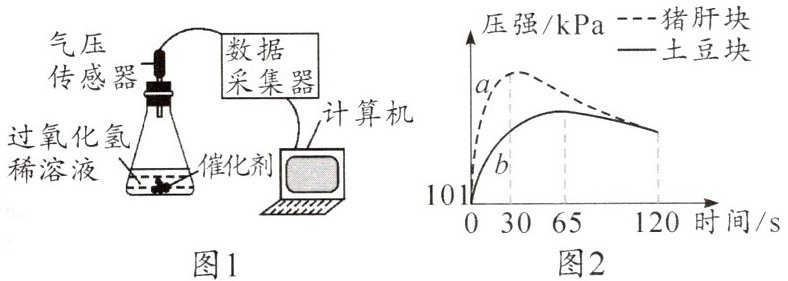
3. [数学化实验](2024·烟台改编)兴趣小组用图1所示装置探究不同催化剂对过氧化氢分解的催化效果。取大小相同的新鲜土豆块和新鲜猪肝块作催化剂,分别加入10mL相同浓度的过氧化氢稀溶液后,用传感器测量装置中气压的变化,如图2中曲线a、b所示。
(1)结合实验和曲线a、b分析,两种催化剂中催化效率更高的是
(2)从曲线a、b的变化可以看出,过氧化氢分解的反应是
(3)曲线a、b最终达到相同的压强,说明
(4)若要证明土豆块、猪肝块是该反应的催化剂,还需要验证它们在化学反应前后的
(1)结合实验和曲线a、b分析,两种催化剂中催化效率更高的是
猪肝块
。(2)从曲线a、b的变化可以看出,过氧化氢分解的反应是
放热
(填“放热”或“吸热”)反应,加猪肝块催化的过氧化氢完全反应所用的时间大约是30
(填“30”“65”或“120”)s。(3)曲线a、b最终达到相同的压强,说明
催化剂只改变化学反应速率,不改变生成物的质量
。(4)若要证明土豆块、猪肝块是该反应的催化剂,还需要验证它们在化学反应前后的
质量
和化学性质
没有改变。
答案:
(1)猪肝块
(2)放热 30
(3)催化剂只改变化学反应速率,不改变生成物的质量
(4)质量 化学性质
(1)猪肝块
(2)放热 30
(3)催化剂只改变化学反应速率,不改变生成物的质量
(4)质量 化学性质
4. (2023·广东改编)[基础实验与跨学科实践]
(1)实验室制取$O_{2}$及性质检验。
①图1中仪器a的名称是
②用过氧化氢制取$O_{2}$应选择图1中的发生装置
③收集一瓶$O_{2}$并进行性质检验。
④[跨学科·物理]做硫在氧气中燃烧实验结束后,取出燃烧匙,立即用玻璃片盖住瓶口并振荡,若将集气瓶倒转,发现玻璃片被“吸住”而不掉下来(如图2),其原因是
(2)制作氧自救呼吸器。
查阅资料: 超氧化钾($KO_{2}$)为黄色固体,可分别与$CO_{2}$、$H_{2}O$反应生成$O_{2}$和白色固体,产氧效率高,适合作生氧剂。
原理分析: $KO_{2}+CO_{2}\to K_{2}CO_{3}+O_{2}$,$KO_{2}+H_{2}O\to KOH+O_{2}$。
动手实践: 设计并制作氧自救呼吸器,如图3所示,使用一段时间后,观察到生氧剂由
(1)实验室制取$O_{2}$及性质检验。
①图1中仪器a的名称是
锥形瓶
。②用过氧化氢制取$O_{2}$应选择图1中的发生装置
B
(填字母),若想控制反应速率,则可将长颈漏斗换为分液漏斗
;反应的文字表达式为过氧化氢$\xrightarrow{二氧化锰}$水+氧气
。③收集一瓶$O_{2}$并进行性质检验。
④[跨学科·物理]做硫在氧气中燃烧实验结束后,取出燃烧匙,立即用玻璃片盖住瓶口并振荡,若将集气瓶倒转,发现玻璃片被“吸住”而不掉下来(如图2),其原因是
二氧化硫与氢氧化钠反应,导致集气瓶内的气压减小,外界大气压将玻璃片“托住”
。(2)制作氧自救呼吸器。
查阅资料: 超氧化钾($KO_{2}$)为黄色固体,可分别与$CO_{2}$、$H_{2}O$反应生成$O_{2}$和白色固体,产氧效率高,适合作生氧剂。
原理分析: $KO_{2}+CO_{2}\to K_{2}CO_{3}+O_{2}$,$KO_{2}+H_{2}O\to KOH+O_{2}$。
动手实践: 设计并制作氧自救呼吸器,如图3所示,使用一段时间后,观察到生氧剂由
黄色变为白色
(填颜色变化)时,则基本失效。
答案:
(1)①锥形瓶 ②B 可将长颈漏斗换为分液漏斗 过氧化氢$\xrightarrow{二氧化锰}$水+氧气 ③c 吸收反应生成的二氧化硫,防止其污染空气 ④二氧化硫与氢氧化钠反应,导致集气瓶内的气压减小,外界大气压将玻璃片“托住”
(2)黄色变为白色
(1)①锥形瓶 ②B 可将长颈漏斗换为分液漏斗 过氧化氢$\xrightarrow{二氧化锰}$水+氧气 ③c 吸收反应生成的二氧化硫,防止其污染空气 ④二氧化硫与氢氧化钠反应,导致集气瓶内的气压减小,外界大气压将玻璃片“托住”
(2)黄色变为白色
查看更多完整答案,请扫码查看


