2025年优化探究同步导学案高中化学选择性必修1人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年优化探究同步导学案高中化学选择性必修1人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第51页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
8.(2023·北京卷,节选)近年研究发现,电催化$CO_2$和含氮物质($NO_3^-$等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的$KNO_3$溶液通$CO_2$至饱和,在电极上反应生成$CO(NH_2)_2$,电解原理如图所示。
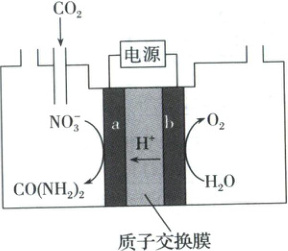
(1)电极 b 是电解池的
(2)电解过程中生成尿素的电极反应是

(1)电极 b 是电解池的
阳
极;(2)电解过程中生成尿素的电极反应是
2NO₃⁻ + 16e⁻ + CO₂ + 18H⁺ = CO(NH₂)₂ + 7H₂O
。
答案:
8.答案:
(1)阳
(2)2NO₃⁻ + 16e⁻ + CO₂ + 18H⁺ = CO(NH₂)₂ + 7H₂O
解析:
(1)电极b上发生H₂O失电子生成O₂的氧化反应,是电解池的阳极。
(2)电极a上硝酸根离子得电子转化为尿素,再由酸性环境可知,电极反应为2NO₃⁻ + 16e⁻ + CO₂ + 18H⁺ = CO(NH₂)₂ + 7H₂O。
(1)阳
(2)2NO₃⁻ + 16e⁻ + CO₂ + 18H⁺ = CO(NH₂)₂ + 7H₂O
解析:
(1)电极b上发生H₂O失电子生成O₂的氧化反应,是电解池的阳极。
(2)电极a上硝酸根离子得电子转化为尿素,再由酸性环境可知,电极反应为2NO₃⁻ + 16e⁻ + CO₂ + 18H⁺ = CO(NH₂)₂ + 7H₂O。
9.(2023·湖南卷,节选)超纯$Ga(CH_3)_3$是制备第三代半导体的支撑源材料之一。近年来,我国科技工作者开发了超纯纯化、超纯分析和超纯灌装一系列高新技术,在研制超纯$Ga(CH_3)_3$方面取得了显著成果。工业上以粗镓为原料,制备超纯$Ga(CH_3)_3$的工艺流程如图1:

已知:①金属 Ga 的化学性质和 Al 相似,Ga 的熔点为$29.8° C$;
②$Et_2O$(乙醚)和$NR_3$(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:

“电解精炼”装置如图2所示,电解池温度控制在$40\sim45° C$的原因是
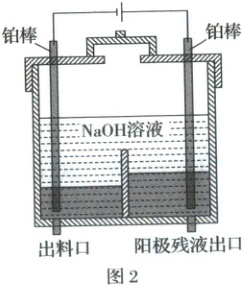
阴极的电极反应为

已知:①金属 Ga 的化学性质和 Al 相似,Ga 的熔点为$29.8° C$;
②$Et_2O$(乙醚)和$NR_3$(三正辛胺)在上述流程中可作为配体;
③相关物质的沸点:

“电解精炼”装置如图2所示,电解池温度控制在$40\sim45° C$的原因是
保证Ga为液体,便于高纯Ga流出
,
阴极的电极反应为
[Ga(OH)₄]⁻ + 3e⁻ = Ga + 4OH⁻
。
答案:
9.答案:保证Ga为液体,便于高纯Ga流出
[Ga(OH)₄]⁻ + 3e⁻ = Ga + 4OH⁻
解析:镓的熔点为29.8℃,电解精炼时温度需高于镓的熔点,电解池温度控制在40~45℃可以保证Ga为液体,便于高纯Ga流出。Ga和Al的性质相似,在强碱性环境中以[Ga(OH)₄]⁻的形式存在,[Ga(OH)₄]⁻在阴极得电子生成Ga,故阴极反应为[Ga(OH)₄]⁻ + 3e⁻ = Ga + 4OH⁻。
[Ga(OH)₄]⁻ + 3e⁻ = Ga + 4OH⁻
解析:镓的熔点为29.8℃,电解精炼时温度需高于镓的熔点,电解池温度控制在40~45℃可以保证Ga为液体,便于高纯Ga流出。Ga和Al的性质相似,在强碱性环境中以[Ga(OH)₄]⁻的形式存在,[Ga(OH)₄]⁻在阴极得电子生成Ga,故阴极反应为[Ga(OH)₄]⁻ + 3e⁻ = Ga + 4OH⁻。
查看更多完整答案,请扫码查看


