2025年优化探究同步导学案高中化学选择性必修1人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年优化探究同步导学案高中化学选择性必修1人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第18页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
1. 加快氧化还原反应的速率


答案:
1.加快
2. 比较金属的活动性强弱


答案:
2.负 正
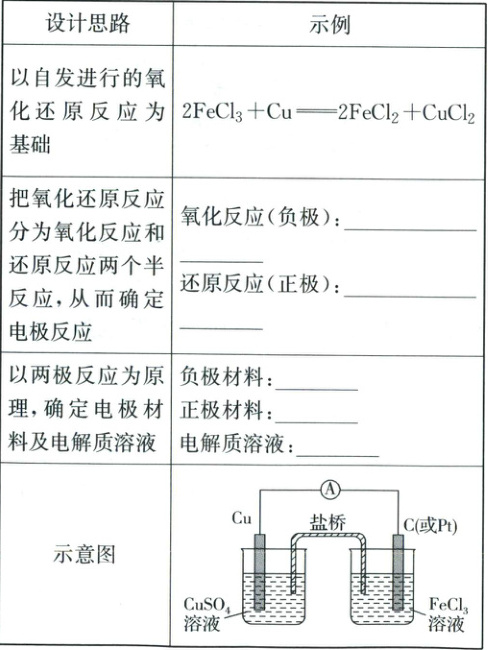
3. 设计原电池
(1)理论上,任何一个自发进行的氧化还原反应都可以设计成原电池。
(2)设计示例
(1)理论上,任何一个自发进行的氧化还原反应都可以设计成原电池。
(2)设计示例

答案:
3.
(2)$\mathrm{Cu}-2 \mathrm{e}^-=\mathrm{Cu}^{2+}$ $2 \mathrm{Fe}^{3+}+2 \mathrm{e}^-=2 \mathrm{Fe}^{2+}$ Cu 石墨(或铂) $\mathrm{FeCl}_3$溶液
(2)$\mathrm{Cu}-2 \mathrm{e}^-=\mathrm{Cu}^{2+}$ $2 \mathrm{Fe}^{3+}+2 \mathrm{e}^-=2 \mathrm{Fe}^{2+}$ Cu 石墨(或铂) $\mathrm{FeCl}_3$溶液
1. 利用原电池原理可以比较金属的活动性强弱,作负极的金属一定比作正极的金属活泼。 (
2. 从理论上讲,任何能自发进行的氧化还原反应都可设计成原电池。 (
3. 增大电解质溶液的浓度,能加快原电池的反应速率。 (
×
)2. 从理论上讲,任何能自发进行的氧化还原反应都可设计成原电池。 (
√
)3. 增大电解质溶液的浓度,能加快原电池的反应速率。 (
×
)
答案:
1.× 2.√ 3.×
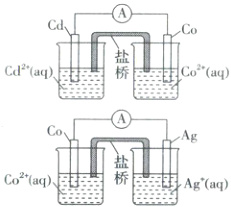
1. 请设计原电池,证明还原性:$Cd$(镉)>$Co$(钴)>$Ag$(银),氧化性:$Ag^+>Co^{2+}>Cd^{2+}$。在下面的方框内画出原电池的装置图(带盐桥),标出原电池的电极材料和电解质溶液。
答案:
1.提示:
1.提示:

2. 运用原电池原理设计实验,验证$I_{2}$、$Fe^{3 + }$氧化性的强弱,请在下面的方框内画出实验装置图(带盐桥)并写出电极反应。
答案:
2. 提示:
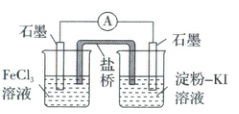
电极反应:
负极:$2I^{-} - 2e^{-} = I_{2}$
正极:$Fe^{3+} + 2e^{-} = 2Fe^{2+}$
2. 提示:

电极反应:
负极:$2I^{-} - 2e^{-} = I_{2}$
正极:$Fe^{3+} + 2e^{-} = 2Fe^{2+}$
1. 要增大锌与盐酸反应的速率,所采取的措施无效的是 (
A.适当提高反应温度
B.增大压强
C.用粗锌代替纯锌
D.增大盐酸浓度
B
)A.适当提高反应温度
B.增大压强
C.用粗锌代替纯锌
D.增大盐酸浓度
答案:
1.B 提高反应的温度,反应的速率加快,故A不符合题意;该反应为溶液中的反应,受压强影响不大,则增大压强,不能增大$\mathrm{Zn}$与盐酸的反应速率,故B符合题意;用粗锌代替纯锌,可以构成原电池,反应速率加快,故C不符合题意;增大盐酸的浓度,氢离子浓度变大,反应速率加快,故D不符合题意。
查看更多完整答案,请扫码查看


