2026年一本密卷高考化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年一本密卷高考化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第68页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
11.(2025·黑龙江·二模)广泛应用于相控阵雷达半导体材料氮化镓有不同的晶型,其中六方氮化镓和立方氮化镓晶胞相互转化关系如图。已知立方氮化镓的晶胞参数为a pm。下列说法正确的是(
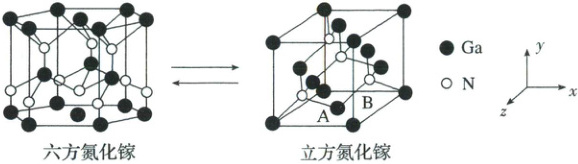
A.六方氮化镓中Ga和N的配位数均为4
B.立方氮化镓中若B原子坐标为(3/4,1/4,1/4),则A原子坐标为(0,1/2,1/2)
C.立方氮化镓中Ga和N的最小核间距为$\sqrt{3}/2$a pm
D.六方氮化镓和立方氮化镓的化学式均为Ga₆N₆
A
)
A.六方氮化镓中Ga和N的配位数均为4
B.立方氮化镓中若B原子坐标为(3/4,1/4,1/4),则A原子坐标为(0,1/2,1/2)
C.立方氮化镓中Ga和N的最小核间距为$\sqrt{3}/2$a pm
D.六方氮化镓和立方氮化镓的化学式均为Ga₆N₆
答案:
11.[答案] A
[解析] A.在六方氮化镓结构中,$Ga$和$N$均采取$sp^3$杂化,形成四面体配位,每个原子周围有4个相邻的异种原子,因此$Ga$和$N$的配位数均为4,A正确;B.在立方氮化镓中,若$B$原子坐标为$(\frac{3}{4},\frac{1}{4},\frac{1}{4})$,$A$原子若为面心立方格子的顶点原子,坐标应为$(0,0,0)$,并不是$(0,\frac{1}{2},\frac{1}{2})$,B错误;C.立方氮化镓中$Ga$和$N$的最小核间距为四面体空隙原子与顶点原子的距离,即体对角线的$\frac{1}{4}$,其距离为$\frac{\sqrt{3}}{4}apm$,而不是$\frac{\sqrt{3}}{2}apm$,C错误;D.晶体化学式需化简呈最简整数比,六方和立方氮化镓中$Ga$与$N$的个数比均为1:1,故它们的化学式应为$GaN$,D错误;故合理选项是A。
[解析] A.在六方氮化镓结构中,$Ga$和$N$均采取$sp^3$杂化,形成四面体配位,每个原子周围有4个相邻的异种原子,因此$Ga$和$N$的配位数均为4,A正确;B.在立方氮化镓中,若$B$原子坐标为$(\frac{3}{4},\frac{1}{4},\frac{1}{4})$,$A$原子若为面心立方格子的顶点原子,坐标应为$(0,0,0)$,并不是$(0,\frac{1}{2},\frac{1}{2})$,B错误;C.立方氮化镓中$Ga$和$N$的最小核间距为四面体空隙原子与顶点原子的距离,即体对角线的$\frac{1}{4}$,其距离为$\frac{\sqrt{3}}{4}apm$,而不是$\frac{\sqrt{3}}{2}apm$,C错误;D.晶体化学式需化简呈最简整数比,六方和立方氮化镓中$Ga$与$N$的个数比均为1:1,故它们的化学式应为$GaN$,D错误;故合理选项是A。
12.(2025·山东·二模)煤焦与水蒸气的反应是煤气化过程中的主要反应,具体反应是C(s)+H₂O(g)⇌CO(g)+H₂(g)。向700K、2L恒容密闭容器中加入1mol C(s)和3mol H₂O(g),测得体系中气体密度(ρ)与时间(t)的关系如图所示(t₂ min时,瞬间缩小容器体积为1L)。下列说法正确的是(
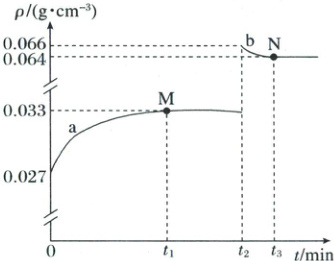
A.M点时,体系已达平衡状态
B.0→t₁ min内,用C(s)表示的平均反应速率为1/2t₁ mol·min⁻¹
C.700K时,该反应的平衡常数K=25/78 mol·L⁻¹
D.N点时,向容器中同时充入1mol H₂O和1mol H₂,则v正大于v逆
A
)
A.M点时,体系已达平衡状态
B.0→t₁ min内,用C(s)表示的平均反应速率为1/2t₁ mol·min⁻¹
C.700K时,该反应的平衡常数K=25/78 mol·L⁻¹
D.N点时,向容器中同时充入1mol H₂O和1mol H₂,则v正大于v逆
答案:
12.[答案] A
[解析] A.$M$点对应$t_1$时刻,此前气体密度$ρ$随时间增大,说明反应正向进行;$t_1~t_2$间$ρ$恒定,表明反应达到平衡,则$M$点体系已达平衡状态,A项正确;平衡时气体密度$ρ = 0.033g/cm^3$,容器体积$2L$,气体总质量$= 0.033g/cm^3×2000cm^3 = 66g$;初始气体质量为$3molH_2O$的质量为$54g$,气体质量增加$12g$,则消耗$1molH_2O$,平衡时$c(H_2O)=1mol/L$,$c(CO)=0.5mol/L$,$c(H_2)=0.5mol/L$,$K=\frac{0.5×0.5}{1}=0.25$,C项错误;用$C(s)$表示的平均反应速率为$\frac{1}{t_1}mol·min^{-1}$,B错误;D.$N$点为缩小体积后新平衡,气体质量$64g$,说明气体减少$2g$,对应逆向生成$\frac{1}{6}mol$的$C$,此时$c(H_2O)=\frac{13}{6}mol/L$,$c(CO)=\frac{5}{6}mol/L$,$c(H_2)=\frac{5}{6}mol/L$,充入$1molH_2O$和$1molH_2$,则$Q=\frac{\frac{5}{6}×\frac{11}{6}}{\frac{19}{6}}≈0.482>0.25$,平衡逆向移动,$v_逆>v_正$,D项错误;答案选A。
[解析] A.$M$点对应$t_1$时刻,此前气体密度$ρ$随时间增大,说明反应正向进行;$t_1~t_2$间$ρ$恒定,表明反应达到平衡,则$M$点体系已达平衡状态,A项正确;平衡时气体密度$ρ = 0.033g/cm^3$,容器体积$2L$,气体总质量$= 0.033g/cm^3×2000cm^3 = 66g$;初始气体质量为$3molH_2O$的质量为$54g$,气体质量增加$12g$,则消耗$1molH_2O$,平衡时$c(H_2O)=1mol/L$,$c(CO)=0.5mol/L$,$c(H_2)=0.5mol/L$,$K=\frac{0.5×0.5}{1}=0.25$,C项错误;用$C(s)$表示的平均反应速率为$\frac{1}{t_1}mol·min^{-1}$,B错误;D.$N$点为缩小体积后新平衡,气体质量$64g$,说明气体减少$2g$,对应逆向生成$\frac{1}{6}mol$的$C$,此时$c(H_2O)=\frac{13}{6}mol/L$,$c(CO)=\frac{5}{6}mol/L$,$c(H_2)=\frac{5}{6}mol/L$,充入$1molH_2O$和$1molH_2$,则$Q=\frac{\frac{5}{6}×\frac{11}{6}}{\frac{19}{6}}≈0.482>0.25$,平衡逆向移动,$v_逆>v_正$,D项错误;答案选A。
13.(2025·甘肃白银·模拟预测)砷盐有用,但亦有毒。古蔡氏法检查砷盐的原理:金属锌与酸作用产生新生态的氢,新生态的氢与药物中微量的砷盐反应,生成具有挥发性的砷化氢气体,砷化氢气体遇溴化汞试纸产生黄色或棕色的砷斑,与一定量标准砷溶液在同样条件下生成的砷斑比较,来判定药物中砷盐的含量。根据该原理,采用如图装置进行砷盐检测,下列说法正确的是(
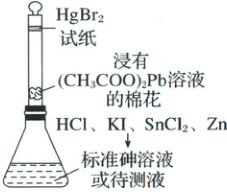
A.在砷盐转化为砷化氢的过程中,锌作催化剂
B.KI、SnCl₂的作用是将五价砷转化为三价砷,由此说明三价砷在锌的作用下更易转化为砷化氢
C.若砷盐中有硫化物杂质,则生成的H₂S遇(CH₃COO)₂Pb反应的离子方程式为Pb²⁺+S²⁻=PbS↓
D.在对照实验中,待测液对应砷斑颜色深于标准溶液,说明待测液中砷含量较低
B
)
A.在砷盐转化为砷化氢的过程中,锌作催化剂
B.KI、SnCl₂的作用是将五价砷转化为三价砷,由此说明三价砷在锌的作用下更易转化为砷化氢
C.若砷盐中有硫化物杂质,则生成的H₂S遇(CH₃COO)₂Pb反应的离子方程式为Pb²⁺+S²⁻=PbS↓
D.在对照实验中,待测液对应砷斑颜色深于标准溶液,说明待测液中砷含量较低
答案:
13.[答案] B
[解析] A.根据题意可知,金属锌与酸作用产生新生态的氢,新生态的氢将砷盐还原为砷化氢,在这过程中,锌作还原剂,A错误;B.+5价的$As$处于最高价,有一定的氧化性,而$AsH_3$中的$As$为 - 3价,因此加入$KI$、$SnCl_2$可将+5价的砷转化为+3价的砷,+3价的$As$再转化为 - 3价的$As$更容易一些,因此+3价的砷在锌的作用下更易转化为砷化氢,B正确;C.$H_2S$、$(CH_3COO)_2Pb$均为弱电解质,不能拆分,C错误;D.砷斑颜色越深,砷含量越高,D错误;故选B。
[解析] A.根据题意可知,金属锌与酸作用产生新生态的氢,新生态的氢将砷盐还原为砷化氢,在这过程中,锌作还原剂,A错误;B.+5价的$As$处于最高价,有一定的氧化性,而$AsH_3$中的$As$为 - 3价,因此加入$KI$、$SnCl_2$可将+5价的砷转化为+3价的砷,+3价的$As$再转化为 - 3价的$As$更容易一些,因此+3价的砷在锌的作用下更易转化为砷化氢,B正确;C.$H_2S$、$(CH_3COO)_2Pb$均为弱电解质,不能拆分,C错误;D.砷斑颜色越深,砷含量越高,D错误;故选B。
查看更多完整答案,请扫码查看


