2026年一本密卷高考化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年一本密卷高考化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第28页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
4. 工业烟气中常含有NOₓ(NO、NO₂)。用NaClO溶液将NOₓ氧化为NO₃⁻,实现烟气中NOₓ的脱除。
(1)NOₓ在大气中会形成酸雨。形成酸雨的过程中,NO表现
(2)向NaClO溶液中加入硫酸,研究初始pH对NOₓ脱除率的影响,结果如下。
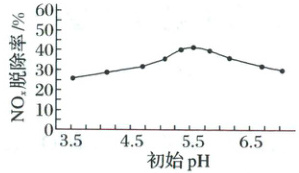
已知:NOₓ脱除率=(脱除前n(NOₓ)-脱除后n(NOₓ))/脱除前n(NOₓ)×100%。
①不用盐酸调节NaClO溶液初始pH的原因是______。
②pH=3.5时NaClO溶液脱除NO的离子方程式(可逆)为
③pH<5.5时,分析NOₓ脱除率随溶液初始pH升高而增大的可能原因:______。
(3)用CrO₃分别将脱除前后的NOₓ全部转化为NO₂,并用库仑仪测定NO₂的量,可计算NOₓ脱除率。库仑仪工作的原理和装置如图:
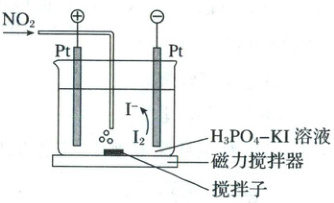
检测前,电解质溶液中的c(I₂)/c(I⁻)保持定值时,电解池不工作。NO₂进入电解池后与I⁻反应,库仑仪便立即自动进行电解,直到c(I₂)/c(I⁻)再次回到原定值,测定结束。通过测定电解消耗的电量可以求出NO₂的物质的量。
①NO₂在电解池中被I⁻还原为NO的离子方程式为______。
②将脱除前、后等体积的烟气分别用上述装置进行测定,电解时转移电子的物质的量分别为amol、bmol。NOₓ脱除率是
③测量结束后,电解池中还检测到少量NO₃⁻和NO₂⁻,这将导致NO₂测定结果
(1)NOₓ在大气中会形成酸雨。形成酸雨的过程中,NO表现
还原
性。(2)向NaClO溶液中加入硫酸,研究初始pH对NOₓ脱除率的影响,结果如下。

已知:NOₓ脱除率=(脱除前n(NOₓ)-脱除后n(NOₓ))/脱除前n(NOₓ)×100%。
①不用盐酸调节NaClO溶液初始pH的原因是______。
②pH=3.5时NaClO溶液脱除NO的离子方程式(可逆)为
2NO + 3HClO + H₂O = 2NO₃⁻ + 3Cl⁻ + 5H⁺
。③pH<5.5时,分析NOₓ脱除率随溶液初始pH升高而增大的可能原因:______。
(3)用CrO₃分别将脱除前后的NOₓ全部转化为NO₂,并用库仑仪测定NO₂的量,可计算NOₓ脱除率。库仑仪工作的原理和装置如图:

检测前,电解质溶液中的c(I₂)/c(I⁻)保持定值时,电解池不工作。NO₂进入电解池后与I⁻反应,库仑仪便立即自动进行电解,直到c(I₂)/c(I⁻)再次回到原定值,测定结束。通过测定电解消耗的电量可以求出NO₂的物质的量。
①NO₂在电解池中被I⁻还原为NO的离子方程式为______。
②将脱除前、后等体积的烟气分别用上述装置进行测定,电解时转移电子的物质的量分别为amol、bmol。NOₓ脱除率是
[(a - b)/a]×100%
。③测量结束后,电解池中还检测到少量NO₃⁻和NO₂⁻,这将导致NO₂测定结果
偏低
(填“偏高”或“偏低”),需进行校正。
答案:
(1)还原
(2)①盐酸具有还原性,能与NaClO反应
②2NO + 3HClO + H₂O = 2NO₃⁻ + 3Cl⁻ + 5H⁺
③脱除NOₓ的反应为2NO + 3HClO + H₂O = 2NO₃⁻ + 3Cl⁻ + 5H⁺ 和 2NO₂ + HClO + H₂O = 2NO₃⁻ + Cl⁻ + 3H⁺,则pH<5.5时随pH升高,氢离子浓度减小,有利于平衡正向移动,从而提高NOₓ脱除率
(3)①NO₂ + 2I⁻ + 2H₃PO₄ = NO + I₂ + 2H₂PO₄⁻ ②[(a - b)/a]×100% ③偏低
(1)还原
(2)①盐酸具有还原性,能与NaClO反应
②2NO + 3HClO + H₂O = 2NO₃⁻ + 3Cl⁻ + 5H⁺
③脱除NOₓ的反应为2NO + 3HClO + H₂O = 2NO₃⁻ + 3Cl⁻ + 5H⁺ 和 2NO₂ + HClO + H₂O = 2NO₃⁻ + Cl⁻ + 3H⁺,则pH<5.5时随pH升高,氢离子浓度减小,有利于平衡正向移动,从而提高NOₓ脱除率
(3)①NO₂ + 2I⁻ + 2H₃PO₄ = NO + I₂ + 2H₂PO₄⁻ ②[(a - b)/a]×100% ③偏低
查看更多完整答案,请扫码查看


