2026年一本密卷高考化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年一本密卷高考化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第30页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
2. 碳酸镧[La₂(CO₃)₃,相对分子质量为458]能抑制人体内磷酸盐的吸收,降低体内血清磷酸盐和磷酸钙的水平,常用于慢性肾衰患者高磷血症的治疗。某课外小组成员进行实验探究La₂(CO₃)₃的制备方法。
已知:①La₂(CO₃)₃难溶于水,易溶于盐酸,溶液pH较高时易生成碱式碳酸镧[La(OH)CO₃,相对分子质量为216]。
②氯化镧(LaCl₃)与易溶的碳酸盐或碳酸氢盐反应可制备La₂(CO₃)₃。
Ⅰ. 利用氯化镧溶液与碳酸氢铵溶液制备碳酸镧(装置如图1,其中夹持装置已略去)。
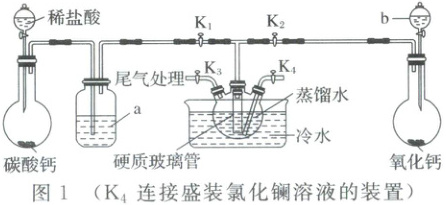
实验步骤如下:
ⅰ. 连接好实验装置,检查装置的气密性,关闭K₁、K₂、K₃和K₄。
ⅱ. 实验时应先打开活塞
ⅲ.
ⅳ. ……,最终制得碳酸镧沉淀。
(1)试剂b的名称是
(2)将操作ⅱ空白处补充完整:______,将操作ⅲ空白处补充完整:______。
(3)实验时,将三颈烧瓶放入冷水中的主要原因是______。
(4)氯化镧溶液与碳酸氢铵溶液反应的化学方程式为______。
Ⅱ. 利用碳酸氢钠溶液与氯化镧溶液制备碳酸镧。
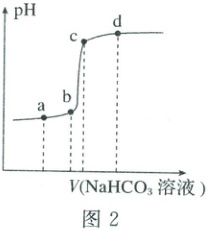
(5)将一定浓度的NaHCO₃溶液滴入氯化镧溶液中,利用手持技术测得氯化镧溶液的pH随加入NaHCO₃溶液的体积的变化如图2。试分析bc段发生pH突变的原因:______。
Ⅲ. 碳酸镧粗产品[设杂质只有La(OH)CO₃]组成的测定。
(6)准确称取6.844g粗产品,溶于10.00mL稀盐酸中,加入10.00mL NH₃ - NH₄Cl缓冲溶液和0.200g紫脲酸铵混合指示剂,用0.5mol·L⁻¹EDTA(Na₂H₂Y)标准溶液滴定至溶液呈蓝紫色(La³⁺ + H₂Y²⁻ = LaY⁻ + 2H⁺),消耗60.00mL EDTA标准溶液。则产品中n(碳酸镧):n(碱式碳酸镧)=
已知:①La₂(CO₃)₃难溶于水,易溶于盐酸,溶液pH较高时易生成碱式碳酸镧[La(OH)CO₃,相对分子质量为216]。
②氯化镧(LaCl₃)与易溶的碳酸盐或碳酸氢盐反应可制备La₂(CO₃)₃。
Ⅰ. 利用氯化镧溶液与碳酸氢铵溶液制备碳酸镧(装置如图1,其中夹持装置已略去)。

实验步骤如下:
ⅰ. 连接好实验装置,检查装置的气密性,关闭K₁、K₂、K₃和K₄。
ⅱ. 实验时应先打开活塞
K₂
(填“K₁”或“K₂”)和K₃,持续通入一段时间气体。ⅲ.
关闭K₂,打开K₁
,继续通入一段时间另一种气体。ⅳ. ……,最终制得碳酸镧沉淀。
(1)试剂b的名称是
浓氨水
,试剂a的作用是除去CO₂中的HCl气体
。装置中硬质玻璃管的作用是防止倒吸
。(2)将操作ⅱ空白处补充完整:______,将操作ⅲ空白处补充完整:______。
(3)实验时,将三颈烧瓶放入冷水中的主要原因是______。
(4)氯化镧溶液与碳酸氢铵溶液反应的化学方程式为______。
Ⅱ. 利用碳酸氢钠溶液与氯化镧溶液制备碳酸镧。
(5)将一定浓度的NaHCO₃溶液滴入氯化镧溶液中,利用手持技术测得氯化镧溶液的pH随加入NaHCO₃溶液的体积的变化如图2。试分析bc段发生pH突变的原因:______。
Ⅲ. 碳酸镧粗产品[设杂质只有La(OH)CO₃]组成的测定。
(6)准确称取6.844g粗产品,溶于10.00mL稀盐酸中,加入10.00mL NH₃ - NH₄Cl缓冲溶液和0.200g紫脲酸铵混合指示剂,用0.5mol·L⁻¹EDTA(Na₂H₂Y)标准溶液滴定至溶液呈蓝紫色(La³⁺ + H₂Y²⁻ = LaY⁻ + 2H⁺),消耗60.00mL EDTA标准溶液。则产品中n(碳酸镧):n(碱式碳酸镧)=
7 : 1
。
答案:
(1)浓氨水 除去CO₂中的HCl气体防止倒吸
(2)K₂ 关闭K₂,打开K₁
(3)防止碳酸氢铵分解,同时降低碳酸镧的溶解度,利于生成沉淀
(4)${2LaCl3 + 6NH4HCO3 = La2(CO3)3↓ + 6NH4Cl + 3H2O + 3CO2↑}$
(5)La³⁺完全沉淀,再滴入NaHCO₃溶液时,碳酸氢根离子水解使溶液的碱性增强,溶液的pH发生突跃
(6)7 : 1
[解析] 在装置中先用浓氨水与生石灰混合发生反应制取NH₃,将氨通入三颈烧瓶中使溶液显碱性。再用石灰石与稀盐酸反应制取CO₂气体,用饱和NaHCO₃溶液除去CO₂中的杂质HCl气体后,通入三颈烧瓶中,在三颈烧瓶中发生反应,得到La₂(CO₃)₃沉淀。
(2)氨在水中溶解度较大,先通入氨,则实验时应先打开活塞K₂和K₃,持续通入一段时间NH₃;然后关闭K₂,打开K₁,继续通入一段时间CO₂。
(6)根据La³⁺ + H₂Y²⁻ = LaY⁻ + 2H⁺得关系式:La³⁺ ~ H₂Y²⁻,n(H₂Y²⁻) = 0.5mol·L⁻¹ × 0.060L = 0.03mol,则n(La³⁺) = 0.03mol,设La₂(CO₃)₃为xmol,La(OH)CO₃为ymol,则2x + y = 0.03,458x + 216y = 6.844,解得x = 0.014,y = 0.002,n(碳酸镧) : n(碱式碳酸镧) = 0.014 : 0.002 = 7 : 1。
(1)浓氨水 除去CO₂中的HCl气体防止倒吸
(2)K₂ 关闭K₂,打开K₁
(3)防止碳酸氢铵分解,同时降低碳酸镧的溶解度,利于生成沉淀
(4)${2LaCl3 + 6NH4HCO3 = La2(CO3)3↓ + 6NH4Cl + 3H2O + 3CO2↑}$
(5)La³⁺完全沉淀,再滴入NaHCO₃溶液时,碳酸氢根离子水解使溶液的碱性增强,溶液的pH发生突跃
(6)7 : 1
[解析] 在装置中先用浓氨水与生石灰混合发生反应制取NH₃,将氨通入三颈烧瓶中使溶液显碱性。再用石灰石与稀盐酸反应制取CO₂气体,用饱和NaHCO₃溶液除去CO₂中的杂质HCl气体后,通入三颈烧瓶中,在三颈烧瓶中发生反应,得到La₂(CO₃)₃沉淀。
(2)氨在水中溶解度较大,先通入氨,则实验时应先打开活塞K₂和K₃,持续通入一段时间NH₃;然后关闭K₂,打开K₁,继续通入一段时间CO₂。
(6)根据La³⁺ + H₂Y²⁻ = LaY⁻ + 2H⁺得关系式:La³⁺ ~ H₂Y²⁻,n(H₂Y²⁻) = 0.5mol·L⁻¹ × 0.060L = 0.03mol,则n(La³⁺) = 0.03mol,设La₂(CO₃)₃为xmol,La(OH)CO₃为ymol,则2x + y = 0.03,458x + 216y = 6.844,解得x = 0.014,y = 0.002,n(碳酸镧) : n(碱式碳酸镧) = 0.014 : 0.002 = 7 : 1。
查看更多完整答案,请扫码查看


