2026年一本密卷高考化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年一本密卷高考化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第12页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
7.磷酸属于中强酸,当反应底物为强酸环境下容易降解的物质时,磷酸有机溶剂更有利于反应的发生。某
团队选择85%磷酸甲苯体系研究化合物Q脱Boc(叔丁氧羰基)的反应,如图所示。下列说法正确的是
(

A.化合物Q分子中碳原子杂化方式有3种
B.化合物Q在酸性条件下完全水解,最终可生成2种有机物
C.基态P原子核外电子的空间运动状态有15种
D.1molR在Cu或Ag作用下发生反应可生成含有醛基的有机物
团队选择85%磷酸甲苯体系研究化合物Q脱Boc(叔丁氧羰基)的反应,如图所示。下列说法正确的是
(
B
)
A.化合物Q分子中碳原子杂化方式有3种
B.化合物Q在酸性条件下完全水解,最终可生成2种有机物
C.基态P原子核外电子的空间运动状态有15种
D.1molR在Cu或Ag作用下发生反应可生成含有醛基的有机物
答案:
7.[答案] B
[解析]

化合物Q分子中含有2个酯基、1个酰胺基,在酸性条件下完全水解,即从虚线处断裂,最终可得到2种有机物和H₂CO₃,B正确。饱和碳原子为sp³杂化,化合物Q分子中碳原子杂化方式有2种,A错误。苯环、碳氧双键、碳碳双键中的碳原子均为sp²杂化。连有羟基的碳原子上没有氢原子,不能发生催化氧化反应,不会生成醛基,D错误。基态P原子的核外电子排布式为1s²2s²2p⁶3s²3p³,其核外电子占据9个轨道,故基态P原子核外电子的空间运动状态有9种,C错误。
7.[答案] B
[解析]

化合物Q分子中含有2个酯基、1个酰胺基,在酸性条件下完全水解,即从虚线处断裂,最终可得到2种有机物和H₂CO₃,B正确。饱和碳原子为sp³杂化,化合物Q分子中碳原子杂化方式有2种,A错误。苯环、碳氧双键、碳碳双键中的碳原子均为sp²杂化。连有羟基的碳原子上没有氢原子,不能发生催化氧化反应,不会生成醛基,D错误。基态P原子的核外电子排布式为1s²2s²2p⁶3s²3p³,其核外电子占据9个轨道,故基态P原子核外电子的空间运动状态有9种,C错误。
8.氢能是一种极具发展潜力的新型清洁能源,储氢材料的发展对氢气的高效存储至关重要。TiFe合金是
近年备受关注的新型储氢合金,氢气在合金表面分解为氢原子,并进入金属原子形成的空隙中。TiFee
合金的一种储氢过程如图所示。下列说法不正确的是 (
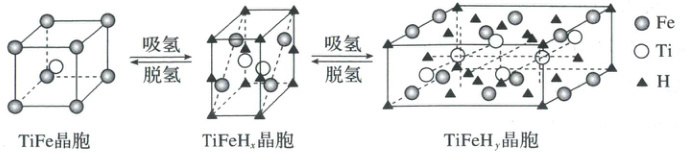
A.Ti与Fe在元素周期表中均位于d区
B.TiFe晶体中每个Fe周围与其距离相等且最近的Ti有8个
C.1molTiFe完全转化为TiFeHy时,可以吸收标准状况下11.2yLH2
D.已知TiFe合金吸氢过程放热,则提高TiFe储氢率的措施有升高温度、增大H2分压
近年备受关注的新型储氢合金,氢气在合金表面分解为氢原子,并进入金属原子形成的空隙中。TiFee
合金的一种储氢过程如图所示。下列说法不正确的是 (
D
)
A.Ti与Fe在元素周期表中均位于d区
B.TiFe晶体中每个Fe周围与其距离相等且最近的Ti有8个
C.1molTiFe完全转化为TiFeHy时,可以吸收标准状况下11.2yLH2
D.已知TiFe合金吸氢过程放热,则提高TiFe储氢率的措施有升高温度、增大H2分压
答案:
8.[答案] D
[解析] 基态Ti原子的价层电子排布式为3d²4s²,基态Fe原子的价层电子排布式为3d⁶4s²,Ti与Fe在元素周期表中均位于d区,A正确。由题图TiFe晶胞结构可知,该晶体中每个Ti被8个Fe所形成的立方体包围,每个Fe亦被8个Ti所形成的立方体包围,即TiFe晶体中每个Fe周围与其距离相等且最近的Ti有8个,B正确。根据氢元素守恒可得,1molTiFe完全转化为TiFeH_y可以吸收y mol H原子,即标准状况下11.2y LH₂,C正确。由题意可知,TiFe合金吸氢形成金属氢化物的过程放热,升高温度,平衡会向吸热反应方向移动,即向金属氢化物脱氢的方向移动,导致合金中储存的氢减少,即TiFe储氢率降低;增大H₂的分压,相当于增大反应物的浓度,平衡会向正反应方向移动,即有利于合金吸收氢气形成金属氢化物,从而提高TiFe储氢率,D错误。
[解析] 基态Ti原子的价层电子排布式为3d²4s²,基态Fe原子的价层电子排布式为3d⁶4s²,Ti与Fe在元素周期表中均位于d区,A正确。由题图TiFe晶胞结构可知,该晶体中每个Ti被8个Fe所形成的立方体包围,每个Fe亦被8个Ti所形成的立方体包围,即TiFe晶体中每个Fe周围与其距离相等且最近的Ti有8个,B正确。根据氢元素守恒可得,1molTiFe完全转化为TiFeH_y可以吸收y mol H原子,即标准状况下11.2y LH₂,C正确。由题意可知,TiFe合金吸氢形成金属氢化物的过程放热,升高温度,平衡会向吸热反应方向移动,即向金属氢化物脱氢的方向移动,导致合金中储存的氢减少,即TiFe储氢率降低;增大H₂的分压,相当于增大反应物的浓度,平衡会向正反应方向移动,即有利于合金吸收氢气形成金属氢化物,从而提高TiFe储氢率,D错误。
查看更多完整答案,请扫码查看


